ニーマンピック病はスフィンゴミエリナーゼと呼ばれる酵素が欠損する病気で、最も重いものでは早くから進行性の脳障害をきたす病気だ。酵素活性がある程度残っている患者さんでは、脳は正常だが、スフィンゴミエリンの蓄積によるライソゾーム機能異常により、肝臓脾臓腫大、呼吸機能低下が起こる。最近、この酵素を注射すると体の様々な臓器に取り込まれて、リソゾーム機能が回復することが示され、脳障害のない子供を治療する治験が進んでいる。しかし、酵素は脳に到達できないので、脳症状は遺伝子治療が最も近道と考えられてきた。
実際、モデル動物を用いて脳に直接アデノ随伴ウイルスベクターに組み込んだ遺伝子を注射する研究が行われてきたが、ウイルスベクターが万遍なく脳に広がらないため、局所的にスフィンゴミエリナーゼの発現が高くなりすぎ、その結果スフィンゴミエリンの分解物が強い炎症を引き起こすという問題が立ちはだかっていた。
これに対し、カリフォルニア大学サンフランシスコ校の研究グループは、この問題をアデノウイルスに組み込んだスフィンゴミエリナーゼ遺伝子を小脳延髄槽に注入することで解決できることを示し、この病気の遺伝子治療を一歩進めることに成功した。(Samaranch et al, Adeno-associated viral vector serotype 9–based gene therapy for Niemann-Pick disease type A Science Translational Medicine 11, eaat3738).
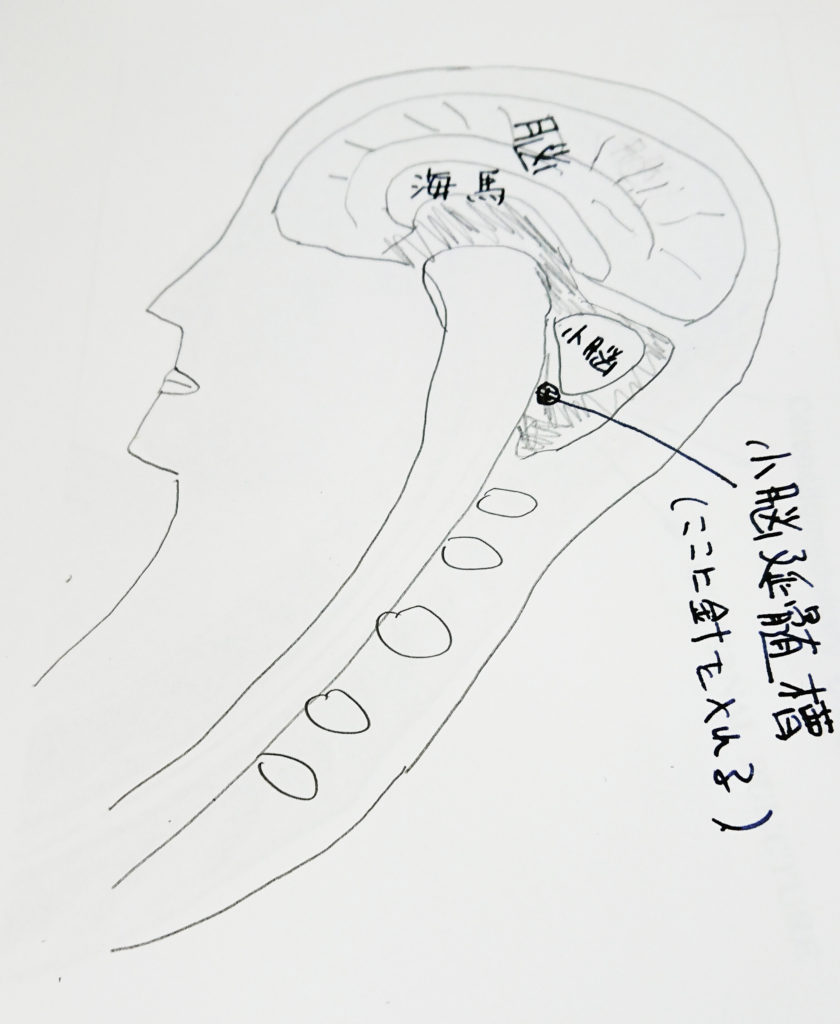
この研究のミソは、向神経性の強いアデノ随伴ウイルスベクター(AAV9)を用いたことと、図に示したように小脳と延髄の間にある脳室にウイルスを注射した点にある。
詳細は全て省くが、私が理解した限り、マウスでは小脳だけでなく、海馬から皮質に至るまで神経細胞とグリア細胞の両方にスフィンゴミエリナーゼを発現させることに成功し、運動機能、記憶機能の回復とともに、通常30週ぐらいで始まる死亡を完全に抑制することに成功している。
もちろん同じプロトコルが人間で有効かどうかはやってみないとわからないが、脳症状については根本的治療方法がない現状で、一刻も早く実際の治験に進んで欲しいと思う。マウスでの前臨床データから見る限り、臨床治験に進むのを躊躇する理由は見当たらない。そして、ぜひ現実的な価格で治療を受けられるようにして欲しいと思う。



アデノウイルスに組み込んだスフィンゴミエリナーゼ遺伝子を小脳延髄槽に注入することで解決し、この病気の遺伝子治療を一歩進めることに成功した。
Imp
今回は遺伝子治療の話題。
アメリカ政府は遺伝子治療を積極的に進める方針だとか。
21世紀です。