2021年5月28日
今回から少し難しい内容になりますがご容赦ください。
これまで、1)自閉症スペクトラム(ASD)特異的に見られる102個の遺伝子突然変異を特定した論文(https://aasj.jp/news/autism-science/15576 )、そして、2)このリストの中の遺伝子変異が脳発生に関わっていることを、カエルやヒトiPSを用いて示した研究(https://aasj.jp/news/autism-science/15595 )をとりあげて、最新のゲノム研究がASDにどう迫っているかを紹介してきた。
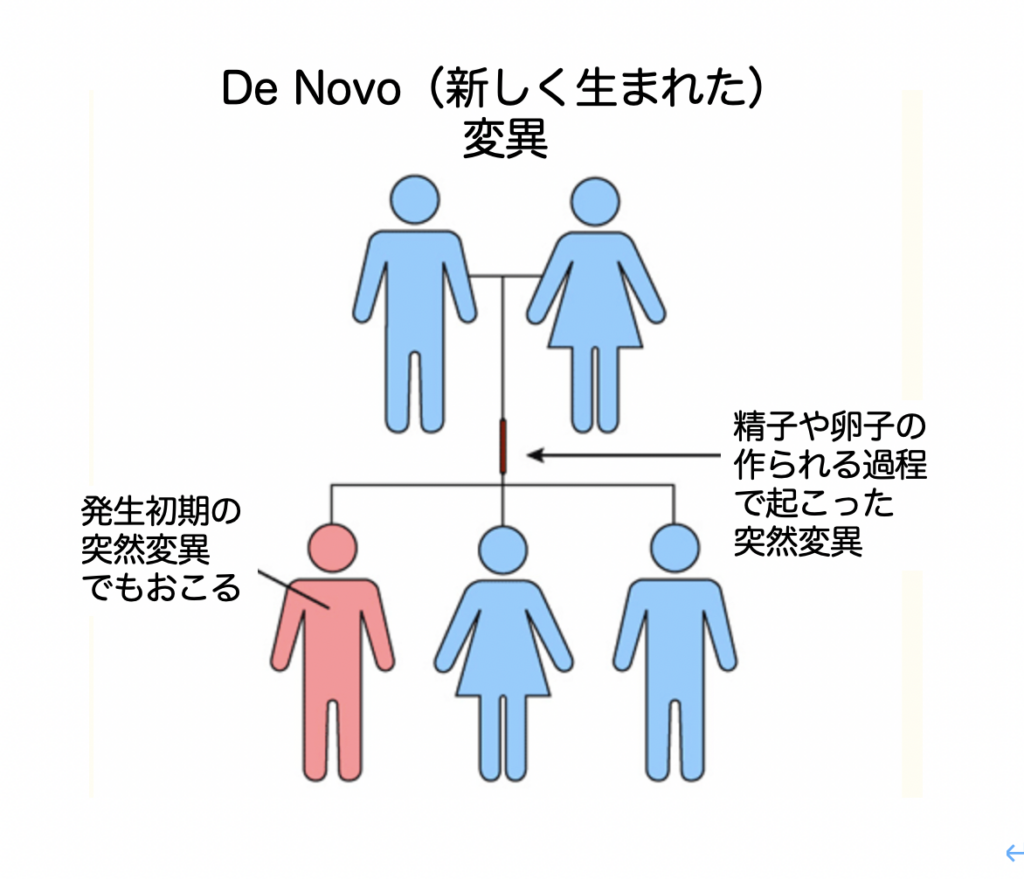
この2編の論文で研究された遺伝子の多くは、de novo変異と呼ばれ、親から伝わった遺伝子変異ではなく、多くは親の精子や卵子の発生過程、場合により本人自身の初期の発生過程で起こってきた変異で、これが脳ネットワーク形成に影響を及ぼし、ASD発症の決定的後押しをしていると考えられるようになってきた(図1)
図からわかるように、このようなde novoの変異を特定するためには、ASD本人で見られた遺伝子変異が、親兄弟には存在しないという消去法を用いざるを得ない。逆に、de novoの変異が本当に発生していることを示そうと思うと、1)精子や卵子の発生過程、2)受精卵からの個体発生の過程に焦点を当て、ASDに関わるレア変異が起こっていることを示す必要がある。
ところが、例えば精子形成過程でASDに関わる変異が起こることは理論的には予想できても、実際に起こっていることをDNA解析で示すのは簡単ではない。というのも、もともとDNA解析には読み間違いが伴うため、何度も読み直してコンセンサスを取ることで、正しい配列を決めるように設計されている。例えば変異が1%の確率で見られるとしても、それを遺伝子解析時の読み間違いとして見落とす可能性があった。
幸いシークエンサーの精度が上がったおかげで、例えば200回繰り返し読んだ時、2%以上の頻度で現れる変異の場合は、読み間違えではないと認定できるようになってきた。これを利用して、ASD児の父親から提供を受けた精子ゲノムを解析し、父親の精子形成で発生した結果、子供に伝達されたde novoの変異を探したのが、最初に紹介する論文だ。
この研究では、ASD児を持つ8家族について、ASD児にのみ見られるde novo変異を912種類特定し、この変異をお父さんの血液や、精子で見つけることができるかを調べている。
もし変異がお父さんの発生途上で生じた場合は、精子だけでなく血液細胞にも見られる。一方精子だけに認められる場合は、精子の元の細胞が他の細胞から分かれた発生後期に変異がおこったと考えられる。一方、精子を作る元の細胞から精子細胞ができる場合にも変異は起こるが、これは頻度が低く、200回繰り返してゲノム配列を読んだ程度では見つけることは難しい。
事実特定されたde novoの912変異のうち、父親由来の染色体上の変異はほぼ半分の501個で、そのうち20種類が父親の精子あるいは血液で発見されている。すなわち、大半のde novoの変異では発生時期を特定できないが、少なくとも4%では、確かに父親の精子形成過程でde novoの変異が発生したことが確認されたことになる。さらにASD児に見られるのと同じ変異が、今回の調べた精子にも存在していることは、この変異が精巣内の精子を作る幹細胞に存在し、持続的に変異精子を作り続けていることを示している(このような状況を変異と正常のモザイク状態と呼んでいる)。
このような変異の多くは、ASD発症に重大な影響を及ぼす変異であることも確認しており、これまで2回にわたって述べてきたように、ASDの発症にde novo変異が大きな役割を負っていることが確認された。このように発生過程で起こった変異は、父親の精子として常に作り続けられるが、幸いほとんどはその頻度は低く、繰り返し子供に伝達されるリスクは低い。しかし今回特定された20変異のうち2変異は、それぞれ14.7%および8.9%という高い頻度のモザイクになっており、これほど高い頻度で存在すると、一定の確率で子供に伝達されることが予想される。
このような場合、同じ変異は精子だけでなく、血液でも見られることから、父親の発生初期過程で起こった変異で、多くの組織に同じ変異を持つ細胞が分布していることが予想できる。
これ以上詳しくは説明しないが、de novoの変異の一部は、親の生殖細胞発生過程のどこかで生じたもので、発生初期に発生した変異ほど、複数の子供に伝達される危険が高いことがわかる。以上の結果から、ASD児のde novoの変異を特定し、同じ変異が父親の精子(母親では同じ検査はできない)で見られる頻度を確かめることで、変異が子供に繰り返し伝達されるリスクがわかることを示唆している。
以上は通常の遺伝形式でなくても、de novoの変異が父親の発生過程で起こり、組織内で変異細胞のモザイク状態が形成されると、de novoの変異として子供に伝達されることを示している。もちろん父親だけでなく、母親の卵子形成過程でも同じことが起こっていい。
これに対し、父親の精子にも、母親の卵子にも、問題になるde novoの変異がなくとも、子供の初期発生過程でde novoの変異が起こり、それが脳細胞で発現して、ASD発症に寄与する可能性も存在する。
この可能性を調べたのがボストン小児病院からの論文だ。
ASDは高次脳機能に関わる状態なので、この研究ではASDと診断され、何らかの理由で亡くなった方59人の脳組織について、全ゲノムを250回繰り返し読むことで、子供の発生過程で起こったde novoの変異が、脳で働いてASDの原因になる可能性を調べている。この精度で遺伝子配列を読んだ場合、受精卵が5-6回分裂して32-64細胞に達するまでに起こった変異であれば、de novoの変異として検出できる。
ASD、正常を問わず一定の確率(一回の細胞分裂あたり2−3変異)でde novoの変異は生じる。変異をさらに詳しく調べると、正常人でも50%で、機能が障害される変異を持つ細胞が2%以上の確率で存在することもわかる。すなわち、正常の脳など存在しないことがわかる。
しかし、変異の性質を調べていくと、ASDの脳では、脳機能に関わる遺伝子の発現に関わる遺伝子の変異の頻度が多いことも明らかになった。すなわち、脳の発生過程でたまたまこのような変異が起こってしまうと、ASDのリスクが高まることを示している。結果、ASDの人を調べると、症状につながる変異の頻度が高まっていることになる。
以上が結果で、前回2回に分けて紹介したde novoの変異が、どのように発生するのかが分かってもらえたのではないだろうか。DNAシークエンサーの進展により、これまでほとんど不可能だったレベルのASDゲノム研究が可能になっているのをみると感慨が深い。
次回は、変異の中でも、特に最近注目されてきたTandem Repeat(縦列反復)のリスクについての論文を紹介する。
2021年5月6日
数万人規模で自閉症スペクトラム(ASD)とその家族のエクソーム(翻訳されて機能的タンパク質をコードする遺伝子部分)を比べた研究により、家族には存在せずASDの人だけに発見され、おそらくASD発症を強く後押ししていると推察される遺伝子変異が102種類発見されたことを、前回紹介した(https://aasj.jp/news/autism-science/15576 )。
1)家族には見られず、ASDの人にだけ発見されること、2)そのほとんどが脳組織で発現していることから、 ASD発症に関わる可能性はかなり高いと言えるが、残念ながら状況証拠を超えない。刑事ドラマに例えると、一つ一つの分子について、しっかりと「裏を取って証拠固めをしないと、起訴には持ち込めない」段階だ。では、どのように証拠固めをすればいいのか。今日から、2回に分けて、そんな証拠固めのしかたについて紹介していくことにする。
今日紹介するカリフォルニア大学サンフランシスコ校からの論文は、まさに前回紹介した研究に啓発され、見つかった遺伝子の機能を特定しようとした研究で、現時点で可能な証拠固め実験の典型とも言える論文だ。
説明の前に、ある遺伝子がASD発症に関わることを示すためにはどうすればいいのか考えてみよう。
ゲノム研究から、同じ遺伝子の変異が、1)複数のASD患者さんで発見され、2)患者さん以外には発見されないとすると(すなわち前回紹介した論文)、この遺伝子がASD発症に関わると決めるための強い証拠と言っていい。ただこれだけでは、どのような過程を経てその変異がASD発症につながるのかを理解したことにはならない。このためには、それぞれの分子の機能を細胞レベル、組織レベルで調べる必要がある。
すなわち遺伝子変異からASD発症までには、遺伝子情報から変異タンパク質への翻訳、変異分子により生じる細胞変化、細胞レベルの変異による脳のネットワークの変化、そして最終的に行動変容と続く複雑な過程があり、この理解が必要になる。
幸い現在では、ASD患者さんで発見されたのと同じ遺伝子変異を導入した実験動物を作成することは可能で、モデル動物レベルではあるが、この過程を詳しく調べる方法は確立している。時間はかかっても、発見された102種類の遺伝子変異を、細胞レベル、脳組織レベル、そして行動レベルと調べていけば、時間はかかるが102通り(おそらく同じ経路に異なる分子が関わっているので、実際にはもっと少ない)のASD発症への道を理解し、うまくいけば治療法の開発まで進める可能性はある。
しかし、せっかちはどこにでもいるものだ。特に研究者には多い。一つずつ総当たりなどと悠長なことを言わず、102種類の中から優先順位をつけて研究スピードを上げられないか調べたのが今日紹介する研究者たちだ。
まず彼らの基準で選んだASDとの相関確率の高い遺伝子トップ10種類選んで(前回紹介した論文のリストには、このうち7種類がトップ10に入っている)、スピード重視でこれら遺伝子の機能を同時並行的に調べる可能性を探っている。
そこで登場したのがアフリカツメガエルだ。最近この動物を用いた発生研究は下火になっているが、一時は発生学=カエルの研究と言っていいほど重要なモデル動物だった。なぜカエルを持ち出してきたかと言うと、複雑だったアフリカツメガエルのゲノム解読が終わり、さらに昨年ノーベル賞に輝いたクリスパー技術を使うことで、この動物でも遺伝子操作が可能になったことが大きい。
実際には、受精卵が一回分割したところで、片方だけの遺伝子をノックアウトしている。カエルの場合、最初の分割でできた細胞は、左右の体に別れて発生するので、同じ個体で、遺伝子を変異させた側と、正常側を比べて、脳発生での遺伝子の機能を知ることができる。
クリスパー技術のおかげで、ガイドと呼ばれる標的遺伝子に対応するRNAを必要数用意しておけば、一度に10種類の遺伝子ノックアウトの効果を流れ作業で調べることができる。しかも、アフリカツメガエルの脳が発生するまでの時間は5日もあれば十分だ。
結果は驚くべきものだった。10種類の遺伝子全てで、機能欠損させた方の脳の大きさが変化する。遺伝子により大きくなる場合もあるし、逆に小さくなるケースもある。すなわち、遺伝子ごとに作用は異なるが、いずれも脳の初期発生に関わっていることがわかる。もう少し細胞レベルで詳しく調べると、全ての遺伝子で、未分化な増殖細胞の比率が、成熟した神経細胞と比べて上昇していることがわかった。すなわち、未熟細胞の増殖が続いて、神経細胞の成熟が遅れていることがわかる。
調べた10種類の遺伝子でほぼ同じ結果が得られたとは、大変わかりやすい結果だ。しかしカエルで脳発生の異常を誘導できたからと言って、同じことがそのままヒトでも言えるとは限らない。
ここで登場するのが、山中さんたちが開発したiPSだ。カエルと比べるとちょっと時間はかかるが、ヒトiPSで遺伝子機能を欠損させた後、神経細胞まで試験管内で分化させ、様々なことを調べることができる。
10種類の遺伝子全ては調べるのは大変なので、とりあえず5種類の遺伝子の機能を欠損させたiPSから神経細胞を誘導してみると、カエルと同じで増殖する未分化細胞が増え、成熟した細胞が減っていることがわかった。
以上のことから、人間でもASD患者さんだけに見られるde novoの変異があると、未分化細胞の増殖が高まり、成熟細胞が減っているのではと推察できる。
実を言うと、この結果はある程度予想されていた。例えば以前紹介したように、一部のASD患者さんでは脳体積の増加が見られることが知られている(https://aasj.jp/news/watch/6509 )。さらに、遺伝子変異は特定できていないASD患者さんのiPSから神経細胞を誘導すると、たしかに未分化細胞の増殖が長く続いて、神経細胞成熟が遅れることも報告されている(https://aasj.jp/news/watch/3774 )。
詳しくは述べないが、今回明らかにした10種類の遺伝子の脳での発現や機能を基盤にして、前回紹介した102種類の遺伝子の相互関係をコンピュータで調べると、なんと98種類の分子を一つのネットワークにまとめることができること、そしてその多くが未分化な神経細胞が存在するsub-ventricular zoneでネットワークを作っていることも明らかにしている。
以上、完全に理解していただけたか少し不安だが、ゲノム研究で発見されたASDに強く関わる遺伝子が、神経発生時期に、細胞の増殖と分化に関わっており、この遺伝子の変異で、少し未分化細胞が増えすぎて、成熟が抑えられると結論できる。もちろん、同じような解析を続ければ、ASDで変化が起こる他の過程もわかるだろう。
以上の結果で十分面白いと思うが、この論文の著者らはさらにせっかちで意欲的だ。解析した中からDYRK1A遺伝子を選び、この遺伝子が欠損したカエルの脳発生異常を治療できる薬剤をスクリーニングしている。その結果、なんと女性ホルモン(エストロジェン)が、神経細胞の増殖に必要なシグナル分子shhを抑えて、脳の異常を正常化することまで示し、胎児期のエストロジェンで発生異常の一部を直せるかもしれないと結論している。カエルでもうまく使うと、ASD治療のヒントが得られると言うわけだ。
ゲノム研究での発見をできるだけ早く治療開発にまで結びつけたいと言う気持ちが伝わる力作だが、読者の皆さんにとっても、研究の流れを理解する格好の例になったのではと期待する。
次回は、ASD患者さんだけで発生するde novoの変異を、人間でどう研究すしたらいいのかについての論文を紹介する。
2021年5月4日
自閉症の科学再開の手始めは、マスク着用についての論文で、一般の人にも理解しやすいテーマだった(https://aasj.jp/news/autism-science/15523 )。
これに対し、今日から何回かに分けて紹介したいと思っている領域は、自閉症スペクトラム(ASD)のゲノムについての研究領域で、おそらく、日々ASDと向き合っておられる臨床の先生方でも理解しづらい領域だと思う。それでもこの分野は最近急速な進展を見せており、ASD理解には避けては通れない。そこで、この分野の進展をできるだけわかりやすく紹介して、この進歩を感じ取って欲しいと思っているが、はっきりいって自信はない。わかりにくい点があれば、遠慮なくメールで質問して欲しい。
さて、今回のコロナ禍が始まったばかりの頃、「自閉症とゲノム」と言う講義を配信した(https://www.youtube.com/watch?v=wVrq5COGwcY&t=427s )。今回はこの時紹介した論文から始めようと思っているが、このYouTubeを見ていただいた北山さんから、「自閉症は遺伝子の多様性とごまかしてみても、変異体なのですね 」という、胸にグサッとくるコメントをもらった。
考えてみると、ゲノムにしても遺伝にしても、生物の違いを追求する学問で、いくら差別的な言い回しを避けようとしても、この領域では区別や差別を避けて通れない。かわりに、ASDを遺伝的に区別する研究の意義をよく説明していく以外方法はない。
ASD に限らず、今の医学で、病気に関わる遺伝子の変化を発見することの意味は大きい。例えばガンを考えて見よう。普通、身体の細胞はむやみやたらと増えないように制御されている。ガンではこの制御が効かない点で、普通の細胞と区別 区別 区別 区別 区別
ガンと比べると、ASDは、脳の神経ネットワーク形成というまだまだ科学及ばない領域の多い超複雑な過程の結果として現れる変化だ。だからこそ、確実な区別、すなわち遺伝学的な違いを求め、それを手がかりに複雑な過程を攻めることが重要になる。また、ASD発症に関わる具体的遺伝子が少しづつわかってくると、ASDの違いが脳発生の早い時期から見られることがわかってきた(これについてはこのシリーズで紹介していく)。
さて、ここまでASDのゲノムや遺伝子といった言葉を使ってきたが、少し説明が必要だ。一般的には遺伝子やゲノムと聞くと、親から子へと伝わる遺伝情報を思い浮かべるのが普通だが、ASDの発症に関わる遺伝子というとき、必ずしも親から子供へと伝達される遺伝情報を意味しない。すなわち、ガンと同じように、患者さんだけで新たに起こった変異(de novo変異)がASDの発症に大きな役割を演じていることが最近わかってきた。
もちろんAutism(自閉症)という診断名を提唱したカナーが述べているように、ASDの患者さんと同じ性質は親にも見られることが多く、また一卵性双生児でASDになる一致率は、10倍以上高まることから、親から子へと伝達できる生殖細胞レベルの遺伝要因が関わることは間違いがない。
事実、ゲノム研究が可能になった最初の頃の研究は、ほとんど親から子へと伝わる生殖細胞系列の変異に焦点が絞られていた。しかし最初のゲノム研究からASDと相関するとして発見された多くの変異は、ASDに特異的とは言えない変異が多かった。すなわち、正常人にも一定の確率で見られるため、変異というより、人間集団に見られる多様性の一つと考えることができる。そのことから、普通に見られるという意味で、コモン変異と呼んでいる。
ただ最近では、親から子へと伝わるコモン変異だけではASD発症には至らず、ASD発症を後押しする新たに起こった遺伝子変異が、ASD発症に必要ではないかと考えられるようになった。このような変異は稀にしか起こらず、普通、正常人では見つからないレア変異だ。
両親兄弟には存在しない変異がどうしてASDで見つかるのか不思議に思われるかもしれない。ただ、先に述べたガンのケースと同じで、母親の卵子、父親の精子ができる過程で起こる突然変異は、子供だけにしか現れないし、受精後でも早い段階で起こった突然変異は、多くの細胞に影響を及ぼし、結果として個体レベルで異常の原因になる。事実、このような変異はASD に限らず、多くの遺伝子の病気で見ることができる。ぜひ、親から子へと遺伝する病気と遺伝子の病気とは、必ずしも同じでないことを覚えておいて欲しい。
ではこのようなレア変異の重要性はどうしてわかってきたのだろうか?
実はこの背景に、ゲノム解読コストが下がり、病気の有無にかかわらず、詳しいゲノム解析が行われた人の数が急速に増加したこととがある。すなわち、調べる対象者の数を増やせば、当然稀なレア変異が見つかる確率は上がる。
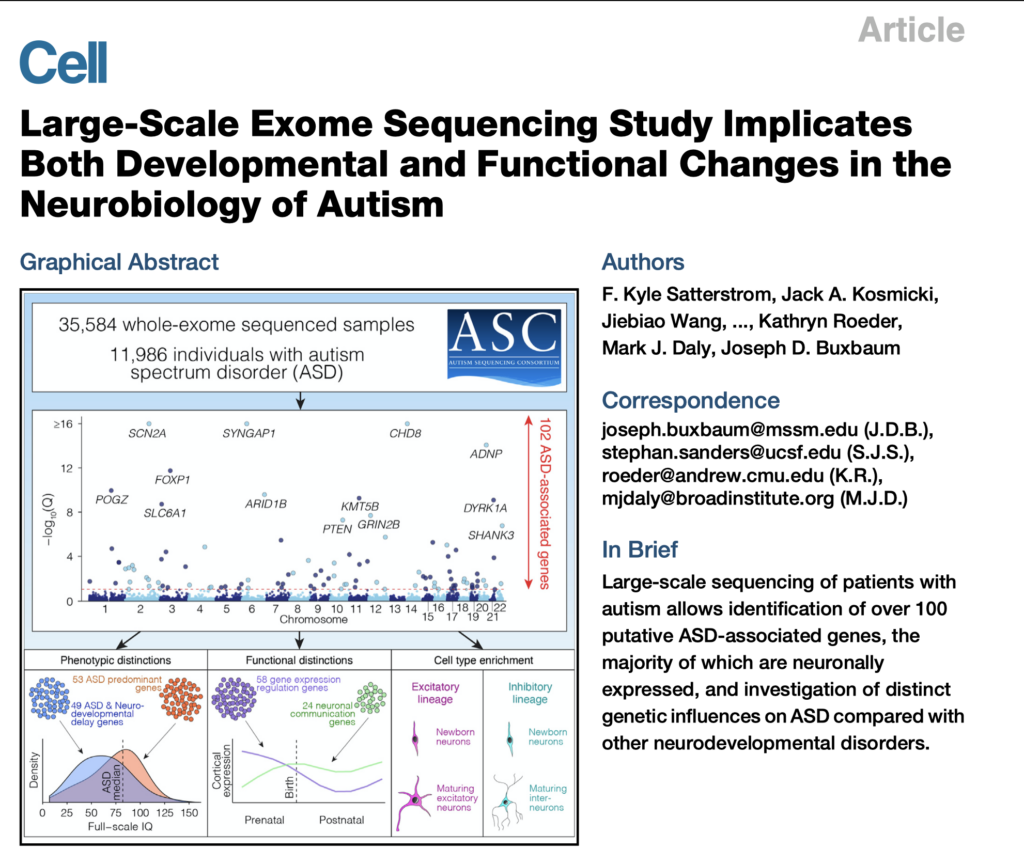
これをフルに利用して、両親や兄弟には存在せず、ASDの子供だけに存在するレア変異を探索したのが、これから紹介するマサチューセッツ工科大学を中心に様々な研究機関が参加して行われた国際研究だ(図1:なおこの論文はウェッブサイトで完全に公開されているので、図などはぜひ参考にして欲しい。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7250485/ )。
この研究では、遺伝子の中でも身体の中で働くタンパク質に翻訳されている遺伝子(エクソームと呼んでおりゲノム全体の5%程度)だけに焦点を当てて、ASD発症に関わりそうなレア変異を探している。
このためには、多くのASD患者さんのエクソームを親兄弟のエクソームと一緒に解読して、ASDだけで見られる変異を探す必要がある。この論文ではなんと1万人以上のASD患者さんと、2万人の正常人を調べ、ASDだけに見られるレア変異を探索している(私のような引退科学者にとって、これほどの数の人の遺伝子配列を解析できると言うだけで感動してしまう。正直なところ、この進歩に頭を追いつかせようと毎日青息吐息で走り続けているが、いつまでもつだろうか?)。
このような大規模解析を行うと、病気とは関わりなく親兄弟にはない新しい変異を見つけることができる。すなわち、私にも、あなたにも、このようなde novo変異は必ず存在する。だからASDで見つかったからといっても、それがASD発症に関わるかどうかはわからない。そこで様々な条件を加えて、最初のリストからASD発症に関わりそうな遺伝子に絞るコンピュータ上の作業が必要になる。例えば、他のASD患者さんで繰し同じ遺伝子の変異が見られる場合はASD発症に関わる確率が上がる。
この研究では、様々な条件をコンピュータで検討して、ASD発症に関わる可能性が9割以上という遺伝子を102種類特定している。このうち60の遺伝子は、これまで関連が指摘されたことがないということから、1万人以上の対象者を調べる大規模研究の重要性がよくわかる。
しかし102種類の違う遺伝子の変異がリストされるとは、多すぎないかと心配になる。同じ自閉症が現れる病気でも、MECP2遺伝子のde novo変異で起こるレット症候群(例えばhttps://aasj.jp/news/watch/6414 を参照して欲しい)では、同じ解析を行えば、必ず原因遺伝子はMECP2に収束してくる。一方、臨床的な自閉症症状の有無だけを条件に探索を行うと、102種類もの遺伝子がリストされることは、ASDが実に多様な状態、まさに自閉症スペクトラムと考えられていることと一致する。
しかし、この研究で明らかになった102種類の遺伝子は全てASD発症に関わっているのだろうか?
実を言うと、この論文から明確な答えは得られない。ただ、いくつかの理由から、全てとは言わないまでも、かなり多くの遺伝子が実際ASD発症に関わっているのではと結論している。
理由その1 、
リストされた遺伝子の多くが発生の初期に脳で発現している。しかも、神経発生の遺伝子のスイッチを調節する遺伝子が半分以上を占め、残りの遺伝子も神経同士のコミュニケーションに関わる遺伝子が多い。この結果は、これまでASDが脳発生での神経ネットワーク形成異常で発生すると言う考えと合致する。
理由その2
細胞レベルでこれらの遺伝子の発現を調べると、抑制性神経細胞や、興奮性神経細胞に強い発現が見られる。これもASDが脳神経細胞の以上であるとする考えと合致する。
理由その3
リストされた遺伝子の多くは、他の精神疾患でも本人に新たに起こった変異として特定されているケースがある。
他にも、これらの遺伝子のASD発症への関わりについて、様々な証拠を提出しているが、これらは全て状況証拠だ。すなわち、せっかくゲノム解析からASDの発症に関わる可能性のある遺伝子を選び出せても、一つ一つの遺伝子の機能から分かりやすいシナリオを皆さんに示すことは、これほど脳科学が進んだ現在でも難しい。結局「レア変異はコモン変異より直接的にASD発症に関わる可能性が高い」ことを示して、論文は終わっている。
では、このような遺伝子の機能を推察し、自閉症との関わりの解明を目指して、少しでも前進するにはどうすればいいのか。次回は、この問題に取り組んだ論文を紹介しながら、自閉症のゲノム研究を見て見よう。
2021年4月30日
連休のstay homeを利用して、新型コロナウイルスパンデミックで、コロナ論文を読む時間が増えた結果、乱れてしまった生活のリズムをもとに戻そうと試みている。その手始めに、一年中断していた「自閉症の科学」論文紹介を始めることにした。ゲノム研究などでは紹介したい論文も集まってきたので、連休中に紹介しようと思っているが、急速に深刻度を増す新型コロナウイルス感染状況を考え、まず自閉症児のマスク着用について発表された論文を紹介することにした。
イギリス型、南アフリカ型と呼ばれている変異ウイルスが蔓延し始め、今回のパンデミックは新しいステージに入ったように思う。特に、ウイルスの感染性を調べる実験から、変異型ウイルスは、細胞への入り口になるACE2により強く結合することがわかっており、入り口が少ないため感染自体が起こりにくかった児童への感染が、多数見られるようになってきた。当然自閉症児にも同じ危険が迫ってきている。その意味で、一般児が行っている日常の新しいルーチンは自閉症児にも習慣づけることが重要になる。
気になって「自閉症」と「マスク」でグーグル検索を行うと、自閉症など発達障害によってマスクの着用が難しいことを周りの人は理解すべきだと言う、「自閉症児の困難を理解しよう」と言う記事がほとんどで、マスクを着けてもらうための具体的な対策について述べた記事はほとんど見つからない。
具体的対策が示されている記事として見つけることができたのは、ノースカロライナ大学の作成した自閉症児支援法を訳したPDFを掲載している大阪大学のサイト(http://www.med.osaka-u.ac.jp/pub/kokoro/pdf/for%20Parents.pdf )だけだった。ただ、この記事もマスク着用については、
「休校明けの学校ではマスクの着用が求められるようですね。マスクがいやというお子さんも多いです。なぜお子さんがマスクを嫌がっているでしょうか?もしマスクのにおいを嫌がっているようであれば、洗える布マスクの方がおすすめです。マスク用の香りづけスプレーもあります。耳にかけるゴムが痛いという方には、マスクのゴムを耳にかけるような商品もあります。もし手に入らなければ、クリップを使ってマスクのゴムを首にかける方法もあるようです。調べてみてくださいね。(上記サイトPDFより引用)
と書かれているだけで、マスク着用を日常に取り入れると言う点で、アドバイスとしては弱い気がする。大事なのは、日常生活で自閉症児をできるだけ感染から守ることで、自閉症児の問題を理解するだけでは不十分だ。必要なのは、マスクを着用して外出できるようにするプログラムだ。
そこで、論文検索サイトで同じようにASDとface maskでサーチすると、今年に入って3篇の論文が同じJournal of Applied Behavior Analysisに発表されていることがわかった。
読んでみると、科学的な治験というより、マスク着用を促すためのプログラムを作成して、数人の自閉症児で確かめてみた観察研究だ。行動学の専門用語が多く、門外漢の私には理解不足の点も多いが、なんとか自閉症児にもマスク着用を促したいと言う強い気持ちが伝わってきた。
もちろんマスク着用のためのプログラム自体は全く思いつきで作られたわけではない。自閉症児に医療上の必要から心電図モニターを持続的に装着してもらう目的で既に使われてきた行動強化のためのプログラムを基礎に考案されたものだ。いずれにせよ、パンデミックが始まって1年以上経過してようやくこのようなプログラムが発表されたことから、簡単な作業でないことがわかる。
3篇の論文だが、まず最初にSilvermanらがマスク着用を促せるプログラムを発表し(図1)、
図1 Silverman論文。(オランダ、ベルギー、ニュージーランド共同論文)
続く2篇(図2、3)は、基本的にこの論文の結果の再現性を確認した論文になっている。そこで、全てを紹介することはやめてSilverman論文のプログラムだけを紹介しておく。
図2 Lillie論文 (米国アイオワPier自閉症センター)
図3 Halbur論文(ネブラスカ大学、ウィスコンシンマーケット大学)
この研究では、マスク着用が難しい六人の自閉症児とその介護者に、リモートで指示を与えながら、論文のTable2で示されたプログラム(図4)を全てのステップが連続してうまくいくようになるまで根気よく続けている。
各ステップを説明した英語は難解な文章ではないので、おそらく皆さんに理解していただけると思うが、念のため訳しておく。
図4 マスク着用を促すためのプログラム。 Table 2の訳
マスクを子供の周り30cm以内に5秒待つ。 次にマスクを子供の周り15cm以内に近づけ5秒待つ。 マスクの紐に触る。 マスクの紐をつかむ。 紐を一方の耳にかける。 マスクのもう一方の紐を片手、あるいは両手で引っ張って、もう一方の耳にかけてフィットさせる。 マスクの上についているアジャスターを押したり引っ張ったりして、鼻にアジャストさせる。(ここは介護者がやり方を教える必要がある) マスクをかけた後少なくとも3秒待つ。 マスクをかけた後少なくとも5秒待つ。 マスクをかけた後少なくとも10秒待つ。 マスクをかけた後少なくとも30秒待つ。 マスクをかけた後少なくとも60秒待つ。 マスクをかけた後少なくとも150秒待つ。 マスクをかけた後少なくとも5分待つ。 マスクをかけた後少なくとも10分待つ。 マスクを外す。 マスクを着ける過程を本当に細かく分解して、根気よく教えると言うプログラムになっている。このような建て付けの行動強化の意味については、専門家の解説を聞きたいところだ。
当然、それぞれのステップができたときには、子供の好きなおもちゃなどを提供し、行動を強化することも行っている。具体的には、「マスクを着けよう」と声をかけて、ステップごとに励ましながら指導するが、うまくいかないとまた最初に戻ると言うことを繰り返している。セッションの間、低酸素にならないかなど、身体的状態はしっかりモニターしており、特に問題は起こっていない。
結果だが、子供ごとに拒否行動を起こすステップは異なっているが、最終的には全員ステップ15までやり遂げている。
他の2篇も、例えば好きなマスクを選ばせる過程を入れたり、フェースシールドも加えたり、よくできた時にはおもちゃだけでなく好きなお菓子を提供して行動を強化したり、あるいは間違った行動を抑制する操作を加えたり(escape extinctionと行動学では呼ばれている)など、いくつかの改変は加えていても、基本はSilverman論文とほぼ同じプログラムを採用しており、同じように参加者全員が10ー15分マスク着用を許容することができている。
もちろんこの10ー15分間のマスク着用がそのまま次の段階、すなわち外出時や学校でのマスク着用の許容につながっていくのかは示されていない。たかだか15分のために、これほど努力する必要はないと言う意見もあるだろう。しかし、学童も含め世界中がマスク着用をルーチンにしている以上、自閉症児についても社会の一員として、なんとかこのルーチンを守ってもらおうとする努力に私は感心した。
今回示されたプログラムは、やはり専門家の指導に基づいて進める必要があると思う。いずれの論文も、両親を含む介護者とリモートでコミュニケーションを図りながらプログラムを進めているので、多くの子供に同時にプログラムを受けてもら得る可能性がある。我が国でも、自閉症児の行動についての専門家から、同じようなプログラムが発信されることを期待したい。
本題からは外れるが、以前、自閉症児は、人の顔を見るとき、目よりも口を注視すると言うことを示した論文を紹介した(https://aasj.jp/news/watch/686 、およびhttps://aasj.jp/news/watch/753 )。これから考えると、マスク着用がルーチンになった現在、自閉症児はマスクを着用した人の顔にどう反応しているのか理解することは重要だ。是非我が国の行動学者も、自閉症とマスクの様々な問題について、検討を進めて欲しいと思う。
2020年4月25日
私たちの子供の頃と違って、ほとんどの家庭にテレビやビデオがあり、乳児がいても、かなりの時間試聴されていると思う。とすると、私たちの世代と、テレビ以降の世代で、物心つく前の乳児期の経験はかなり違っている様に思える。
もしテレビがただの風景と同じなら、何の差も生まれないが、テレビやビデオ画面上での映像が物心つかない乳児にとって、風景とは全く違う内容を持つとすれば、その影響を知りたいと思う。
今日紹介するフィラデルフィアにあるDrexel大学からの論文は、米国で生活環境の幼児の発達への影響を調べる目的で追跡されている子供たちの中から2152人を選んで、乳児期にテレビやビデオ画面に興味を持つことが、性格にどのような影響を持つかを調べた研究で、4月20日JAMA Pediatricsオンライン版に掲載された。
研究は極めて単純で、12ヶ月時点で、保護者(92%は実の親で、他祖父母など)に、「お子さんはテレビを見ますか?」 と「お子さんと一緒に絵本を見ますか?」 と聞いた後、18ヶ月時点でもう一度「この1ヶ月を振り返って、1日何時間ぐらいテレビをみていますか?」 と聞く。
そして2歳児になった時、M-CHAT(日本語版:https://www.ncnp.go.jp/nimh/jidou/aboutus/mchat-j.pdf )で自閉症スペクトラム(ASD)様症状を示すか、あるいは将来のASDリスクを調べ、乳児期でのテレビの試聴や、保護者との遊びの時間と、M-CHATによる性格診断との相関を見ている。
結果は明瞭で、12ヶ月時点で、保護者がテレビやビデオを見ていると答えた子供は、より多くのASD様症状を示すが、ASDになるリスクスコアは変わらない。しかし、18ヶ月時でテレビを見ている時間とASD症状やリスクはほとんど相関がなかった。これに対し、12ヶ月時点で保護者と一緒に絵本を見たりする時間が長いと、ASD様症状は低下することもわかった。
以上をまとめると、
物心つく前にテレビを見る様になる子供は、ASDリスクが高まるわけではないが、ASD様の症状が現れる、すなわASD様の性格が現れる。 一方、保護者と一緒に遊ぶ時間が長いほど、この様な症状の出現を防ぐことができる。 18ヶ月を越すと、テレビを見ることとASD症状とは関係がなくなる。 くれぐれも間違わないでほしいが、1歳までにテレビを見る子供は、ASDのリスクがあるという話ではない。今の所言えるのは、私たち世代の経験したことのない乳児期のテレビという風景が、ASD様症状の出現と何らかの関係ありそうだという観察結果だけだ。もちろん、テレビが原因でASD様症状が出るとも、ASD様傾向を持つのでテレビに興味を示すとも結論できない。しかし、できる限りテレビという人工的風景を避け、子供との時間を持つことはASD症状の出現を防げる可能性を示していると思う。簡単な観察研究だが、典型児、ASD児を問わず、乳児期のあり方の一つのヒントを示している様に感じたので、自閉症の科学として紹介することにした。
2020年4月12日
緊急事態宣言が出され、大都市圏では学校や施設閉鎖が延長された。もちろんASDの子供も例外ではない。この時、ASD の子供と自宅でどう過ごせばいいのかについて、10のヒントが4月1日号のBrain Scienceに掲載されていたのでそのまま訳して掲載する。
もちろん米国とわが国では事情も異なるし、またASDの症状は多様なので、 「米国ではこんな対応が指示されているのか」と、何かの参考にするという気持ちで読んでいただければ幸いです。
ASDの子供は具体的な事象に即して認識して、抽象的なことを理解するのが苦手なことが多い。また、言葉でのコミュニケーションが苦手だったり、周りの現象を理解することも難しい子供達がいる。それでも、何が新型コロナウイルスか、なぜ家にとどまる必要があるのかを説明することは重要。説明は単純で具体的でなければならない。この目的で、意思伝達装置(例えば:https://ogw-media.com/medic/cat_it/4377 )を使う可能性もある。また、新型コロナウイルスとは何かについてのパンフレットがあれば使える(例えば藤田医科大学の資料:http://www.fujita-hu.ac.jp/~microb/Final_version.pdf )。言葉で説明するときには、概念をわかりやすく示した図を使うことも重要(わが国でもこのような準備はできているのだろか?)。
ASD児は実行力に問題があることが知られており、特に日常性が破壊されると毎日の過ごし方を計画できなくなる。このため、できるだけ早く毎日の活動を構造化することが重要。この状況では、家庭が活動の唯一の場になる。そこで1日の活動をいくつかに分けて、部屋を変えて行うことも役にたつ。このような時間割は知能に障害がある子供だけではなく、知能は正常のASD児にも役に立つ。また、この時間割を家族全体で行うゲームのように仕立ててもいい。黒板に、家族がその日何をするのか計画を書き入れてみたらどうだろう。
ASD児は遊ぶのが好きだが、感覚のトラブル、あるいは行動の反復性などから、苦手な遊びがある。いずれにせよ、1日のうち、遊びの時間を持つことは重要。これは一人で遊ぶことでも、だれかと一緒に遊ぶことでも良い。例えばLEGOを用いた治療は知能を問わずASD児には良い遊びの方法になる。この治療方法は子供の社会性を高める目的でますますポピュラーになっており、特に社会性に問題を抱えるASD児のような子供に適している。これを子供と親が一緒に遊ぶ、ある程度自由を持たせた遊びとして、自宅で行うことができる。(レゴセラピーについてはhttps://www.kango-roo.com/sn/a/view/4311 を参照)。
シリアスゲームについてはウィキペディアを参照してほしい:https://ja.wikipedia.org/wiki/%E3%82%B7%E3%83%AA%E3%82%A2%E3%82%B9%E3%82%B2%E3%83%BC%E3%83%A0
シリアスゲームはASD児の社会による認知の促進、表情に現れる感情、感情的な仕草、感情的な状態の理解に役立つ。シリアスゲームはASD児の基本的教育資源として利用できる。多くのシリアスゲームは無料でウェッブからタブレットやPCにダウンロード可能。シリアスゲームは教育目的でビデオゲームやウェッブサイトの代わりとして使える。
親とビデオゲームやインターネットセッションを共有する ASD児はビデオゲームやインターネットに強い興味を示すことが多いが、現在のように子供達が家庭から出られない状況では、逆にはまり込んでしまう危険がある。子供がPCで遊ぶのを避けることは難しいが、現在のように親も家庭にいる機会が増えた場合、ビデオゲームやインターネットを親や、兄弟、あるいは介助者たちと共有できるよう過程でルールを作ることを考えてみると良い。これによって、子供が一人で孤立しインターネット中毒に陥るのを防げる。
特定のものへの興味を持つことはASD児の特徴。このような興味を持つことの重要性については現在ますます理解されるようになっている。このような興味を持つことについては、親や介助者も積極的に励ますことが重要。興味の対象例としては、乗り物、地図、動物、漫画、地理、電子機器、そして歴史などを挙げることができるが、他にも多くの可能性がある。親と子供が自宅で過ごすようになった現在の状況は、このような興味に関する活動を一緒に行ういいチャンスになる。
ASDには、ASDとは別の精神的な脆弱性や病気を高頻度で抱えていることがよく知られている。これらの病気の中でも不安神経症は最も報告が多い。このような精神疾患が青春期に起こると精神発達崩壊につながる恐れがある。特に新型コロナウイルスによる非常事態はASDの子供にとって自分のこととして理解しにくい出来事と言える。このため、新型コロナウイルスの非常事態宣言が出る前から精神治療を受けていた場合、それを続けることは大変重要。ところが外出自粛状態では殆どのセラピストは対面での治療を中止せざるをえない。そこで、ビデオやオーディオを用いての遠隔精神治療を、毎週予約して受けることは大変大事なことになる。これにより、不安が解消され、気分をチェックし、子供が専門家と話す機会が得られる。
親や介護者のため、毎週オンライン相談の機会を持つ。 ASD児の親は典型児や他の障害を持つ親より強いストレスにさらされており、また影響を受けやすい。現在のような事態になると、親だけで子供の面倒を見なければならない。この結果、それでなくとも疲れきっている親のストレスはますます高まる。この問題は子供の知能レベルとは関係ない。これに対し、子供のセラピストに毎週オンラインで相談の機会を持てると、かなり改善する。知能の遅れのある子供の場合、子供が自由に遊んでいる様子や、あるいは決められた課題を行なっている様子をホームビデオにとって、セラピストに見せることは役に立つ。また、知能が正常な子供の場合、この難局をどう乗り切ればいいのか対話形式で相談し、子供への対応方法の知識レベルをアップデートする時間にできる。
学校で先生や友達と関係を保つことが学習の助けになることがわかってきている。毎日決まった時間を学校が指示するホームワークに、日課として続けることは重要だが、学校の社会的付き合いを維持するためには、少なくとも1週間に一回は、先生を含むクラスの誰かと接触を保つことが示唆されている。コンタクトを取る方法は子供の症状や性格による。問題なければ、オンラインでのコンタクトは重要な可能性だ。オンラインによる接触が嫌なASDの子供に対しては、先生やクラスの誰かに手紙を書いたり、あるいは直接電話で話すこともよい。子供と親の両方にとっても、特定の先生とオンラインや電話で接触を維持することは強く推薦できる。
すでに1−9で述べたように、ASDの子供が積極的になるよう刺激することは重要だが、1日のうち適当な時間を予備の時間として残すことも大事(例えば家の近くを散歩する)。というのも、緊急事態では子供の行動は型にはまってしまう可能性が高い。もちろんだからと言って心配することはないが、習慣が変化すると、ASDの子供のストレスレベルは高まり、紋切り型の行動が増えることがある。これは、ストレスを感じていることの現れで、決して退行ではない。
我が国では支援が進んでおらず羨ましいと思える点もあるかもしれないが、参考になる論文だと思い紹介した。
2020年3月12日
社会性障害、言語能力低下、繰り返し行動がASDの三大症状などと言われると、何か最終宣告のように聞こえてしまうが、全くそんなことはない。今まで2回にわたって、絵本を通してのコミュニケーション、スポーツクラブに入って他の子供たちと運動する、などのプログラムで少しづつ新しい能力が開発できる可能性を示す論文を紹介してきた。
3回目の今日はバージニア大学のグループが学校で使えるようにデザインした言葉の能力を高めるためのプログラムについての治験研究で3月2日にJournal of Autism and Developmental Disordersに発表された。
このグループは長年にわたってASD児の言葉に関わる能力を高めるためのプログラムや材料を開発しており、この治験は彼らが2014年に開発した「Building Vocabulary and Early Reading Strategies 」というプログラムを小学校の課外授業として実施し、1)話し言葉の能力が改善するか、2)聞き取り能力が改善するか、3)教師がこのプログラムを実行できるか、の3つの問題を調べている。
具体的には5−9歳のASD児43人の参加を募り、まず年齢、背景、ASDの症状を揃えたペアに分けて、そのあとで無作為にペアの一人をプログラムを受ける群、もう一人を受けない群に振り分けている。
プログラムの内容だが、本に書かれた物語を大きな声で音読させることを基盤にして、読んでいる物語の内容を理解する、これまでの知識と比較する、物語をもう一度語る、物語から想像する、などの能力を途中で質問したり、文字に書せたりして意識させていくことで、言葉を使う能力を高めるようデザインされている。
重要なことは、このプログラムを学校で国語(?)の補修科目として組み入れている点で、このためにこのプロジェクトに協力してくれた先生を訓練している。
この補修プログラムは1日30分、週4日続き、全体で平均65セッション行うように計画している。そしてプログラム前後で様々な言語能力をテストして、改善が見られるかどうか調べている。
もちろん二重盲検、プラシーボなどは不可能な治験だが、プログラムを受けたグループは、ボキャブラリーのテスト、語る能力、言語全般の能力などで、受けなかったグループと比較して明確な改善が見られることから、効果は高いと結論している。
私も専門家でないので、言語能力測定に使われたEVT-2テスト、NEPSY-IIテスト、CELF-4テストで見られた改善が、実際にはどの程度なのかイメージすることはできないが、全てのテストでしっかり改善していることが示された。
詳細は専門家に任せることにして、学校で週4日、1回30分のコースが、ASD児の言葉の能力を改善できたことに感心した。おそらくわが国でも同じようなプログラムが開発されているのではないだろうか。大事なことは、これほど多面的な効果が得られるなら、学校での学習過程の中にそのようなプロジェクトが組み入れられ、多くの子供たちがプログラムを受け、その効果が常に検証されることだと思う。
以上、3回にわたって紹介した気になる治験論文は、家庭、スポーツクラブ、学校と異なる場所でのプログラムが少しづつではあってもASD児の能力を高めることができることを示している。思いつきでも、まだまだASDに対しては対症療法が重要であることが良くわかるが、それを治験として検証し、多くの人に使えるようにすることが最も重要だと強調して、ASD児に関する気になる治験シリーズを終える。
2020年3月9日
前回はASD児に絵本を読み聞かせたり、説明したり、質問したりする行動が、ASD児の言葉に対する注意を促すことを示す研究を紹介した。2回目の今日は、運動の効果だ。ASD児ではしばしば運動症状が認められる(例えば視覚と手の運動の連携が悪いなどの症状)。また、これらの運動症状とASDの心の問題とは密接に関連していることも知られている。もしそうなら、ASDの子供たちの運動能力を高めるプログラムは、運動能力にとどまらず、社会性や性格の変化をもたらしてくれる可能性が高い。
今日紹介するオーストラリアDeakin大学からの論文は、ASD児にオーストラリア全国で活動している子供を対象にしたサッカークラブAuskickのプログラムに参加させて、社会性や様々な性格に変化が起こるかどうか調べた研究で2月27日Journal of Autism and Developmental Disordersに掲載された。
研究は単純で、61人のASDと確定された5−12歳のASD児を2グループに分け、半分はAuskickクラブ(https://play.afl/auskick )が提供するプログラムを最低12回受けさせ、残りのグループは自宅で普通の生活を送らせる。そしてプログラム終了時に、知能、社会性、性格などを一般的な方法で調べている。
どのようなプログラムを受けるかはそれぞれのクラブに任せており、ハンディキャップを持った子供たちのプログラムに入る場合も、全く普通の子供のためのプログラムに入る場合もある。
結果だが、様々なマニュアルに従った検査については専門的なので、ここは著者らを信用して結論だけを手短にまとめると、次のようになる。
子供も行動を診断するCBCLチェックリストの様々な項目について調べると、全項目を総合した結果、内向性を評価する結果、そして米国精神医学界のDSMマニュアルによる不安神経症の程度が、サッカークラブでプログラムを受けることではっきりと改善した。 サッカークラブを経験したASD児は、サッカークラブセッション終了後も、他のプログラムに参加する傾向があった。 チームスポーツではあるが、コミュニケーションや社会性の改善ははっきりしない。ただ、CBCLによる社会性の問題は明らかに改善している。 上記の変化はプログラムの強とあまり関係はなく、一般児と同じプログラムでも、ハンディキャップ児と同じプログラムでも同じ程度に改善が見られた。 結局最後までプログラムを受けられたASD児は20人足らずになってしまったため、統計的に結果を信用できるのかどうかなどいろいろ問題はありそうだが、おそらく上手にプランされたチームでやるスポーツは受けさせてみる価値があるという結論になる。
しかしこのためには、上手に管理されたプログラムが必要だ。日本のサッカークラブの現状は知らないが、サッカーの上手な子供を育てることが目的になっていて、なかなかASDの子供まで受け入れる余裕はないのではないかと思う。また、一般児のプログラムにASD児が参加するのを、クラブや親が許すかどうか疑問だ。しかしわハンディキャップを持った子供たちの身体機能や精神機能の促進にも一肌脱いでこそ、我が国もプロ野球大国、サッカー大国になれるのではないかと思う。そんなスポーツクラブが増えることを望んでいる。
2020年3月6日
自閉症スペクトラムについての医学生物学的研究は急速に進んではいるものの、ようやく早期診断のための方策が見えてきた段階で、まだ治療の決め手はなく、一見思いつきとも言える手作りの治療法の効果を探っている段階と言えるだろう。大事なことは、これらの手探りの多くが論文として公開されている点で、論文を見ていると「こんなことまで調べているのか」と本当に感心する。これから3回に分けて、こんな気になる治験について紹介しようと思っている。
1回目の今日は、絵本の読み聞かせとASD児の言語反応との関係を調べたオーストラリアGriffith大学の研究で、Journal of Autism and Developmental Disorderに発表された(上図)。
両親との言葉を通したコミュニケーションが子供の言語能力に大きな影響がある事はよく知られている。その典型的な例が、絵本を前にして子供にその内容を読み聞かせる行動で、これが子供の言語能力を発展させることについてはすでに多くの報告がある。
しかし、社会性と言語能力の低下が見られるASDの子供たちに絵本を読み聞かせることで言語能力や社会性が改善するか調べた研究は不思議なことに殆どなかったらしい。
この研究では47人のASDと診断された4歳から6歳の子供とその家族に参加してもらい、この研究のために選んだ2種類(一冊ははっきりした物語、もう一冊は絵が飛び出すカラフルなビジュアル系)の絵本を、ASD児と一緒に見ながら親が説明する課題を行ってもらい、その一部始終をビデオに撮影してもらっている。
このビデオを解析して、親の行動と子供の反応や能力との相関を調べ、社会性や言語能力を改善させるヒントを得ようとしたのがこの研究だ。従って、この研究だけからは本を読み聞かせることがASDの社会性や言語能力に効果があるとかないとかは結論できない。
本を読み聞かせる時間の平均は高々一冊の本で6-7分で、短い場合は3分、長い場合は20分と大きくばらつく。この間のお母さんの行動を、
本に書かれている絵を指差したりして言葉を教える行動、 物語の構築についてもう一度わかりやすく説明する行動 子供への質問、 テキストに書かれている文を読みながら、その中の単語を教える行動。 にわけている。
これに対する子供の行動としては、親とコミュニケーションを取ろうとする発語と、発した単語の数を記録し、親の行動との相関を調べている。
わかりやすく言うと、ASD児の言葉の反応が、親のどの行動に対して起こるかを調べている。詳細を省いて結果をまとめると次のようになる。
本を読み聞かせる時の親の行動は多様。 しかし、個々の行動と子供の反応との相関を調べると、本の内容に基づいて、その意味を伝えようとするときに子供はより強く反応する。 本に書いてある単語について説明すると子供の文字の知識が増える。 かなり単純化したが、結果は以上で、本を読み聞かせることはASDの子供の言葉の使用を高め、文字を習得するのに役立つと結論している。しかし残念ながら、この読み聞かせがどの程度の症状改善をもたらせるかなどの臨床的検討は全く行われていない。
それでも、両親が絵本を読み聞かせるとき、子供のどんな行動に注意すればいいのか、参考になるのではないだろうか。
明日はASDの子供をサッカークラブに入れたらどうなるかを調べた論文を紹介する。
2020年2月18日
「自閉症の科学」では、繰り返し繰り返しASDに関わる遺伝子変異の論文を紹介してきたが、これは21世紀に入ってこの分野の研究が急速に進展し、今も多くの論文が発表されつづけているからだ。しかもこれで十分というレベルには到底達しておらず、知識は今もアップデートされ続けている。これを裏返すと、それほどASDの遺伝的背景が複雑であることを物語っている。これまでの研究から見えてきたのは、ASD状態は、多くの遺伝子が合わさって形成される性格と同じような脳の多様性とともに、その多様性が最後に「異常」として表現されるために必要な遺伝的変異が組み合わさって形成されることで、この二つのタイプの変異の質が大きく異なっているという認識だ。
今日紹介したい論文は、ボストンのMITを中心に1万人以上のASDのゲノム配列を調べ、特にASDが異常として表現される遺伝子変異を特定しようとした探索研究だが、論文をいきなりそのまま紹介したのでは、おそらく医学部の学生さんでもすぐ理解するのは難しい内容だと思うので、まず遺伝子変異の質についての基礎知識から紹介してみたいと思う。
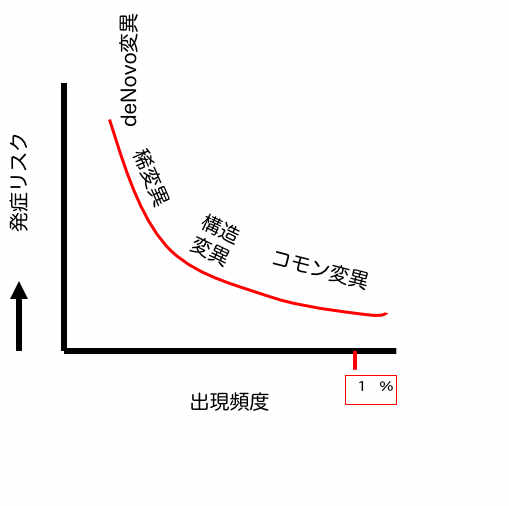
私たちの細胞は外界からのストレスがなくても、細胞が分裂するたびにDNAが複製され、そのたびに様々なタイプの複製ミスが生まれるようにできている。このような個人レベルのゲノムの違いが、環境要因に影響される遺伝子の使い方(エピジェネティックス)と合わさって一人一人の性質や性格の違いを生み出している。図に示すように、こうして生まれる遺伝子変異は、大きく頻度の比較的高いコモンバリアントと、稀にしか見つからないレアバリアントに分けることができる。この、コモン、レアを決めている要因が、遺伝子変異への選択圧力で、例えば個体の生存に関わる多くの変異は、子孫が残せないため集団内の頻度は必然的に低くなり、レアバリアントになる。一方、現在個人の病気の遺伝的リスクを調べるために提供される個人ゲノムサービスの多くは頻度が比較的高いコモンバリアントを調べる検査だ。例えば、身長などはこのようなコモンバリアントがいくつか合わさって決まることがわかっており、最近ではこのようなコモンバリアントの組み合わせから身長を推察することも可能になっている。要するに私たちが一般的な性質や性格と呼ぶものは、コモンバリアントの複雑な組み合わせからなるといっていい。
ASDも、コモンバリアント(CV)、レアバリアント(RV)の両面から調べられてきた。例えば脆弱性X症候群、RETT症候群など特定の遺伝子機能が失われるRVは、発達遅延とともにASD様症状を示すことが知られており、異常状態が発生させる過程を理解するために重要な変異だ。実際このようなRVは、動物に導入するとASDに似た症状を示すことが多く、ASDモデル動物として研究されている。ただ、発達障害のような目立つ症状が出る場合以外は、RVを発見することは難しく、調べるためには千人以上のゲノムを調べることが必要になる。
一方頻度の高いCVのほとんどは個体の生存に直接関わることは少なく、個々のCVは変異というものの、性質の大きな変化につながることはまずない。すなわち変異への選択圧は弱く、結果その変異が一定の頻度で維持されてきたと考えられる。個々のCVの影響は大きくないが、他の様々な変異と合わさることで様々な病気の発症に関わることも確かで、全ゲノムレベルでCVを調べる検査(GWAS検査)で疾患との相関を調べることでリスクを計算することができる。ASDについても多くの研究が行われ、100を超すCVがASDのリスク因子として相関することが明らかになっている。ASDと相関するCV がこれほど多く見つかったと言う事実は、ASDがまさに様々なタイプを包含するスペクトラム障害で、性格と同じようにCVの組み合わせで決まる脳の多様性を反映している根拠として考えられるようになった。
その後次世代シークエンサーの利用により、個人ゲノムのDNA配列を読むコストが急速に低下した結果、千人を越す人のゲノム配列を調べる研究が可能になり、自閉症という一枚のコインを、CV,RV両面から一体的に調べる研究が進み始めた。その典型が前回「自閉症の科学」で紹介した「父親の精子に見られる遺伝的変異のモザイク」(https://aasj.jp/news/autism-science/12266 )についての論文で、この研究では図でde Novoの変異として示した、両親、兄弟にはなく自閉症児本人だけにみられるRVを調べている。
さて、今日紹介したいMITを中心とする国際チームからの論文では1万人を越すASDについて、ゲノムのうちタンパク質に翻訳される部分(エクソン)を解読し、ASDだけに存在し、一般人には見つからないRVを探索している。RVを特定したい場合、対象が多ければ多いほど新しいRVを見つけることができる。これまでの研究では千人規模だったので、1万人規模にスケールアップすることでさらに稀なRVも見つけることができる。ただ、この探索には終わりはなく、次は10万人、その次は100万人と、すべてのASDリスクRVがリストできるまで研究は続くと思う。従って、この研究も中間報告として考える必要がある。
膨大な研究なので詳細は省いて、RVを調べることの意味を中心に以下にまとめてみた。
分子の構造変化につながるRVがASDでは3.5倍多く蓄積する傾向がある。逆から言うと、ASD発症には確かに分子機能の変化を伴うRVが関わっている。統計学的には、RVはASDで見られる変異の2%ほどで、50%以上はCV。 RVの頻度は女性のASDの方が2倍高い。ASDは男性が圧倒的に多いことを考えると、この結果は不思議に思われるかもしれない。しかし、女性がASDを発症しにくいということは、逆に発症のためには男性より多くのRVが必要であることを意味し、これまで考えられていた様に、女性はASDになりにくい事実の裏返しと見ることができる。 この研究では全体で102種類のASD特異的RVと特定されたが、そのうち60は新しく発見されている。即ち、対象の数を増やせばさらに新しいRVが発見できる可能性がある。 ほとんどのRVは神経細胞で発現しており、ASD特異的RVp(53種類)と、他の精神疾患にも見られるRVn(49種類)に分けることができる。他の神経疾患でも見られるRVを持つ児童は、歩く時期が遅く、軽度の発達障害が見られる事から、RVpとRVnの機能は異なることが推察できる。 RVの機能は、遺伝子発現調節に関わる分子か、シナプスなどの神経管結合に関わる分子に分けられる。また、101種類のRVは出生前の脳で発現が高い事から、神経発達に関わると推定される。 これ以外にも、いくつか面白い解析が示されてはいるが、あまりに専門的になるので割愛する。
要するに対象の数を増やすことで、ASD特異的RVを特定することができ、統計学的解析からこれらRVが確かにASD発症に関わることが証明できたと言える。
これまで自閉症と相関することが発見されたCVがあまりに多いため、ゲノムから新しい治療法を発見することは難しいのではと考えられてきたが、この脳の多様性が「異常」として表現されるために必要なASD特異的RVが明らかになることで、ゲノムからASD治療法を開発することも夢でないと思っている。