2019年8月19日
毎日書いている論文ウォッチは主に生命科学の大学生以上を対象としているので、一般の方に対する情報としては少し難しい。そこで、今日から一般の方にもわかりやすい論文を紹介する「生命科学をわかりやすく」というセクションを設けることにした。毎日紹介することはできないが、こちらもぜひ読んでほしい。原則として、査読を受けた論文を対象としているので、間違った情報が発信される確率は低いが、もちろん捏造という場合もあるので、そこは大目に見てほしい。
第一回目の今日はウィーン医学大学からの論文で、最もよく処方される薬剤の一つ、胃酸を抑制する抗酸剤の使用が、アレルギーを増やしているという研究でNature Communicationに掲載された(Nature Communications (2019) 10:3298 | https://doi.org/10.1038/s41467-019-10914-6)。タイトルは「Country-wide medical records infer increased allergy risk of gastric acid inhibition (オーストリア全国の医療記録から胃酸抑制によりアレルギーのリスクが高まることが推察される)」だ。
この研究は最初から制酸剤を投与するとアレルギーリスクが高まるということを仮定して研究を進めている。2009年から2013年までの期間、オーストリアで処方された制酸剤、抗アレルギー剤、そして高脂血症や高血圧に対する一般的な処方を抜き出し、それぞれの薬剤が組み合わさる確率を調べただけの研究だ。これにより、制酸剤とアレルギー発症の関係を調べられると期待できる。
結論は明確で、様々な制酸剤(プロトンポンプ阻害剤が一番多い)が処方された後、抗アレルギー剤が処方される確率は、全オーストラリアで2倍近くに達し、一部の地域ではなんと3倍に達するという結果だ。
女性の方が影響を受ける確率が高く、また60歳以上の高齢者は、20歳以下の若者よりリスクが高い。
様々な原因が考えられるが、制酸剤の免疫細胞への直接作用よりは、胃酸をおさえて食べ物の消化が抑えられることで、抗原が分解されずに摂取されることが、最も大きく寄与しているようだ。
他にも原因は考えられるが、原因追及より先に制酸剤の処方をもう少し慎重に行うことが重要だと思う。
2019年8月19日
最近あまりにも論文が多すぎて光遺伝学を用いた研究を紹介する機会が減ったが、技術的には急速に進んでいる。というのも、光を使う問題点ははっきりしており、それを解決してより精密な神経コントロールが可能になりつつある。したがって、一度この辺についてもジャーナルクラブで取り上げる予定にしている。
そのとき是非取り上げたいのが今日紹介する光遺伝学の本家本元Karl Deisseroth研究室からの論文で、視覚認識の経験を、光遺伝学的に脳内に再現するという研究で、重要な課題を設定しその解決のために必要な技術を開発していくこの研究室の迫力に満ちた研究だ。タイトルは「Cortical layer–specific critical dynamics triggering perception (知覚を誘導するために必須の皮質特異的動態)」だ。
光遺伝学の重要な進歩の一つは、立体的に構成されている神経細胞を狙って光刺激を入れるホログラム方法の開発だろう。まず自然の感覚刺激により興奮する神経細胞を記録し、それをもう一度刺激するという離れ業だ。ただ、こうして作成する光のスポットに迅速にしかも強く反応できるロドプシンは存在しなかった。
この研究ではまず、微弱な光に反応できる海洋の微生物600種類以上のゲノム解析から、彼らがChRmineと名付けたチャンネルロドプシンを特定する。これは、赤い光に反応するため、カルシウムイメージングで出てくる光の影響を受けないため、刺激と興奮記録を同時に行うことができる。また、光への感受性も高く、さらに反応時間も短く、ホログラム刺激と組み合わせるのに最適の分子であることを示している。
あとは、マウスが縦縞、横縞の資格刺激を受けたときのV1視覚野で興奮する神経を記録し、皮質2/3層と5層に散らばる神経細胞を刺激できる様にしている。
この方法により、視覚刺激に対して訓練されたマウスを用いて、視覚で刺激される神経興奮と同じ認識が光遺伝学で再現できること、さらには視覚でははっきり区別がつきにくい刺激を光遺伝学を同時に組み合わせて正確な認識が可能になることなどを示している。また、視覚認識形成時の皮質の回路についても、刺激と記録を組み合わせた実験から明らかになっている。
もちろんこのためには、視覚により興奮した細胞だけでなく、興奮しなかった細胞で光遺伝学刺激で興奮した細胞など、刺激と記録が同時に可能であるという利点を生かして詳しく調べ、それをもう一度至適な刺激として再構成することまで行っている。おそらくネズミは、見るという経験を、光遺伝学的にもう一度経験し直しているのだろう。
極端に言えば、将来私たちの経験を脳の興奮のパターンとして記録し、それを再現してもう一度思い出を体験するということが可能であることを示しており、この分野がもうSF作家の想像力の世界にまで到達していることを示している。次はなにを見せてくれるのか、興味が尽きない。
2019年8月18日
転写について今どの様に教えているのだろう。基本は、DNAをRNAに読み替えるポリメラーゼ(Pol II)を正しい場所にリクルートし、それを開始点としてRNAを合成しながら、正しい場所でスプライシングする過程といえるが、これだけなら普通の代謝マップの様な簡単そうな図がかけてしまう。しかし、転写開始点ではPol IIはプロモーター、エンハンサーに結合する転写因子とメディエーター含む複合体を形成しているし、スプライシングのためにはこれもスプライソゾームと呼ばれる大きなタンパク質複合体と結合する。この機能の違うしかし巨大な複合体とPol IIの相互作用を追跡することは簡単ではない。
今日紹介するRichard Young研究室からの論文はこの過程をPol IIがタンパク質複合体の中に一種の相転換のように隔離される過程として可視化しようとした研究で、Natureオンライン版に掲載された。タイトルは「Pol II phosphorylation regulates a switch between transcriptional and splicing condensates (Pol IIのリン酸化により転写複合体と、スプライシング複合体のスイッチがおこる)」だ。
転写からRNAの合成までに何が起こっているかは明確なイメージがすでにできている。まず、転写因子とメディエーター複合体とPol IIが合体することで転写の開始の用意ができる。このPol II のC末端の2つのセリンがリン酸化されることでPol IIがDNAを移動してRNA合成が起こるが、この時スプライシング複合体がPol II上に形成される。
ただ、この様な巨大な複合体がPol II上でどう転換するのか、そんな簡単な話ではない。この研究では転写のMediator複合体とPol IIのC末が、例えばNanog遺伝子上で合体していること、このMediator との合体にはC末がリン酸化されていない必要があることを示している。
エンハンサーにより転写が進む遺伝子上では、当然のことながらPol IIはスプライシング分子とも合体していることも確認している。すなわち、この転写因子とMediator複合体からスプライシング複合体の乗り換えがおこるのだが、これがPol
II のRNA合成開始を誘導するC末のリン酸化に依存しているのか、試験管内で分子の複合体形成を組織化させて調べる一種の相転換を利用した方法で調べている。
結果は予想通りで、C末がリン酸化しないときはMediatorを含む複合体を形成するが、CDD7, CDK9でリン酸化すると今度はスプライシング分子と複合体を形成する。すなわち、C末のセリンリン酸化により、転写因子・Mediator複合体からスプライシング複合体へ乗り換えが起こることが確認されたことになる。
結論はこれだけで、当然の話だと思われる人もいるだろう。しかし、彼らが開発したdroplet assayで、分子が液相からタンパク質複合体へと自然に合体することを目に見えるようにしたことは重要で、これにより現象論から化学的胴体解析へと踏み込めるのだという実感がもてる、さすがYoungのグループだと思える研究だ。
2019年8月17日
ゲノムの発生
2016年8月1日
これから何回かにわけて、生物進化とその過程で生まれた情報について見ていく。この作業を通して生物進化を、様々な情報が生まれる過程として眺めてみたい。そしてこれらの情報を、「伝達性・コミュニケーション」と「環境の自己への同化」の観点から再検討することで、なぜ進化の究極に言語が誕生出来たのかに至る議論が出来ればと思っている。
前回述べたが、ある現象を特定のシグナルとして解釈できる生物機構がうまれると、この機構により解釈されることで、あらゆる現象は情報に変わる。この機構を理解することは当然生物進化の理解に欠かせないが、このシリーズでは、個体間、細胞間で伝達・コミュニケーション可能な情報に限って議論を進める。
元々、20世紀の情報理論は情報の伝達とコミュニケーションについての科学として生まれた。例えばシャノンの情報理論は、非物理的存在である情報が、伝達という観点から見ると、物理的物質(例えば電線)と量的な相互作用をすることができること、また情報が物理量による変化を受けてもコミュニケーションを成立させるための理論として始まった。また、選択された形質の子孫への「伝達性」はダーウィン進化論の中核をなす概念だ。生物にとっての情報は必ずしも個体間で伝達される必要はないが、今回は伝達・コミュニケーション可能な情報に限って議論する。
しかし、生物間で伝達とコミュニケーションに使える情報はゲノムだけではない。高等動物になると、ゲノム以外にも他の種の生物に伝えることのできる情報は数多く存在する。例えば言語も人間(生物)が持つ情報媒体だ。言語を獲得することで、私たちは自己を身体から解放し、ほぼ全ての人にほとんど無限の情報を伝えることができ、さらには他の個体と瞬時にコミュニケーションすることが可能になった。
このことを哲学者ヘーゲルはうまく表現しているので引用しよう。
この様に伝達性・コミュニケーション性から見ると言語は情報進化の究極にあるが、言語に至るまで伝達可能な他の情報が進化の過程で現れた。これらの情報がどこに向かって、どのように伝えられるのかを見ていくのがこれからの作業だ。
情報の進化を理解するためのもう一つの観点に「環境の同化」を選んだのは、環境を同化しようとする指向性が進化の原動力と考えているからだ。環境による選択と言ってもいいのだが、ゲノム以外の情報が加わってくると、もっと積極的な環境の取り込みが起こっている。従って、ゲノム以降新しく生まれた様々な情報が環境を同化する過程を見ることで、進化の力学の本態を知ることができる。
環境の同化を考えることで、「進化は多様化した個体を環境が選択すると過程」といった紋切り型の議論を排して、進化の本当の力学を理解できるようになると期待している。そのため、個々の情報が進化にどう関わり得るかについても丁寧に検討してみたい。
伝達性を考えるとき、一つ注意してほしいのが、環境の変化を通して個体の活動が子孫に伝達できる点だ。あらゆる生物は様々な大きさの領域に拡がる環境を変化させる可能性を持っている。生物により変化させられた環境は、回り回って子孫の生存を制約できる。すなわち、生物による環境変化に関わった全ての情報は、こんどは環境からの制約という形で子孫に伝わる。少しわかりにくいと思うが、例えば言語情報を介する高次機能によりこれまでなかった新しい生活環境(例えば都市)が生まれたとしよう。こうして出来た都市は影響力のある環境として、子孫の生存や進化を制約する。これは人間だけの問題ではない。都市から排出されるスモッグで黒い羽を持つ蛾が都市では優勢になるという有名な「工業暗化」の話は、生物同士が環境を変化させることで、それぞれの進化に影響した例と言える。この生命の「歴史性」の問題は、進化を考える上でも重要な問題で、ゲノム以外の情報の進化への影響を扱う際常に留意する必要がある。
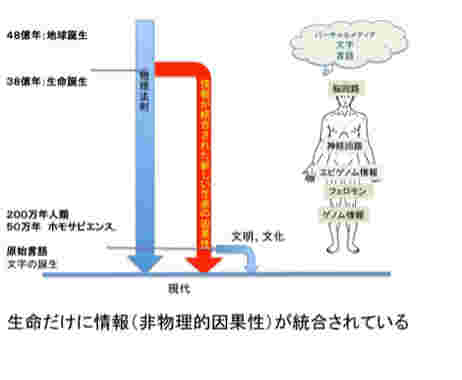
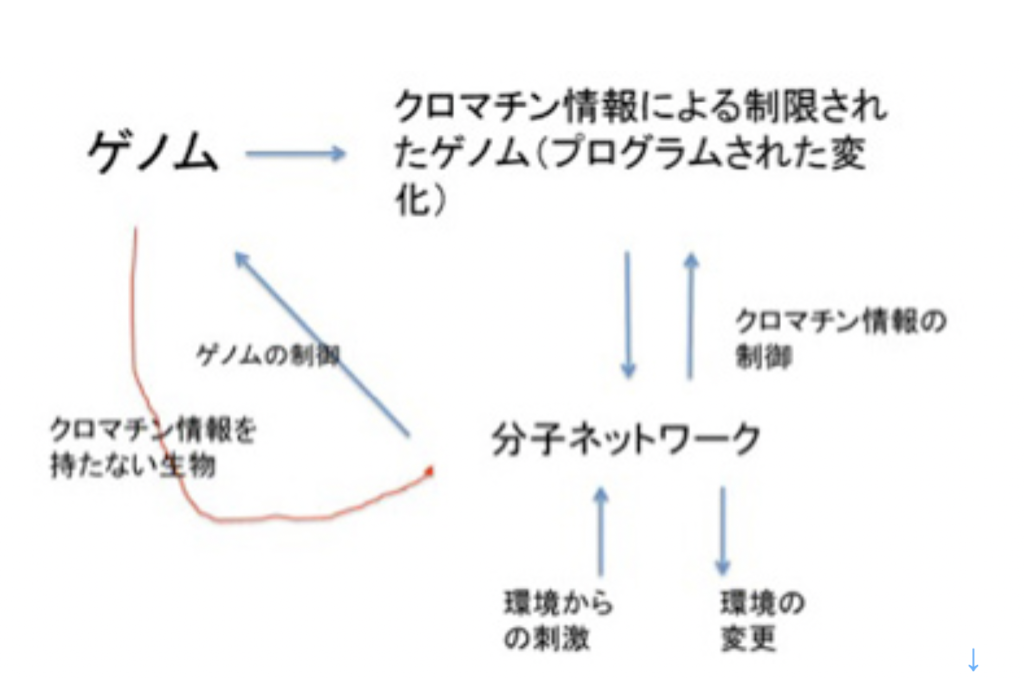
図1にこれから扱おうと思っている情報を図示したが、1)ゲノム、2)フェロモン、3)エピゲノム、4)神経回路と脳の高次機能、5)言語、そして最後に6)バーチャルリアリティーに限ろうと思っている。図に示すように、これらの情報を全て持つ生物は現在地球上には人間しか存在していない。また、地球上で生まれた伝達可能な情報は全て生命活動と連関しており、生命誕生と同時に生まれたゲノムから、約2万年前に誕生する言語まで、それぞれの情報の誕生は、生命の進化の方向性を大きく変化させ、また地球自体を作り変えてきた。
次回から図1に示した、生命情報、というより地球上に順番に現れた様々な情報進化として生物進化を眺め、それぞれの情報を伝達性と、環境同化性の観点から整理してみたいと思う。
ただ、地球に現れた最初の情報、ゲノムに関しては、これまで十分述べてきたので、今回手短に触れておくだけにする。
情報1:ゲノム
ゲノムを一言で定義せよと言われれば、私は「生殖を通して伝えることができる唯一の生物の情報」と定義している。生殖を通してだけ伝わるということは、ゲノムの伝達性は、ほぼ子孫に制限されていることを意味している。すなわち、複製を通して情報が子孫に共有され、それにより生きるためのメカニズムも共有される。
しかし他の生物の遺伝子が一部、あるいは丸ごと統合した名残を現在の生物にも見ることが出来る。例えばミトコンドリアやクロロフィル、あるいは水平伝搬でゲノムに入り込んだDNA断片だ。このため、生殖でしか伝えられないと言ってしまうのは言い過ぎとは思うが、高等動物になればなるほど「生殖を通してのみ伝えられる」という条件に従うようになる。
ただ忘れてならないのは、「生殖を通してのみ子孫に伝わる」というメカニズムと、他の個体の遺伝子を同化する過程を融合させた、「性生殖」という方法が生まれたことだ。
生物学的「性」とは、まさに個体間の遺伝子情報交換のことだ。これは原核生物にも存在し、一つの個体から他の個体に情報が移り、そこで相同組み替えが起こることで、異なる個体間の情報が一つの情報に作り直される。さらにこの方法でゲノム自体のコミュニケーション(相同組み換え)も可能になった。すなわちゲノムは伝達可能でコミュニケーション可能な情報になった。
このスッキリした定義は20世紀になり、少し危なっかしくなった。すなわち、人為的にゲノムを改変することが自由に行えるようになった結果、ゲノムの伝達性に関する制約条件は新たに変わろうとしているが、これについては言語を考えるときにもう一度議論したいと思う。
次に進化を環境の自己への取り込みという観点から見たとき、ゲノムが取りうる方法について見てみよう。
まず環境をRNAやDNAとして直接取り込むことが可能だ。この最たる例が、ミトコンドリアや葉緑体で、最初は体内の寄生生物として存在していたミトコンドリアの遺伝子が徐々に宿主のゲノムに移行して、宿主の自己に一体化していく過程は、まさに環境の取り込みとして見るとわかりやすい。
ミトコンドリアに限らず、環境 を情報として直接取り込む遺伝子伝搬は誕生初期の生物では普通に起こっていたと考えられる。ただ、この方法で直接環境からゲノムを取り込むことは、原始ゲノムから、単細胞、そして多細胞個体へと生物の自己の範囲が拡大するにつれてその頻度は下がっていった。特に多細胞動物になると、自己の制約から完全に独立した情報をそのまま取り込むことは、弊害の方が多くなったのだろう。この危険は、侵入した外来のゲノムの活性化を抑え込むエピジェネティックなメカニズムが進化しているのを見ると理解できる。
このことから、ゲノムは外来のDNA(情報)を容易に受け入れることができるが、自己という制約とは無関係に生まれた情報をそのまま取り込むことは、それがいかにゲノムの多様化に寄与するとしても、危険を伴うことがわかる。
例外として、既に述べたが性生殖という様式により、他のゲノムの断片を、別のゲノムに移すことが可能になっている。この場合、相同組み換えという機構が用いられるが、自己の制約の中で(相同性)ゲノム同士の情報が交換されるという様式が厳しく守られていると見ることが出来る。
もちろん、現在もなおトランスポゾンがゲノムの多様化に寄与する例はあるが、ゲノムが環境をとりこむための過程は、
1)変異と性を介したゲノムの多様化、 2)多様化した情報の翻訳、 3)翻訳された形質の選択 を繰り返すことで進む。
繰り返すが、この稿では選択を環境の同化として捉えていく。誤解を恐れず言ってしまうと、これはキリンの長い首を、丈の高い木の幹という環境が同化した結果と考えることだ。
同じような同化の例として亀の甲羅の進化についての最近の研究を紹介して終わろう。論文のタイトルは「Fossorial origin turtle shell (かめの甲羅は穴掘りが起源)」で、7月号のCurrent Biology (Vol 26:p1887, 2016)に掲載されている。
亀の甲羅の進化は、通常頭などの体の柔らかい部分を隠す硬いシェルターとして進化したと考えられてきた。例えば強い歯や爪を持った天敵の存在が、心臓や肺を守る硬い肋骨の進化を促したとでも考えればいいのだろうか。すなわち天敵のいるという環境圧が硬い甲羅を選択したと考えられていた。
ところがこの論文では、最初からシェルターを肋骨から作ろうとすると、運動能力や呼吸機能が低下し、逆効果になる。一方、亀の甲羅は最初穴掘りに適した骨格として進化したと考えると、2億年から2億5千万年前に生息していたと考えられるカメが、強い肋骨に支えられた前腕、長い爪など穴掘りに適した骨格を持っていることとも話は合うと主張している。
この主張の真偽はともかく、シェルターの必要性の観点から見ると、先に甲羅を発達させるより、確かに穴を掘った方が早い。そして、その後カメだけはこのシェルターとしての穴を、甲羅という形で自己に同化することに成功したと考えると、まさに環境が自己に同化している。
進化での選択を、環境の同化と置き換えてみるのも悪くないと思っていただいただろうか。
さて、次回はまずフェロモンから始める。
[
西川 伸一 ]
情報の進化:1 フェロモンから見る情報の伝わり方と意味
2016年8月15日
情報を伝えるというと、私たちはすぐ何らかの媒体で表現された情報を個体間でやりとりすることを考えるが、原始ゲノムから細胞へと自己を拡大したばかりの単細胞生物では、情報の伝達とは、個体と一緒に同じ情報が増殖することで、この結果、同じ情報を共有した異なる個体が生まれる。もちろんゲノムの複製はゲノムの多様化につながり、同じ情報というのは正確ではないが、ゲノムの伝達のためには複製以外の道はない。
こう言い切ると、「原核生物には水平遺伝子伝播で文字どおりDNAを媒体とした情報を伝えるメカニズムがあるではないか」と指摘を受けそうだ。しかし、ウイルスやプラスミドのような寄生体のDNAを別にすると、水平伝播で伝えられるDNA断片を情報と呼ぶことには問題がある。というのも、多くの場合DNAがゲノムに取り込まれても、取り込んだ方の個体がその情報を解釈する仕組みを持っていないことが多い。例えて言えば、私にとってロシア語の文章が情報になりえないのと同じだ。逆に、解釈できない異なる種由来のDNAを闇雲に取り込んでしまうと、情報が伝わるどころか、自らのゲノムの完全性(genomic integrity)が損われるほうが問題になる。事実、原核生物のゲノムは、環状化し、相同性のないDNAが挿入されないようにして、外来のDNAの侵入に備え、ゲノムのインテグリティーを守っている。
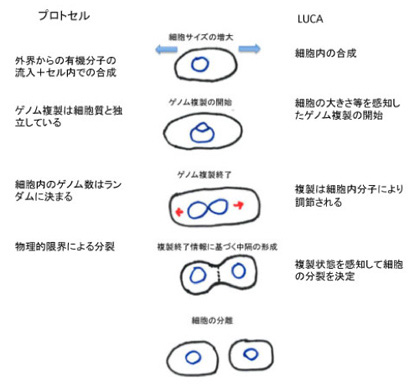
おそらくLUCA (Last Universal Common Ancestor:全生物の共通祖先)が誕生した最初の頃は、ゲノムがコードする分子の特異性も高くなく、少々の外来DNAの挿入は許容され、外来のDNAを積極活用する余地があったかもしれない。しかし、時間をかけて最適な機能分子が進化し、自己の範囲の中で(実際には細胞の中で)厳密な分子ネットワークが生まれると、変異や外来DNAの侵入は、進化には都合が良くても、個体にとってのリスクは大きい。
ゲノムのインテグリティーを守るためのDNA修復機構は、地球上の全ての生物に備わっており、LUCA誕生後おそらく急速に発展したはずだ。自らのゲノムと相同性を持つ場合にのみDNAをゲノム内に受け入れる仕組みは、まずゲノム修復を転用するシステムとして生まれ、その後DNA情報を交換する細胞の「性」の基本メカニズムとして発展する。
いずれにせよ、性を通して自分と相同性が高いDNA情報だけを伝える仕組みが発達し、ゲノム間の部分交換が可能になるまでは、他の個体からDNAが情報として伝えられることはなかったと言っていい。
ゲノムの新しい世代への伝達を生殖(増殖)に限ることにより、一個の個体由来の子孫がほぼ同じ分子を共有できることは重要だ。すなわち、細胞内外の同じメカニズムを全て共有する、自分のコピーが数多く周りに存在することで、様々な刺激に集団が同じように反応するポテンシャルが用意される。すなわち、生命を成り立たせている制約自体を集団へと増殖させることが可能になっている。
フェロモン
このような準備の後、新しく生まれた情報伝達機構が、フェロモンとエピジェネティック機構と言える。フェロモンは現存の原核生物や古細菌から存在しており、一方完全なエピジェネティック機構は真核生物から見られることを考えると、おそらくフェロモンの方が早く誕生したのだろう。
原核生物のフェロモンが最もよく研究されているのがQuorum sensing(クオラムセンシング)と呼ばれる過程だ。そこで、先ずこのQuorum
sensingが何かから見ていこう。
Quorum
Sensing
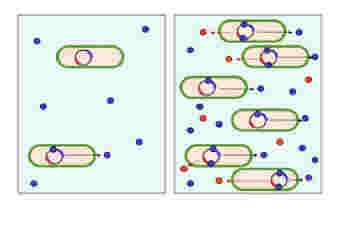
Quorumは日本語で定足数と訳される。すなわち、何かを行う決断するために必要な個体数のことだ。図1に示すように、Quorum sensingは個体濃度を常に測定して、個体数が一定数を超えた場合のみ、特定の分子発現(図では赤丸)のスウィッチをオンにする仕組みだ。
実はこの現象が最初に明らかになったのは、イカに住みついて光を発する発光バクテリアvibrio fisheriの研究からだ。すなわち、vibrio
fisheriが蛍光物質を作るためには、菌がイカの体内で一定の濃度に達する必要があることがわかった。その後この仕組みが、様々な過程に使われていることが明らかになる。例えばQuorum sensingは細菌感染学でも重要な問題になっている。食中毒などのトキシンを分泌する事が出来る菌も、一定の菌数濃度に達しないと毒性を発揮しないことが知られている。このセンサーを破壊して、トキシンの分泌を止めることができると、有効な治療法になる。
Quorum
sensingの分子メカニズムはほぼ完全に解明されている。このメカニズムには、定足数(菌濃度)を教えるための指標(インデックス)となる分子、その分子が一定濃度に達したことを感知する分子、そしてこの認識を様々な物質の生産につなげるための転写活性化メカニズムが必要になる。この分子機構については多くのバクテリアで解明が進んでいるので、ここではグラム陽性菌を例にQuorum sensingに関わる分子機構を示す。
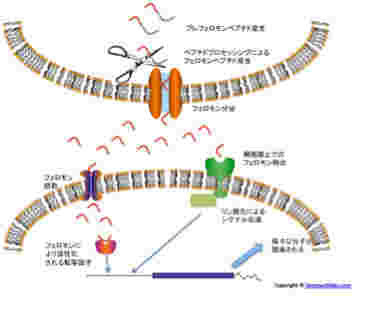
この系で定足数の指標になる分子がフェロモンだ。グラム陽性菌では私たちのペプチドホルモンと一緒で、先ず長めのペプチドが作られ、それが細胞外へ分泌されるとき短く剪定される。この仕組みにより、ペプチドを作った同じ細胞にセンサーが存在していても、一度細胞外へ出たペプチドだけが刺激できるようになっている。
一方、グラム陰性菌ではペプチドの代わりにラクトンを核にした有機化合物を使っている。これはエストロジェン(Estrogen:女性ホルモン)などの核内受容体に対するリガンドと似ていると言えるかもしれない。
Quorum
sensingが働く菌は常にフェロモンを作り続けているが、菌濃度が低いと細胞外のフェロモン濃度は検出感度以下でとどまり、フェロモン受容体は活性化されない。ところが菌数が増えてくると、それに応じて細胞外のフェロモン濃度が上昇し、受容体は活性化され、標的遺伝子の転写のスウィッチが入る。これがQuorum sensingのメカニズムだ。
どちらのタイプのフェロモンにも2種類のセンサーが特定されている。一つは、細胞内に入ってきたフェロモンと結合して、転写活性のスウィッチが入る転写因子で、もう一つは細胞表面上でフェロモンと結合し、リン酸化反応を介してシグナルを伝える細胞表面受容体タイプだ。この構造を見ていると、人間がホルモンとして使っている、核内受容体(例えばエストロジェン受容体)と細胞外受容体(例えば成長ホルモン受容体)などと同じタイプのメカニズムがバクテリアから存在していることがわかる。
メカニズムはこのぐらいにして、フェロモンシステムの進化を考えてみよう。まず、原核生物で見られるフェロモンシグナル伝達システムの基本構造は、その後の生物で普遍的に見られることから、フェロモン自体の進化については割愛して、LUCAがフェロモンシステムを進化させてきた過程について考えてみよう。
理解を容易にするため、ここではフェロモンが細胞内で転写因子に結合して転写を活性化させる系だけを考える。ここで使われている分子メカニズムは、まさに細胞内で合成された分子を使ってフィードフォワードループを動かす系と同じで、あらゆる生物で普遍的に見られる。ジャコブとモノーが発見したトリプトファンに結合してトリプトファンオペロンを抑制するトリプトファンレプレッサーは最も有名な例だ。ただ細胞内部にメッセンジャーがとどまるフィードフォワード回路とは異なり、そのまま、或いはプロセッシングを受けたあとフェロモンとして細胞外に分泌されることで、自分だけでなく他の個体にも作用できるようになっている。
メッセンジャーを細胞内だけでなく、細胞外に分泌できるようにして他の個体にも情報を伝達する進化により、それまで全く単独で生きてきた生物は自己の範囲を広げ、他の個体と情報を共有し、同じ行動を取る一種の社会行動が可能になった。
Quorum
sensingの意義を考えるとき、バクテリアがEPSと呼ばれるポリマーを分泌して集合体を作るバイオフィルム形成過程で、同じ機構が働いていることは興味深い。バイオフィルムは単独では決して形成できない。形成に必要な細胞数に達しているかどうかの情報共有をQuorum sensingは可能にしている。すなわち、自己の範囲を拡大する進化をここに見ることができる。さらに、バイオフィルムは、環境の自己への同化が起こっている例として見ることができないだろうか?
ではこのシステムで生まれた情報の特徴について最後に見ておこう。まず情報の媒体にコード性はない。しかし、記号論的にいうとフェロモンは個体数のインデックスになっている。そしてこのインデックスを解釈する仕組みを共有することで、インデックス自体とは物理的に関係のない物質を作ることが可能になっている。このように、フェロモンシステムはゲノムと異なりコード性は全くないが、代わりにインデックス記号性を持ち、これを介して同時代の他の個体と情報の共有とコミュニケーションが可能になっている。
バイオフィルム形成と同じ情報共有システムはその後、あらゆる単細胞動物で発達を遂げ、多細胞動物への道を開く一つの条件となり、生物の新しい情報の重要な類型となった。
次回は、単細胞生物から多細胞生物への進化に必要だったもう一つの情報伝達・コミュニケーションシステム、エピジェネティック機構について考える。
[
西川 伸一 ]
情報の進化 II クロマチン構造を媒体とした情報
2016年9月1日
フェロモンの次に議論する情報は「クロマチン構造を媒体とした情報」だ。この情報は一般的にエピジェネティックスと呼ばれることが多い。ただ、エピジェネティックスという言葉の指す範囲は曖昧で広い。このため、ここではエピジェネティックスを「クロマチン構造を媒体とした情報」に限定する。
まず簡単に「クロマチン構造を媒体とした情報」、エピジェネティックスについて簡単に解説する。
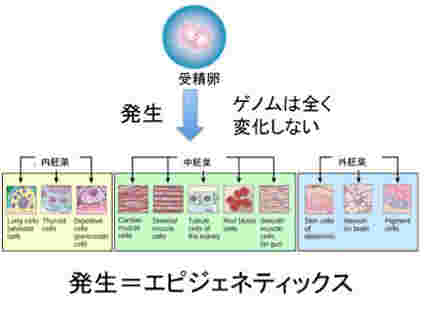
私たち人間は40兆個近くの細胞を持っているが、全て一個の受精卵が発生過程で、発生プログラムに従って様々な細胞に分化した結果だ。リンパ球のような一部の例外を除くと、何百、何千種類もの異なる細胞ができるためにゲノムの変化は全く必要ない。細胞の形は異なり、作られる分子は全く違っていても、私たちの体の中の細胞は全て同じゲノムを持っている。このゲノムの変化なしに異なる性質の細胞が発生し維持されるメカニズムがエピジェネティックスだ(図1)。
次にこの発生の結果何が可能になったか考えてみよう。何百種類の細胞がただ発生したというわけではない。例えば皮膚の細胞は皮膚細胞を作り続け、血液細胞は血液を安定に作り続けることが可能になっている。同じゲノムを持っている細胞同士なのに、決して皮膚の細胞が血液に変わることはない。もしそんなことが一定の確率で起こったら私たちの体の統合性はたちどころに破綻する。
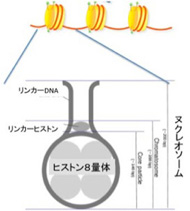
これを支えるメカニズムがクロマチン構造を媒体とした情報=エピジェネティックスで、原則として真核生物で初めて見ることができる。このゲノムとヒストンと呼ばれるタンパク質が互いに協調することで形成されるのが、クロマチン構造で、それぞれの細胞種でパターンが異なる。また、細胞分裂でヒストンが外れても、もう一度同じように再構成できることから、クロマチン構造を繰り返し形成し直すための一種の鋳型ができていると考えると判りやすい(図2)。
このクロマチン鋳型は、全ゲノムにわたって活性化部位と、不活性化部位を区別する印をつけることにより形成される。これらの印は、ノートの開きたい場所と、閉じておきたい場所につける付箋のようなものと考えるといい。
体の全ての細胞には、それが属する種類、すなわち皮膚細胞、血液細胞といった種類に対応する異なる鋳型が存在している。そして何よりも重要なのは、細胞分裂でこの鋳型も複製され、二つの娘細胞に伝わる。このような性質から考えれば、エピジェネティックスをクロマチン構造を媒体とした情報と呼ぶことは何の問題もない。また、この鋳型があるおかげで皮膚細胞は間違って血液細胞や脳細胞になる心配なく、皮膚細胞を作り続けることができる。実際、この鋳型を維持するメカニズムが狂うと、皮膚細胞が思いもかけない細胞へ分化するといった乱れが生ずる。ガンで見られる異型細胞の出現はこの例だ。
ではこのクロマチン鋳型とは何で、情報としてどのような役割を担っているのか見てみよう。すでに図2に図示したように、ゲノムは細胞の種類に応じてヒストンが詰まった閉じた状態と、結合しているヒストンが少ない開いた状態にわかれている。
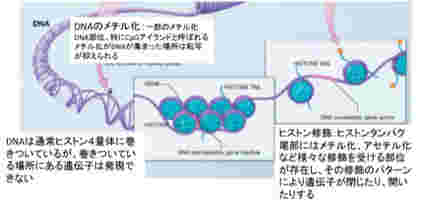
この開いた状態、閉じた状態を決めているのが、染色体と結合しているヒストンのN末端にある領域に存在する数種類のリジン残基のメチル化とアセチル化、そしてDNA自体のメチル化だ。このゲノムの場所特異的なヒストン修飾パターンやメチル化DNAパターンが鋳型として子孫に伝わり、繰り返し働く。これを可能にするのが、発生過程で細胞分化に合わせて鋳型を書き込むメカニズムと、細胞分化のあと完成した鋳型を維持するメカニズムだ。
このメカニズムについての理解は最近急速に深まってきたとはいえ、今も研究途上の分野なので、ここでは解説は省く。ただ、多能性幹細胞を始め、様々な培養細胞のクロマチン鋳型を精密に調べる研究から、
1)細胞が分裂を繰り返しても同じ鋳型が子孫細胞に受け継がれること、 2)多能性幹細胞から様々な細胞系列が分化する過程で、各細胞に特異的なクロマチン鋳型が形成されること、 3)分化細胞をそのまま培養しても普通はクロマチン鋳型が変化することはないが、iPS誘導のように特殊な条件下ではリプログラムが可能で、この時実際に変化するのはこのクロマチン鋳型であること。 などが明らかになった。
この結果は、発生や成長で細胞分化のシグナルに応じてクロマチン鋳型を書き換えるメカニズムと、書き換えたクロマチン鋳型を安定に維持するメカニズムが間違いなく存在することを示している。すなわち、塩基配列のようなコード性は存在しないが、クロマチンのパターンを解釈して複製できることから、エピジェネティックスをフェロモンの次に誕生した情報と呼ぶことができる。
最後にクロマチン構造を媒体とした情報の特徴を、ゲノム、フェロモンと比較しながら見てみよう。
前回 見たように、フェロモンはリアルタイムの個体間のコミュニケーションを可能にした全く新しい情報で、ゲノムだけがどれほど複雑化してもなしえない可能性を拓いた。前回 このフェロモンの役割について、単位あたりの個体数を感知して一定の反応を起こすquorum sensingを例に説明した。ただフェロモンが活躍するのはquorum
sensingだけではない。研究が進むもう一つの領域が、バクテリア同士がプラスミドを受け渡すときに働くフェロモンだ。これによって薬剤耐性が多くのバクテリアに伝搬するため、医学にとっては重要な分野になっている。
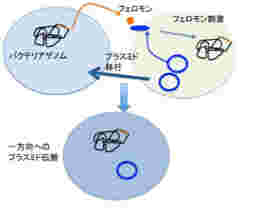
図3:フェロモン刺激によりプラスミドを持つバクテリアから持たないバクテリアへのプラスミドの伝搬が起こる。このメカニズムで薬剤耐性遺伝子が伝播される例が多く知られており、医学でも問題になっている。
図3に示す腸球菌の系では、フェロモンはバクテリアのゲノムにコードされているが、その受容体は薬剤耐性を持つプラスミドにコードされている。この結果、フェロモンに反応するプラスミド(+)バクテリアと、フェロモンを分泌するプラスミド(ー)バクテリア同士が特異的な接合を起こし、プラスミド陰性のバクテリアにプラスミドを渡すことが可能になっている。実際には、プラスミド(+)バクテリアが自分のフェロモンに反応しないよう、うまく抑制システムができているが、詳細は省く。
この現象からわかるのは、フェロモンが引き金となって、DNAを媒体とする情報のやりとりが行われ、この結果、効果が一過性のフェロモンのシグナルが、遺伝子変化として記録されることだ。すなわち、一過性のフェロモンの効果を長期間保持するためには、バクテリアでは遺伝子の変化として記録する必要がある。しかし、プラスミドのような限られた情報の伝搬は簡単でも、ゲノムを書き換えたりすることは難しく、出芽酵母のような一部の例外を除いて、同じ書き換えを繰り返すことは難しい。
一方真核生物への進化により、一過性に誘導される遺伝子発現状態をもとに、クロマチン鋳型を形成する能力、すなわちエピジェネティック過程が誕生すると、遺伝子の書き換えなしに、外界からのシグナルを特定のクロマチン構造として書き残すことが可能になる。
これをバクテリアがゲノムに記録する場合と比べると、外来の情報を持続的に記録するという点では同じだが、
1)記録が書き換え可能 2)多くのシグナルに対応して記録が可能。 3)同時に多くの個体がシグナルを共有し、それを同じ記録として維持することが可能。 などの、ゲノムでは不可能とは言えなくとも、簡単ではない記録が可能になっている。
これがクロマチン構造を媒体とする情報の誕生により生まれた可能性で、この獲得には20億年、生物の進化全過程の半分以上の時間が費やされている。次回は、この新しい情報の進化と、この情報がもたらしたインパクトについて考える。
[
西川 伸一 ]
外界の情報を記憶するためのエピジェネティックス
2016年9月27日
前回 「クロマチン構造変化を媒介とする情報(<エピジェネティックス)」が、
これを読んでいる読者のほとんどは、ルイセンコの名前を聞いても誰かわからないだろう。ルイセンコは、メンデル遺伝理論だけでは説明がつかなかった植物の現象を捉えて、獲得形質は遺伝することを主張したソビエトの農学者だ。彼を政治的に支持したスターリン政府の後ろ盾を得て、論敵を逮捕・追放したことで、科学的議論に政治を介入させたとして科学史に大きな汚点を残した人物だ。彼の理論は我が国にも様々な影響を残したようだが、これは私が大学に入学するより前の話だ。幸い、ルイセンコと彼の理論をめぐる我が国での議論については本館名誉顧問の岡田節人先生が生命誌ジャーナル に紹介されているのでぜひ読んでほしい。
さてルイセンコがメンデル遺伝学の反証の根拠にしたのが「春化(春処理)」と言われる現象で、植物を低い温度に晒すことで開花時期が調節できるという現象だ。低温という環境で獲得した形質が、世代を超えて伝わる場合もあることから、獲得形質が遺伝すると考えたようだ。結局エピジェネティックス(遺伝した後)の問題で、ゲノム自体の変異を基盤とする遺伝学の問題でないことが明らかになる。このように、春化メカニズムは、エピジェネティックス、すなわちクロマチンの構造を介した情報の問題として現在解明が進んでいる。外界からのシグナルがクロマチン構造を媒体とする情報として書き換えられるメカニズムを理解するのにうってつけの例なので、まずこの春化とそのメカニズムについて見てみよう。
各々の植物は発生過程で開花を調節する機構を確立する。これには温度や日照時間を感知しながら様々な遺伝子の発現を調節する複雑なメカニズムが関与する。話をわかりやすくするために、実験のためのモデル植物として研究されているシロイヌナズナの開花を抑制するマスター遺伝子FLCに絞って春化の現象を解説する。
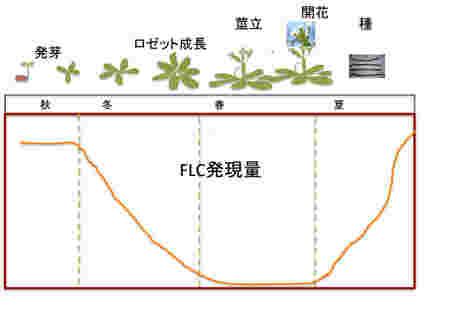
まず越冬一年草型シロイヌナズナのライフサイクルを見てみよう。秋に発芽、ロゼット型葉を形成してゆっくり成長しながら越冬する。その後、茎が伸びて開花、そして夏になると種ができる。この間の開花抑制遺伝子FLCの発現を見てみると、発芽時の秋には最も高いレベルにある。しかし、ロゼットが形成される冬には急速にそのレベルが低下し、春の開花期には0になる。開花が終わると夏に向けて急速に発現レベルが回復する。
FLCが開花抑制に関わることを頭において発現の季節パターンを見ると、開花の起こる春以外は開花抑制遺伝子であるFLCを発現させ、間違った時期に開花が進まないようできているのがわかる。すなわち、秋から冬にかけて気温が下がり始まるのを合図に、FLCの発現を安定に抑制するための準備を始め、この状態で急速に温度が上がると、開花を優先した植物の発生が進み、開花する。その後、種ができ、発芽するまでにFLCの発現を戻して開花を抑え、植物はエネルギーを成長に使うことが可能になっている。
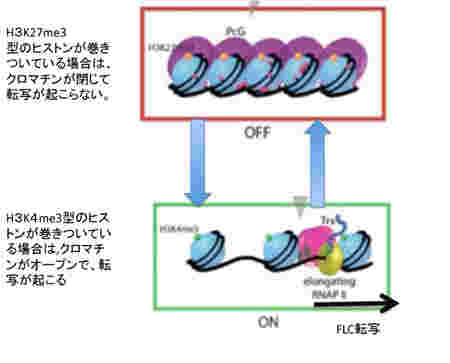
次に、このパターンの背景にあるメカニズムを細かくみていこう。この季節に合わせた発現の調節にはFLC遺伝子領域とそこに結合しているヒストンのメチル化パターンが大きな役割を演じている。すなわちFLCの発現を抑えるときはこの領域に巻きついているヒストン3のN末27番目のリジンがメチル化されており(H3K27me3)、一方発現が高いときは4番目のリジンがメチル化されている(H3K4me3)(図2)。すなわち、クロマチンが閉じて転写が抑制されるか、あるいはクロマチンが開いて転写が行えるかは、ヒストンの標識の違いによって決まる。
http://www.stembook.org/node/585.html )
つまり、FLCに巻きついているヒストンのメチル化の異なる2つの状態を温度スウィッチでシフトできるようになっている。このようにクロマチン構造を媒体とする情報の誕生は、外界の変化を細胞自体の記憶に変えることを可能にした。
このヒストン標識によるクロマチン構造のスウィッチのメカニズムについてはずいぶんわかってきたが、複雑でその全像について解説するには本1冊必要になる。とりあえず、図にあるように、クロマチンの構造を維持する鍵になる分子が、ポリコム複合体とTrithorax複合体であることを理解しておけば十分だろう。
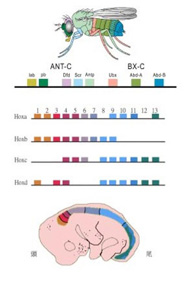
H3K4のメチル化と、H3K27のメチル化パターンを転換させクロマチン構造を変えることで大きな領域の遺伝子発現を調節するメカニズムは、実は酵母から人間まで保存されているメカニズムだ。事実、ポリコム複合体やTrithorax複合体という名前はショウジョウバエ突然変異の研究が由来となっている。例えば、ショウジョウバエから哺乳動物まで、体の前後軸に合わせて体節の特異性を決めているHox遺伝子が集まる大きなゲノム領域のどこまでを活性化し、どこまでを不活化するかは、まさにこのクロマチン構造変化により調節維持されている。
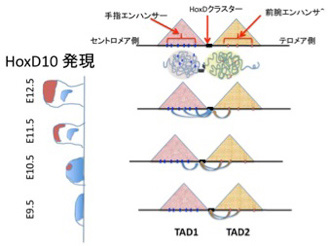
図3は哺乳類の発生でのHox遺伝子領域のヒストン標識パターンを図示しているが、Hox遺伝子の発現はクロマチン構造の変化で調節され、植物とほぼ同じメカニズムが使われていることがわかる(図3)
図3 クロマチン構造変化によるマウスHoxa1-13遺伝子の発現調節。内部細胞塊のような多能性幹細胞ではHox領域は完全にH3K27me3ヒストンで標識され、発現が抑えられている。前から後ろの体節に移行するのに合わせ(i)(ⅱ)(ⅲ)、Hoxa1からH3K4me3ヒストンは拡大していく。http://rstb.royalsocietypublishing.org/content/368/1620/20120367 )
最後に、春化時のクロマチン構造の変化の際、他生物で見られない特徴について見ていこう。実は、FLC遺伝子発現を抑制するH3K27me3標識の範囲の量を調節できるようにできている。すなわち寒い時期が長いと、H3K27me3が結合するFLC遺伝子領域が拡大し、暖かくなってもこの抑制標識を外しにくくなる。これは、低温に長くさらされた植物の場合、開花が早くなり、開花期間は長くなり、さらに開花量も上昇するという量的な変化が、FLC遺伝子に結合するH3K27me3の量的な変化と相関していることを意味している。このように、外界からの情報を細胞内に量的な記憶として残すことができるのも、クロマチン構造を媒体とする情報の特徴だ。これをゲノム自体の調節機構で実現することはほぼ不可能だ。
春化を例に、クロマチン構造を媒体とする情報が、外界の情報を、細胞自体の情報に書き換えて記憶することを可能にしていることを示した。重要なことは、この記憶が書き換え可能で、量的にも変化させることが可能なことだ。進化が環境の自己への取り込みであるという観点から見ると、クロマチン構造を媒体とする情報は、ゲノムよりはるかに迅速に環境の自己への取り込みを可能にした新たな情報記憶の登場といえる。
今回例として使った春化では、環境の温度がクロマチン構造の情報として書き換えられる。一方、クロマチン構造の書き換えはフェロモンによっても誘導することができ、生命進化で誕生した新しい2種類の情報がここで出会う。すでに述べたように、フェロモンは個体間、細胞間のコミュニケーションに関わる情報と言える。一方、今回見てきたようにクロマチン構造を媒体とする情報は記憶媒体と言える。このように、コミュニケーションと記憶が揃った時、生命進化が大きく進む。こうして可能になったのが多細胞動物だ。次回はこの進化過程について考えてみる。
[
西川 伸一 ]
コミュニケーション・伝達・記録
2016年10月3日
前回 まで、ゲノム、フェロモン、クロマチン構造が媒介する情報と進化で生まれた新しい情報について見てきた。これらの情報を、伝達、コミュニケーション、記録という3つの情報機能について見直してみよう。
伝達、コミュニケーション、そして記録は情報が可能にする重要な機能だ。ゲノムはこれらすべての機能を併せ持っている。新しく生まれた情報には伝達機能は存在するが、フェロモンには記録という機能はなく、クロマチン構造を媒介とする情報はコミュニケーション機能を持たない。前回述べたが、フェロモンとクロマチン構造はゲノムの持つ情報を補完するように別々に誕生し、真核生物になると統合された情報システムへと発展する。そしてこの統合から生まれた新しい可能性が、多細胞動物の誕生の基盤になる。今回は、情報の記憶とコミュニケーション機能について整理をした上で、多細胞体制が生まれるまでに、生物の情報システムがどう発展したのか整理しよう。
まず、フェロモンやクロマチン情報が必要とされた背景、情報としてのゲノムの限界から見てみよう。
いうまでもなく、細胞が複製できるのは、ゲノムがDNAを記憶媒体として使って生物のオペレーションを指示する情報として働いているからだ。この記録機能と記録の伝達の原理については、DNAが2重螺旋構造をしていることが発見された時、解明されたと言っていい(図1)。
図1 2重螺旋の複製。2重螺旋が一本鎖にほどけ、それが2本の2重螺旋になることがDNAの構造から明らかになり、伝達と記録機能の原理が理解された。(wikipediaより)
ではコミュニケーション機能はどうだろう。複製されたゲノムは2つの娘細胞に伝わる。これは生殖を通しての情報伝搬だが、コミュニケーションではない。
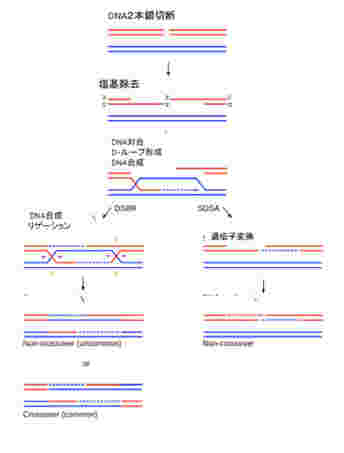
ゲノム同士のコミュニケーションは基本的に相同組み換え機構を介して行われる。私たちの体細胞には、母親からの染色体と、父親からの染色体が存在するが、条件が整うと両方の染色体同士で相同組み換え(図2)が起こり、染色体の部分交換がおこる。これにより異なるゲノム同士のコミュニケーションが可能になる。
この機構はほぼすべての生物で保存されており、大腸菌から人間まで、異なる個体のゲノム同士のコミュニケーションにはこの機構が使われる。ただ、相同組み換えが起こるためには、DNAの切断が必要で、実際には放射線などによるDNA切断に対する修復機構として進化してきたと考えられる。通常の状態で相同組み換えが起こるためには、DNAを自然に切断する過程が必要で、細胞にとっては危険極まりない。このため多くの生物では、この機構を通したゲノム間のコミュニケーションが高い確率で起こる状況は限られている。例えば、人間では生殖細胞の減数分裂過程に限られ、体細胞で起こる頻度は低い。
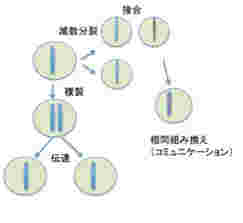
このように、ゲノムの記憶、伝達、コミュニケーションの様式を見てみると、全てが生殖サイクルと完全に一体化していることがわかる。単細胞動物では、異なる個体同士が接合するとゲノムレベルのコミュニケーションが起こるのを観察できるが、コミュニケーションの範囲は1対1に限られており、一つのゲノム情報が同時に異なるゲノム情報とコミュニケーションすることはない(図3)
図3: ゲノムには情報が記録されており、複製を通して娘細胞に伝達される。また、接合、ゲノム間の相同組み換えにより、他の個体のゲノムとコミュニケーションできる。ただ、図からわかるようにゲノム情報の伝搬、コミュニケーションは全て一対一で個体(細胞)が対応しており、同時に複数の個体とコミュニケーションしたり伝達することはない。
ではなぜコミュニケーションが必要か、その利点を考えてみよう。ダーウィン進化を現代的に翻訳すると、様々な様式のゲノムレベルの多様化がまず起こり、ゲノムの多様化が形質の多様化として反影されると、この形質の環境適合性を指標に生殖優位性での差異が生じ、環境に適応した個体の比率が高まることで進化が進むと言えるだろう。このゲノムの多様化の一番の駆動力は、DNA複製に必ず伴うエラーだが、もう一段質の高い多様化の駆動力が相同組み換えによる多様化だ。
全くランダムな多様化と比べると、相同組み換えによる多様化は、ゲノムレベルのコミュニケーションを基盤にしている点が大きく異なる。通常これが起こるのは性生殖だが、この場合異なる環境で生きてきた個体がそれぞれ持っているゲノム同士の部分を交換し合う。視点を変えてこの過程を見てみると、その種が分離してから世代を重ねてきた異なる個体のゲノム同士、いわば環境によりすでに「テスト済み」のゲノム同士で情報交換が行われていることを意味する。それぞれの個体のゲノムがその個体が出会ってきた環境を同化していると考えると、この環境との相互作用の歴史が一つのゲノムの中へ再構成されているとみることができる。言葉を変えると、ゲノム間のコミュニケーションにより、より多くの環境との出会いが、ゲノムに同化される。これがゲノム間でコミュニケーションが行われることの重要な役割だ。
この様にゲノムには、情報としての全てが備わっている様に思える(事実それが進化の原動力となってきた)が、特定の生物集団の生存から見た時、ゲノムの対応能力には限界がある。すなわち、ゲノムだけで環境の変化に対応しようとすると、伝達やコミュニケーションが1:1に限られ、空間的にも、時間的にも急激な環境変化には対応できない。この限界を埋めるのが、フェロモンと、クロマチン情報だ。
詳しく検証したわけではないが、フェロモンは、細胞内の分子間相互作用ネットワークが、細胞外へ拡大したものと考えられる。フェロモンは接合の相手を惹きつけ、接合時の方向性(オスメスと考えて貰えばいい)を決める過程にしばしば登場する。これは1:1の個体間相互作用と言えるが、他にもクオラムセンシング(前々回 )のように1:1の限界を超え、同時に多くの個体とコミュニケーションをとりあう手段を提供し、全ての個体が環境に対して同じように反応するための情報としても働いている。
この様に、生存環境に関する情報を他の個体と同時的に共有することを可能にしたのがフェロモンの機能だ。フェロモン自体の情報には記録機能がないため、フェロモンのシグナルは一時的な反応を誘導して終わるか、あるいはフェロモンの情報を引き金に、遺伝情報を書き換え(酵母の交配型の変換)や、プラスミドを介したゲノム情報のやりとり(前々回 )を行うことで、経験が記録される。このゲノム自体の書き換えの代わりに、クロマチン情報の書き換え機構とフェロモンシグナルをリンクさせることもできる。実際、クロマチン情報の書き換えが、反応の多様性、伝達範囲の大きさ、伝達と記録の迅速性の点で、ゲノムの書き換えをはるかに凌駕しているため、これがその後の生物の主要な伝達様式になっていく。
前回 みた様に、クロマチン構造を媒介とする情報は、書き換え、すなわち繰り返して記録が可能だ。このメカニズムが完成するのは、おそらく真核生物以降だが、これに必要な個々のメカニズムは原核生物や古細菌で進化してきた。事実DNAメチル化は原核生物から存在するし、ヒストンと相同性を持つタンパク質も古細菌から認められる。更には、遺伝子の相同性は欠如しているが、DNAと結合してヌクレオソーム構造を形成するためのタンパク質は原核生物にも存在している。
この様なヌクレオソーム構造が広く認められることは、プラスミドの様な小さなゲノムは別として、メガベース以上の大きさのゲノムは裸のままで存在することが不可能であることを示している。実際、バクテリアやアルケアでは、1mmの長さのDNAを1ミクロンの大きさの細胞内に安全に収納している。その上に、収納した全ゲノムをなんども複製することが求められる。ヒストンの様な、DNAをコンパクトに巻き取る仕組みなしには、ゲノムサイズの急速な増大はありえなかっただろう。
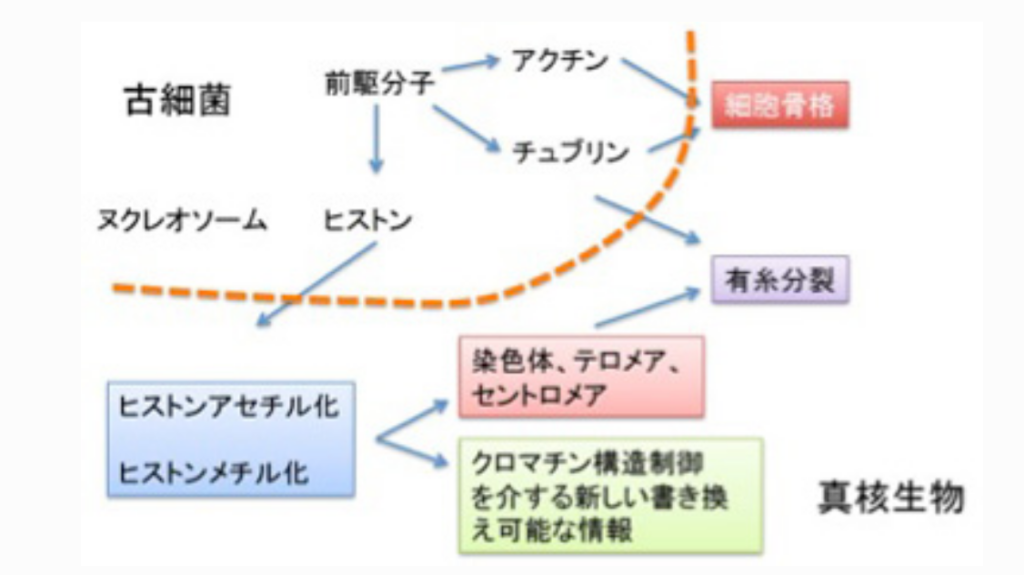
真核生物の誕生にはヒストン修飾を基盤とするクロマチン構造制御機構、分裂時の染色体分離に必要なチュブリン、そして形態や細胞分裂を制御できる細胞骨格分子アクチンが必要だが、この3種類のタンパクは同じ分子からできてきたと考える魅力的な仮説がある。すなわち、いずれもリン酸化やアセチル化による修飾を介した細胞の構造変化に関わる。この考えを採用した、真核細胞進化過程について図3にまとめてみた。
ここでは話をヒストンに限るが、最初DNAをコンパクトに折りたたみ保護するヌクレオソーム形成分子として誕生したヒストンは、N末端に集まるリジン残基のアセチル化/脱アセチル化、メチル化/脱メチル化を介する修飾により、単純なヌクレオソームから、各ゲノム領域を構造的に標識するクロマチン構造へと発展した。これにより、テロメアやセントロメアのように、有糸分裂に必要な条件が整った染色体が生まれる。そしてゲノム領域を構造的に標識するヒストンの同じ能力が、遺伝子発現調節に使われるようになったのが、クロマチン情報だ。
春化の例でクロマチン情報は、環境のストレスを、多くの個体が同時に、同じシグナルとして感知し、このシグナルを同じ様に記録することを可能にしている。このようにクロマチン情報は複数の個体が同時に共有できる、ゲノムではなしえなかった情報と言える。
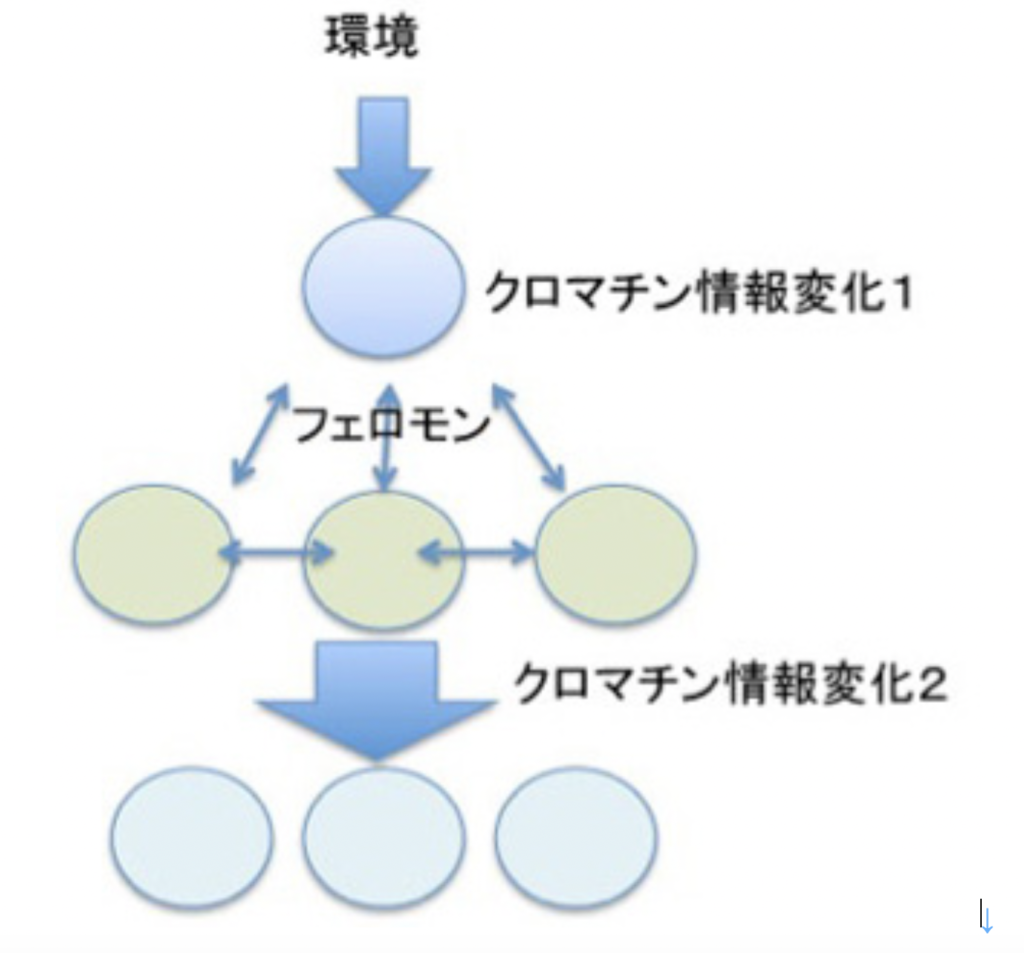
最初環境ストレスに対する反応として誕生したクロマチン情報の書き換え機構に、フェロモンによる細胞間情報共有機構が統合されると(図4)、それ自身では互いに未完成であった情報が補い合って、コミュニケーション、伝達、記録のすべて備わった新しい情報システムが完成する。
図4で示した構造をよく見てもらうと、ある環境シグナルに対して直接対応する細胞と、その後フェロモンの作用で反応する細胞が別々に描かれているのに気づいてもらえたと思う。これは多細胞体制を想定して描いている。多細胞体制では、個体と環境、個々の細胞と環境、個々の細胞間、そして個体と個々の細胞間の4種類の関係が成立しており、この関係から生じる細胞の変化はすべてゲノムの変化を伴わない、クロマチン情報の変化が背景にある。例えば、個体と個々の細胞の関係には、同時的な情報の共有と、細胞レベルの経験の記録が必須で、これはクロマチン情報とフェロモン情報(細胞間情報伝達機構)だけで行われている。逆に多細胞体制成立から考えると、フェロモン情報とクロマチン構造を介する情報が誕生し、それが統合されることが、多細胞体制誕生の必須の条件であることになる。
[
西川 伸一 ]
新しい情報と進化
2016年10月17日
前回 まで、ゲノム、フェロモン、クロマチン構造が媒介する情報と進化で生まれた新しい情報について見てきた。これらの情報を、伝達、コミュニケーション、記録という3つの情報機能について見直してみよう。
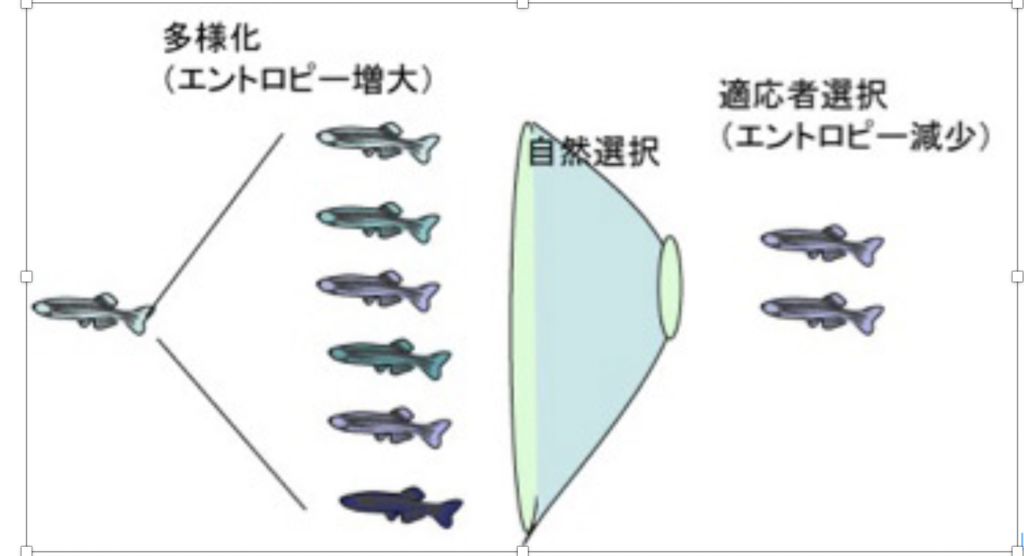
進化についてのダーウィンの考えは、「集団は本来多様化する傾向を持っており、この多様化した個体の中から、環境に適合した個体が選択される」というものだ。ただ当時は全く理由の分からなかった個体の多様化の背景には、形質(フェノタイプ)よりはるかに大きな、ゲノムレベルでの多様化がある。
ゲノム情報の多様化はエントロピーの増大と同じで物理的に自然におこる。この多様化したゲノムに対応する形質が環境にフィットした個体が選択されることになるが、これにより多様性(エントロピー)は、低下する。
この過程を単純な図式にすると図1のようになるが、この過程がただ続くとすると、せっかく獲得したゲノムの多様化も、選択により打ち消されるため生物が多様化する方向には進まないことになってしまう。
実際、全球氷結や隕石衝突など、生命自体にとって極端な条件が生まれると、ほとんどの種が絶滅し、生命の多様性は極端に低下する。ただ、通常はこのような条件が生まれるのは稀だ。なぜなら、地球は広く多様な環境が存在しているため、環境の違いだけ、それを同化した生物も多様化することになる。
ただこの説明のほとんどは、生命の情報としてゲノムしか想定していない。しかし私自身は、情報であれば全て進化に関わるものとして扱おうと考えて、これまで生命から生まれた全ての情報をリストする作業を進めてきた。もしフェロモン及びクロマチン構造を媒体とする情報のセットを生命の情報として認めるなら、当然この情報の多様化を統合して生物進化を考える必要がある。
そこでまず、フェロモンとクロマチン情報が新しい情報として加わることで、進化過程がどう変わるのか見てみよう。ダーウィン進化で問題になる情報は遺伝可能な情報であるという縛りがかかる。だとするとこの条件を満たす情報はフェロモンではなくクロマチン情報になり、クロマチン情報だけがダーウィン進化の駆動力として働く資格があるように見える。
しかし多様化できる情報をゲノムに限定しない新しい進化過程を構想するとき、フェロモンは記録情報でないからといって無視してもいいかというと、答えはノーだ。実際にはフェロモンにより新しい能力を獲得した集団が、環境を書き換えることで、能力の効果を記録してしまうことがありうる。例えば、古い旧家で何代もの子供が育ったとすると、先祖の建てた家という環境が、そこで育った子供たちに繰り返し制約を加える。この制約による変化も、ある意味で遺伝していると言って良い。
単細胞動物でも、多細胞動物でも、フェロモンは個体同士、細胞同士の行動の統合を可能にする仕組みだ。例えばクオラムセンシングを考えてみよう。この仕組みはフェロモンの濃度を感じて、周りに集る個体の濃度を感じ、十分な個体が集まったときに環境へ働きかけ、環境を自らの生存に適すように作り変えるのに使われている。このように、フェロモンに記録機能はなくても、環境側を変化させることで子孫へと一種の記録を残すことができる。この、環境を変化させるという記録の仕方は、後で神経細胞による情報を考えるとき重要になる(図2)。
他に、フェロモンは個体に働きかけ、接合を誘導したり、プラスミドを伝達したり、様々な方法で、ゲノムの多様化を促進する働きがある。こうして起こる多様化は、突然変異によるランダムな多様化ではなく、相同組み換えに基づくことで、多様化による生存への脅威を制約できるようになっている。すなわち、これまで生存を支えてきたゲノム情報の上に少しだけ変化を加える漸進的進化に適した変化の基盤になりうる。
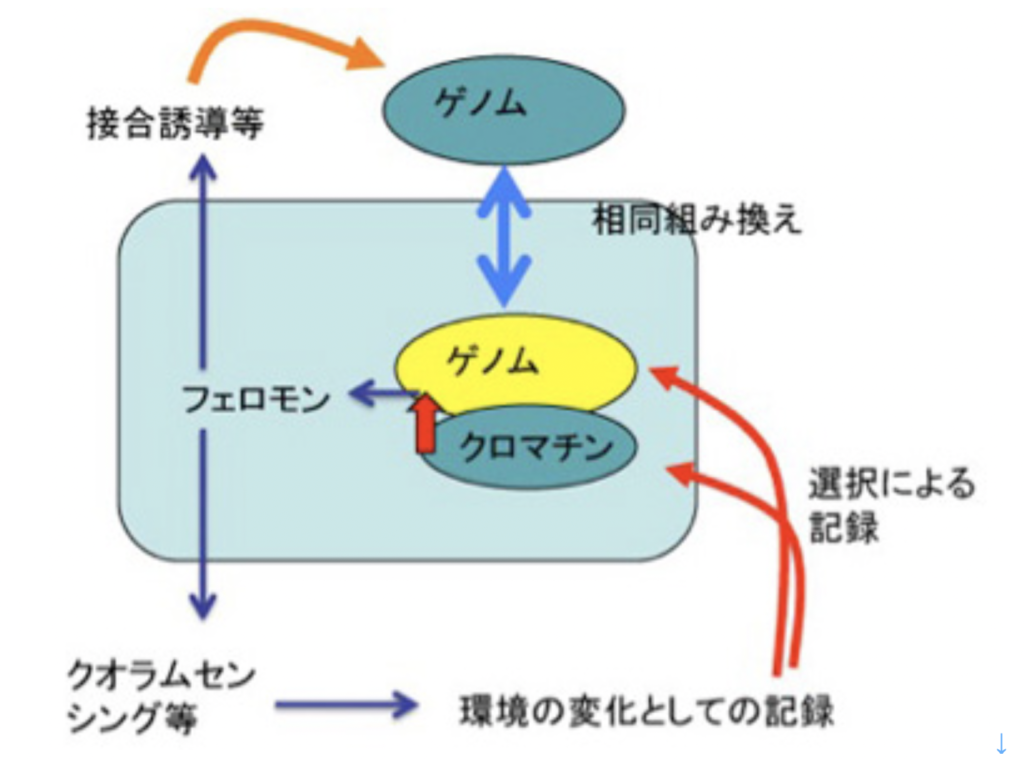
一般的には、ダーウィン進化の駆動力、ゲノムの多様化は、DNA自体の化学的・生物学的性質により、自然に起こると考えられている。しかし、フェロモンが加わることで、変化させられた環境による新しい様式のゲノムや、クロマチン情報の選択が起こるようになる。また、接合誘導のような他の個体への働きかけの結果が、相同組み換えのような、単純なランダムなゲノムの多様化とは異なる、より制約を受けた様式による多様化が可能になる。このように、フェロモンだけでも、ゲノム多様化の様式を大きく変革できる(図2)。
次に、記録できる新しい媒体クロマチン情報は、それ以前の進化過程をどのように変化させただろうか?
前回 述べたように、ヒストン修飾やDNAのメチル化を介したクロマチン情報は、テロメアやセントロメアの形成を通してゲノムを構造化することに成功した。これにより、環状DNAでは限界があったゲノムサイズの増大が可能になる。そして、同じクロマチン構造変化を誘導するメカニズムが遺伝子転写のOn/Offを指示する情報へと発展する。このクロマチン情報によって、遺伝子発現パターンの調節、記録、そして子孫への伝達が可能になっている。
クロマチン情報で常に問題になるのが、「エピジェネティックな記録は子孫に伝わるのか?」という遺伝の問題だ。しかし、多くの細胞は分裂を繰り返しても、同じクロマチン情報を維持できる機構を有しており、原理的にはクロマチン情報は遺伝できると考えていい。
もちろん多くの動物の初期発生過程では、卵子と精子などの配偶子が持っていたクロマチン情報が一旦キャンセルされたあと、体細胞とともに生殖細胞が新たに発生する。従って、新しい個体が発生する過程では、親の持っていたクロマチン情報は消えることが多い。ただ、iPSリプログラムによるクロマチン情報の変化についての研究からわかったように、クロマチン情報を完全にリセットできないケースがある。このような場合、エピジェネティックな状態が子孫に伝わったとして、大きく取り上げられることになる。
いずれにせよ、単細胞生物や、あるいは培養細胞のクロマチン情報を調べた研究から、細胞分裂を経てもクロマチン情報は維持され、子孫に伝達されるのが普通だ。したがって、単細胞動物の進化過程では、クロマチン情報も子孫に伝達される情報として、進化過程の駆動力として貢献できたはずだ。
次にクロマチン情報が加わると、どう進化は変わりうるだろう?
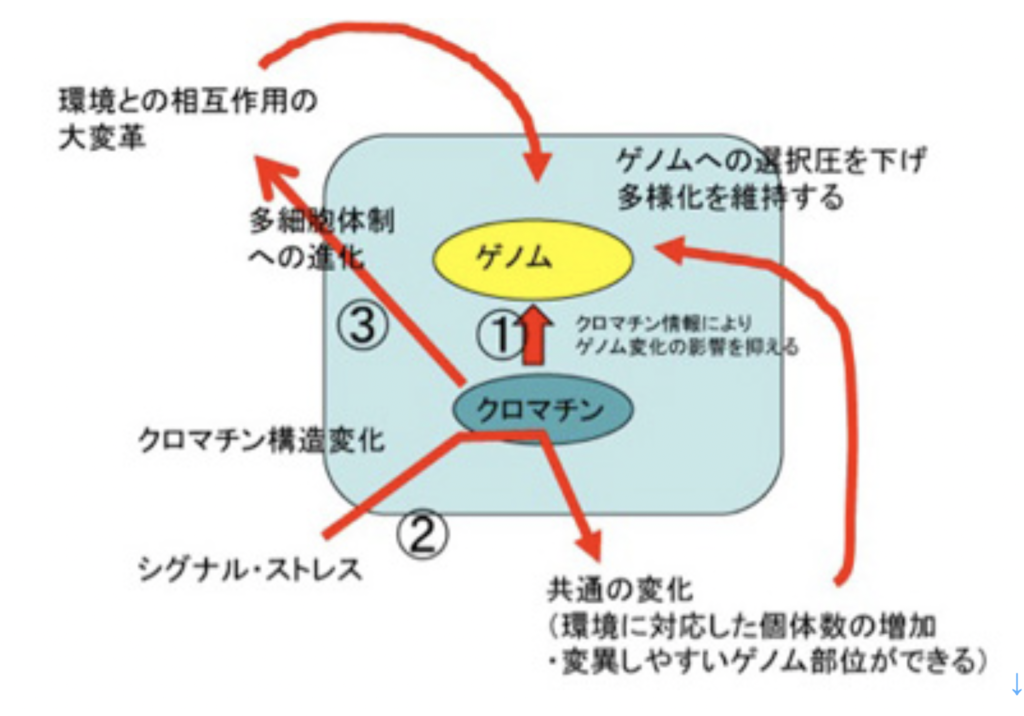
①クロマチンによるゲノムの構造化により、ゲノムサイズや複雑さを格段に高めることに成功した。ただ、サイズの大きい複雑なゲノムになるほど不安定性は増し、またゲノムに大きな変化が起こることは当然個体の生存にとっては大きな脅威になる。しかし、クロマチン構造変化を介する情報が利用できると、ゲノムの変化に伴う個体への影響を減らすことができる。 ②クロマチン情報は、環境ストレスやフェロモンシグナルに対して、多くの個体が同時に一定の反応を起こし、新しい状況に適応することを可能にする。例えば細胞増殖速度を落とし、あるいは環境変化に強い細胞を形成するなどがそうだ。この環境への早い一様の対応により、クロマチン情報誕生前はゲノム情報がそのまま形質に反映し、その適合性で個体自体選択されていた状況は大きく変化する。すなわち、様々な環境変化やシグナルに対し、クロマチンシグナルによりまず多くの個体が共通の反応を起こし適応する。このクロマチン情報レベルの変化は、環境に適応した個体数を増やし、またゲノム内で変化しやすい部位とそうでない部位の違いを生み出す。選択を受ける個体数が多いと、選択後の個体数の増加が望める。また、変異が選択的に起こることで、生存への選択圧を下げたり、あるいは上げたりしてより環境に適合(選択圧を下げた)した状態でのダーウィン進化が可能になる。 ③あまり議論しなかったが、フェロモンとクロマチン情報は多細胞体制誕生に必須の条件だ。多細胞生物では、フェロモンを起源とする様々な細胞間シグナル伝達分子により、細胞のアイデンティティーが決められるが、アイデンティティーの確立には全てクロマチン情報の書き換えが必要になる。もちろん、多細胞体制への進化には他にも様々な条件が必要だが、細胞間シグナル伝達と、クロマチン情報は中でも基本中の基本条件になっている。こうして多細胞体制が生まれると、環境と個体との相互作用のあり方が大変革する。すなわち、個体の異なる構成部分は環境と異なる様式で関わる。例えば、葉で太陽を利用し、根は地下で水を利用する。この環境との相互作用の様式の大変革が、進化の様式を多様にし、例えばカンブリアの大爆発をもたらすことになる。
以上、クロマチン情報とフェロモンが情報に加わることで、進化の様式が大きく変革することを理解してもらえたのではないだろうか(図3)。
これまで、進化の様式が大きく変化するためには、選択圧が高まることの必要性が強調されることが多かった。しかし、情報を統合的に考えることで、私は逆に淘汰圧が下がり、最終的に種の多様化を決めるゲノムの多様化が保障されることが、生命の多様化には重要でないかと思っている。これまで述べてきたように、ダーウィン進化の結果は環境の自己への同化だ。多くの環境要因を同化できるということは、種が多様化することと同じだ。図1に示したゲノムしか情報がない場合の単純な進化過程をいくら積み重ねても、真核生物誕生後の急速な進化を説明することはできないのではないだろうか。ただ残念ながら、これは私の個人的意見に過ぎないと断っておく。
ゲノム、フェロモンからクロマチン情報へと進んだ情報の多様化と統合過程の繰り返しが、次は神経細胞の誕生から始まる。
[
西川 伸一 ]
動物と神経の誕生
2016年11月1日
神経系がゲノムやクロマチン情報とは全く異なるレベルの情報システムを形成していることは明らかだ。ただ、これは神経系が高度に発達した動物についての話で、神経細胞誕生=新しい情報の誕生ではない。即ち、無生物から生物が誕生した過程と同じ問題が、神経系から新しい情報が生まれる過程に存在している。そこで、今回から神経細胞の誕生によって可能になった情報システムの成立について、動物進化過程を振り返りながら考えようと思っている。
この新しい情報システムは、もちろんゲノムやクロマチン情報とは密接な相互依存関係にあるものの、半独立の情報システムを形成していると言える。
例をあげて説明しよう。これまで述べてきたフェロモン、クロマチン情報は、ゲノム情報から独立して情報として働くことはできない。例えば、クロマチン情報はゲノムを構造化するとともに、この構造を変化させることでゲノム上の様々な大きさの領域にある遺伝子が利用可能かどうかを決定する(65話図3 )。すなわち、クロマチン情報はゲノムとの関係を前提に複製可能で、その情報はゲノム上の遺伝子発現の違いとして表現される。誤解を恐れず例えるなら、ゲノム上の遺伝子の発現を指令するアルゴリズムと言える。
同様にフェロモンも、クロマチン情報やゲノム情報の変化を誘導することが主要な機能だ。フェロモンやクロマチン情報は独自の情報として振舞っても、ゲノムから決して独立することはない。
しかし、神経系による情報の解釈、生成、伝達は、ゲノムは言うに及ばず、クロマチン情報からもかなりの程度独立していると考えられている。実際、人間の脳が生み出した情報は、ゲノムやクロマチン情報からは独立している。だからこそ、神経系をコンピュータで再現できると考える科学者は多いし、また脳自体をコンピュータの一種として理解しようとする科学者は多い。
私自身は、神経を媒体とする情報システムは、コンピュータと同じで、神経細胞同士が階層的なネットワークや回路を基盤にしたシステムだが、その回路自体がクロマチン情報やゲノム情報と相互作用できることが、神経系独自の情報システム形成に重要な役割を果たしていると思っている。ただ、この問題については最初から議論するのを避けて、まず神経細胞の誕生から脳の誕生に至る神経系の進化を段階的に見ていきながら、それぞれの段階で神経系を情報の観点から眺め直すとともに、結合性とクロマチン情報や、ゲノムなどの下位の情報との相互作用について考える。
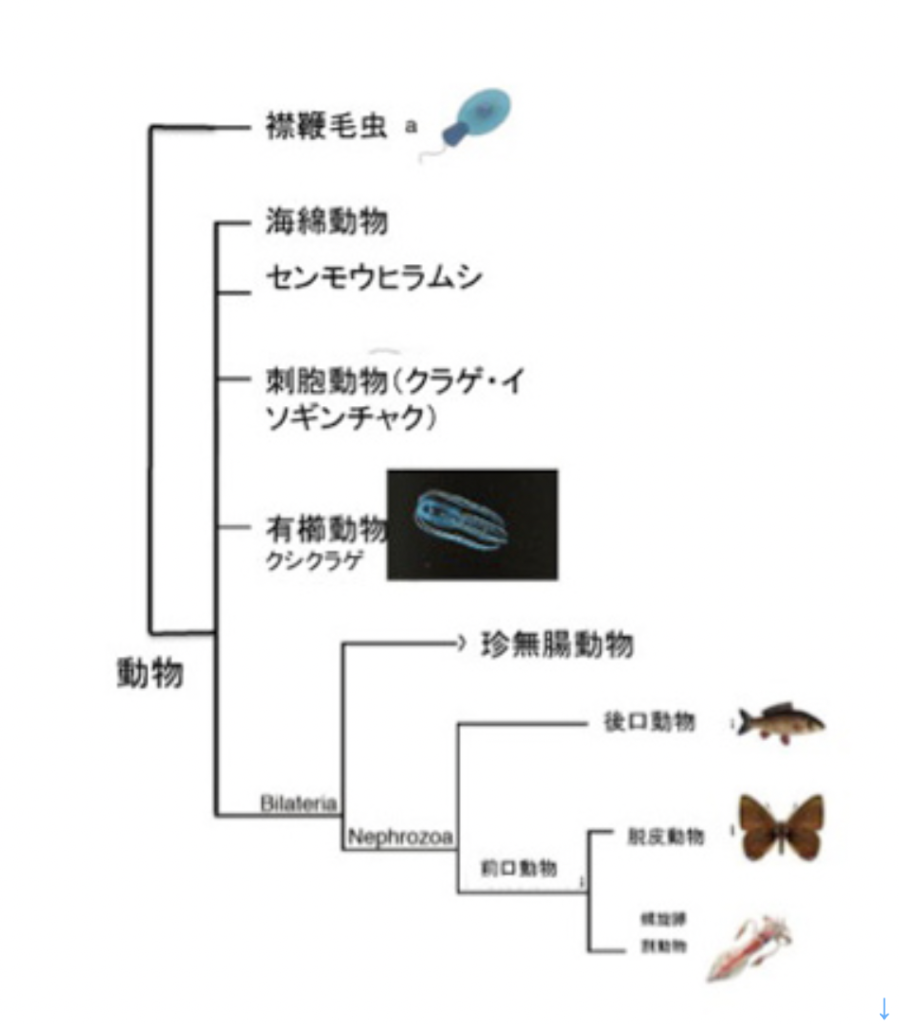
最初は神経細胞の誕生だ。現存の生物の系統樹から判断すると、神経細胞は動物、すなわち動く能力を持った多細胞生物の誕生とともに生まれてきたことは間違いない。図1に示した系統樹では現存の多細胞生物を5種類に大別しているが、海綿動物とセンモウヒラムシには、いわゆる神経細胞は存在しないことがわかっているが、残りの動物は全て神経細胞を持っている。
では神経細胞は動物が進化した後現れたのか?
海綿やヒラムシに最初から神経がなかったかどうかは議論が分かれている。というのも、図1のクシクラゲは、ゲノム系統樹から見ると他の4種の動物から最も早く分離した系統で、左右相称動物から見て系統上最も離れている。ところがこのクシクラゲに神経細胞が存在することから、より左右相称動物に近いヒラムシや海綿にも最初は神経細胞が存在し、その後神経細胞を退化させたと考える説もある。
これとは逆に、神経細胞と、他の興奮性の細胞とを区別する指標として用いられるナトリウムチャンネルは左右相称動物だけにしか見つからないことから、クシクラゲと他の動物が別れた後、クシクラゲと左右相称動物は独自に神経細胞を発生させたと考える説もある。
いずれにせよ、最初の神経は私たちが一般的に持っている軸索、細胞体、樹状突起からなる典型的な神経ではなく、外界からの刺激に反応し、その興奮を他の細胞に伝達する能力を備えていても、より普通の細胞に近い形態を持っていたのではないだろうか。実際、興奮性の細胞系列の一部は、興奮を力に変える筋肉細胞へと発展する。一方、様々な刺激を感知して、他の細胞に伝達する能力を持つ細胞から神経細胞が生まれたのだろう。細胞の興奮に必要なイオン勾配の維持機能、そのイオンを選択的に通過させ膜電位を発生させるイオンチャンネル、そして興奮を他の細胞へ伝える化学システムは動物の誕生前に進化し、採用を待つだけになっていた。
では、神経細胞が生まれることで何が可能になったのか、現存の生物で見てみよう。
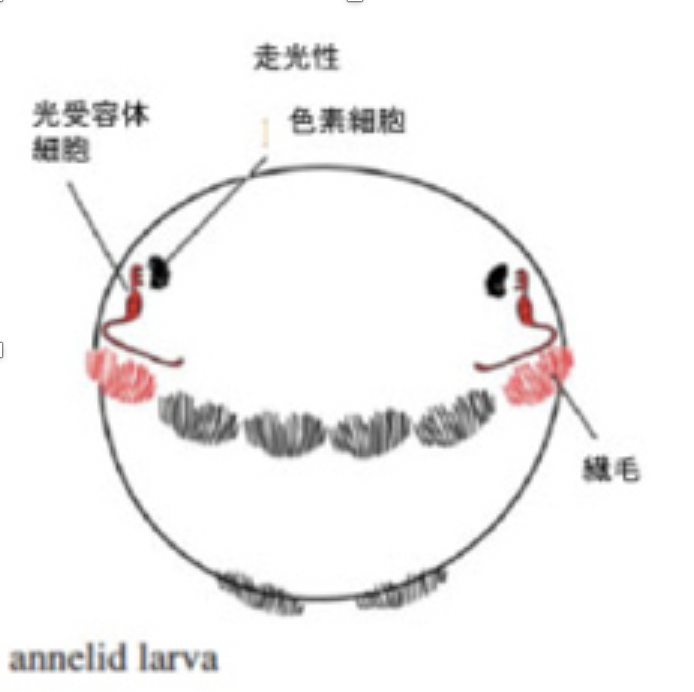
図2にゴカイの幼生の光受容体神経細胞について示すが、環形動物幼生の神経系は、まだ組織化されない単独の神経細胞が、どう神経細胞進化の初期に使われていたかを考えるいい材料になる(図2)。
図2:ゴカイ幼生の走化性
ゴカイの幼生は繊毛を使って水中を浮遊しているが、光を感じると繊毛運動を調整して光の方向へ移動する走光性を示す。これに関わるのが図2で示した3種類の細胞、色素細胞、神経細胞(光受容体細胞)、そして繊毛を持つ上皮細胞だ(original 論文はJekely et al,
Nature 456, 395, 2008)。図に示す様に色素細胞とそれに結合する神経細胞により色素細胞で吸収された光エネルギーが神経興奮として受容され、同じ神経細胞が繊毛上皮とコリン作動性のコンタクトを形成することで繊毛の動きを調節している。片方の目にだけ光を当てると、光を受けた方だけ繊毛の運動頻度が低下し、結果幼生は光の方に進む。
この研究から、神経細胞の出現により、外界の物理的刺激を感知して、他の細胞(近くの繊毛上皮細胞)にそれを伝達して、活性を変化させる一連の過程が可能になっているのがわかる。
光や温度、あるいは圧力などの物理変化に素早く対応することは、生物の生存にとって重要な条件だが、神経細胞出現後の素早い反応はフェロモンのような化学的シグナル分子だけでは実現できない。このため、光などの外界の物理的刺激に素早く反応するための分子メカニズムは動物誕生以前から存在していた。例えば、単細胞生物クラミドモナスの走化性に利用される光を感じて開くイオンチャンネル、チャンネルロドプシンはその典型で、この分子を使った光遺伝学は、脳研究を席巻する勢いだ。
このような様々な物理刺激を感知して素早く個体の行動を変化させるシステムは、高等動物への進化過程で神経系の属性へと集約していくが、ゴカイの幼生の走光性行動には様々なメカニズムが組み合わさっている。
動物の運動のほとんどは筋肉、あるいは筋上皮と呼ばれる筋肉と上皮の中間のような細胞により行われる。実際、ともに興奮性の細胞と言える神経と筋肉は動物の誕生とほぼ同時に出現している。一方繊毛による運動は例えばゾウリムシなどの繊毛虫から見られるシステムで、より古い起源の運動生成システムと言える。私たち人間も含め、繊毛運動が神経支配を受けることは珍しく、その方向性やパターンは上皮の持つ極性を含むplanar polarityと称される特性により決められている。ゴカイの幼生は、この古いplanar polarity様式と神経支配という新しい様式を組み合わせて運動を調節している面白い例だと言える。
神経細胞により繊毛運動の強弱を直接神経支配することは難しい。結局ゴカイの幼生で見られるように、繊毛を持つ上皮自体に働いて、その細胞の持つ繊毛の運動を全て止めるという方法をとらざるをえない。
またもともと繊毛は早い大きな動きには向いていない。このため動物では、神経とアクトミオシン収縮系を備えた筋肉とがセットで働く”運動”が優勢になっていく。この組み合わせにより、一つの神経シグナルを複数の筋肉細胞の収縮に使うことが可能になり、大きな力を発生させることができるようになった。
もちろん、神経支配による上皮の活性調節は、ホルモン分泌の神経支配などとして今も見ることができる。
以上繰り返しになるが、ゴカイの幼生で見られる神経細胞の役割は、1)物理刺激を感受して、2)それを素早く他の細胞に伝達し、3)個体全体を刺激に対応させる、ことに尽きる。また同じ系が収縮性の筋肉細胞と組み合わさると、繊毛運動をはるかに超える大きな運動が可能になる。
最後に、神経細胞誕生により生まれた新しい可能性を情報と進化の観点から考えてみよう。
高等動物の脳神経システムには、間違いなく新しい情報システムが存在しているが、神経細胞や筋肉細胞の誕生により、これにつながる新しい情報システムが誕生したとは言えない。例えばクオラムセンシングでのフェロモンの働きに見られるのと同じ、環境の変化を感受して決まったアクションを起こす、インプット・アウトプットの関係が、より複雑化しただけと言っていい。事実、ナトリウムチャンネルの出現といった、新しい分子の誕生によるメカニズムの多様化がこの過程で起こったものの、例えば脊椎動物進化で抗体分子が現れるといった、本当のイノベーションは起こっていない。
しかし、物理刺激を感知できるようになり多様な環境変化に対応できるようになったこと、素早い反応が可能になったこと、そして筋肉の誕生により大きな運動が可能になったことは、環境を自己に同化する進化の駆動力の観点から見ると、大きなイノベーションだったと思える。
環境を感知して自己を守る反応という点ではフェロモンと同じだが、素早く、方向性を持った動きが可能になると、好ましくない環境を回避することで生存する個体数は当然増える。さらに、筋肉が生まれると素早い大きな回避行動をより刺激に合わせてコントロールすることで、多様な生息環境を選ぶことができる。これは環境を作り直したのと同じことで、環境の自己や種への同化が起こっていると見ることができる。こうしてより適した環境に移動することで、当然選択圧は下がり、多様性を維持する方向に働く。
このように、フェロモンも、神経や筋肉も、ゲノム情報による自然選択をできるだけ回避する方向に働く。実際、生きている個体の適応性は、それ以前のゲノム多様化と、選択の結果だ。新しい現在の環境に適合するかは試されたことがない。これに対し、新しく生まれた情報システムは全て、今生きている個体の生存に関わる。このように、今という時間への適応を拡大することが、生物の多様化に貢献したと思う。神経や筋肉で言えば、運動性が質及び量の面で大きく高まることで、動物は急速に地球上の様々な環境へと拡大できた。すなわち、過去の進化で獲得された環境適合性に合うよう個体が環境を選び、場合によっては改変することで、選択をかわしてゲノムをさらに多様化できたと思う。
新しい情報誕生まではまだまだだが、神経細胞の誕生はさらに新しい展開を見せる。次は記憶の誕生について見ていく。
[
西川 伸一 ]
神経記憶 I
2016年11月15日
今回から記憶について考える。
記憶自体は情報ではない、しかし、皆さんのパソコンでの情報処理に記憶素子が欠かせないように、情報が成立するために欠かすことができない機能だ。情報を論じるために記憶の問題を避けて通れないことを理解してもらうため、これまで見てきた情報を、記憶という観点から見直すところから始める。
通常「記憶」という言葉は、経験によって脳内に誘導された神経活動パターンを、時間を経た後で呼び起こすことを意味する言葉として使っている。この神経記憶については後に考えるとして、この言葉が私たちの神的活動にとどまらず、あるパターンを繰り返し呼び起こす現象を表現するのに使われていることを思い出して欲しい。例えば、形状記憶合金というと、形が壊れてもまた自然に同じ形を取り戻すことができる合金を意味している。
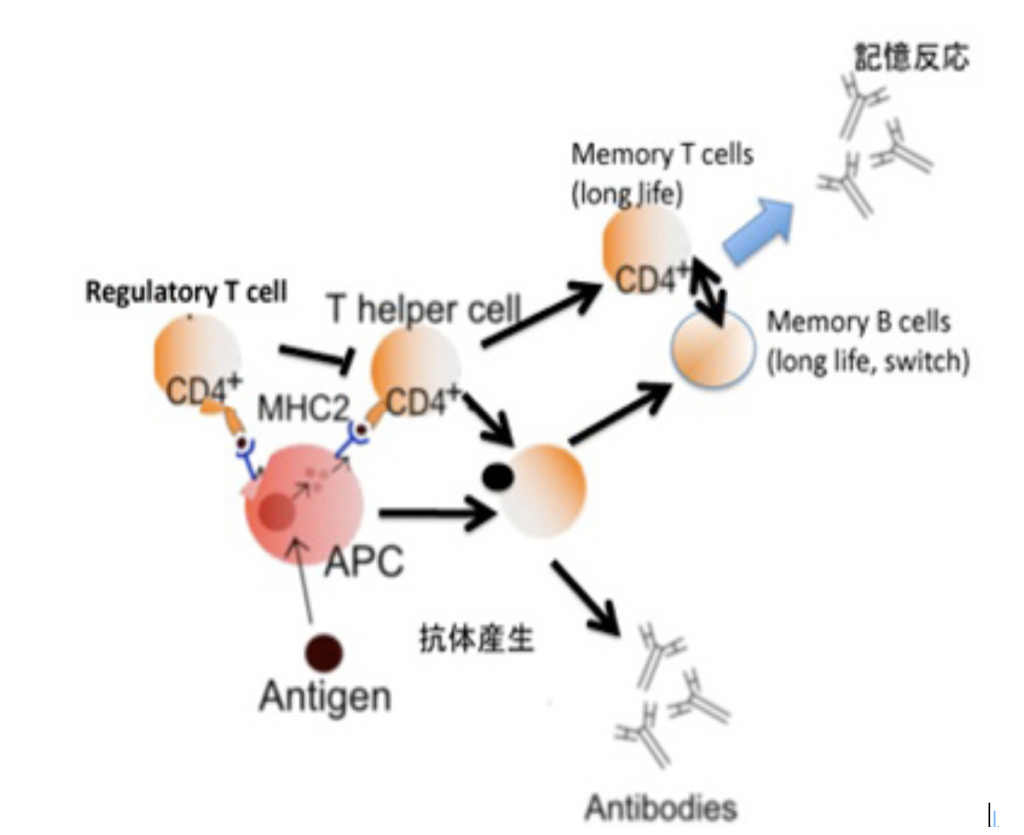
生物学でも記憶という言葉が使われる現象は多い。例えば免疫記憶は、一度経験した抗原に対して免疫系が最初よりより速やかに、しかもより強い反応を起こす過程と定義できる。免疫記憶の背景には、かなり複雑な細胞間相互作用が存在するが、極めて単純化して説明すると、経験した抗原に反応するリンパ球が選択的に増加する、あるいは寿命が長くなることにより記憶が形成される。すなわち、経験を、この抗原特異的リンパ球の数や活性の変化に変換して記録している。
このように何らかの形で一定のパターンを記録することを記憶と考えると、生物にとって最も根源的な記録を担うDNAも一種の記憶と呼ぶことができる。実際、ゲノムは、ゲノム自身の複製だけでなく、それを持つ生物の複製も可能にしている。そして、複製とは同じパターンが繰り返すことに他ならない。もし、コンピュータのメモリーのように記憶=記録情報だとすると、ゲノムをメモリーと呼んでよさそうに思える。
しかし、塩基配列としてゲノムに書かれている情報を決して記憶と呼ぶことはできない。なぜなら、ゲノム複製も、細胞複製も、ゲノム情報だけでは実現できず、ゲノムの情報に基づいてオペレーションを行うための様々な条件が揃って初めて可能になる。以前、マイコプラズマの再構成実験を例に(http://www.brh.co.jp/communication/shinka/2016/post_000013.html )この問題について議論したが、今の所ゲノムは生きている生物にしか移植できない。同じことは、発生初期の受精卵では胚自体のゲノムからの転写がほとんどないことからもわかる。個体の一生を通じてあらゆる細胞で働くことができるゲノムも、まず母親から受け継いだRNAから作られた分子による発生のプログラムが活性化されて初めて、その個体の情報として働き始める。
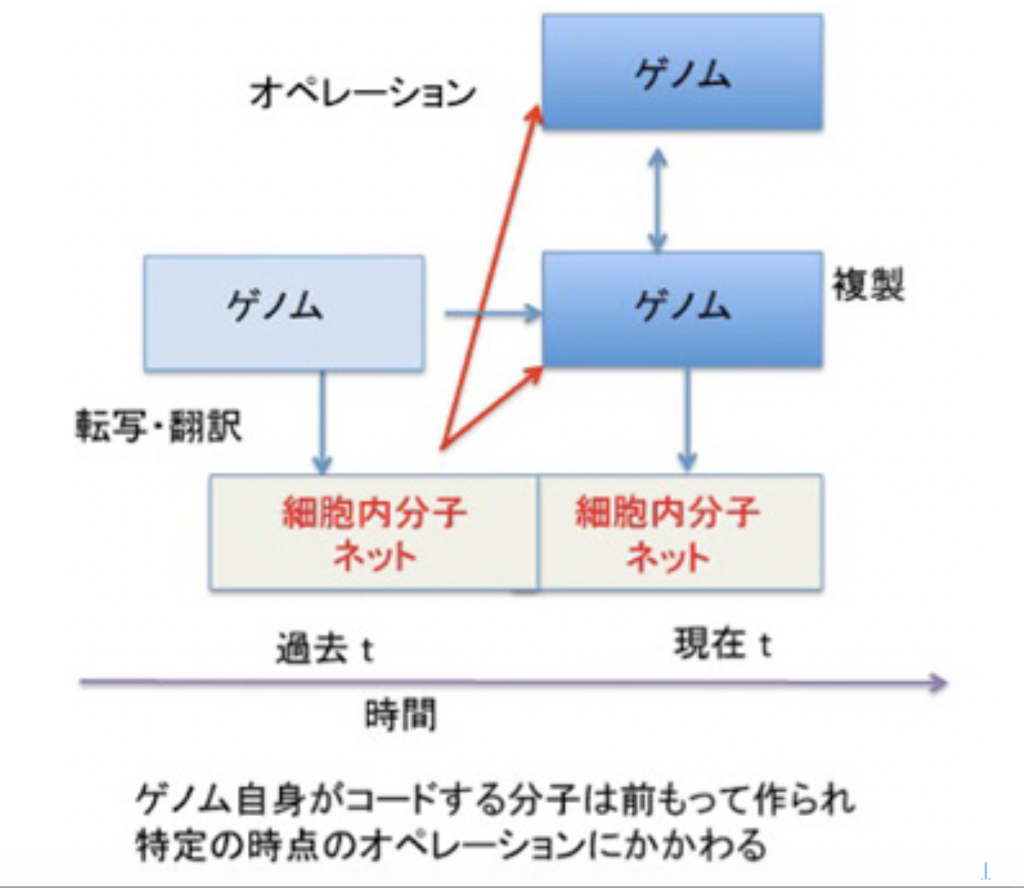
このように、記憶は記録された情報ではなく、体験、記録、呼び起しという順序で進む一連の過程全体に他ならない。例えば、図1に示すように、ゲノムは情報として二つの役割を担っている。
一つは自分を複製するための情報と、複製のための鋳型としての役目だ。ただ、ある特定の時点(図1:現在 t)のゲノムのオペレーションは、同じゲノムによりその時点より前に作られた(過去 t)分子ネットワークによりオペレートされている。生命特有の鶏が先か、卵が先かという問題がここでも現れる。いくら外来遺伝子を細胞の中で機能させられるからといって、ゲノムとそのオペレーションは互いに分離不可能で、ゲノム=記録として切り離すことはできない。
ではなぜ今使っているコンピュータでは、アプリケーションや記録をメモリーに記録して分離することができるのか。これは、コンピュータ自体が一定の命令で動くように人間により作られているからというしかない。生命に、コンピュータにとっての人間のように、明確なデザインの出し手は存在しない。
ゲノムのオペレーションがそれ以前に準備された分子ネットワークに依存しているとすると、ゲノムのオペレーションに関わる分子ネットワークを辿れば、結局最初の生命誕生時にゲノムをオペレーションした分子ネットワークに行き着く。すなわち、ゲノムが38億年前に誕生した最初のゲノムまで連続しているのと同じで、細胞内の分子ネットワークも途切れることなく過去から現在そして未来と、ゲノムとともに受け継がれる。このように、現存の生物の記憶には無限の過去の経験が持ち込まれていることになる。こう考えると、進化自体DNAを記録媒体とした記憶と考えることができる。言いかえよう。ゲノムを記憶という観点から考えると、必然的に38億年という全進化史が含まれる壮大な過程と見ることができる。どの体験がゲノムに記憶され現存の種に維持されているのかを研究するは、進化学に他ならない。
一方、クロマチン情報は、基本的には各生物の一生という時間枠の中での記憶と言える。この意味で、神経記憶と同じだが、クロマチン情報が記憶と定義することに抵抗を感じる人も多いだろう。ただ思い出して欲しい。生物発生では、卵から個体誕生まで、ほぼ同じ過程が概ね正確に繰り返される。この過程では、ゲノムは変化せず、時間、場所に応じてクロマチン情報が変化していく。例えば発生学でよく研究される両生類の初期発生を例に見てみると、どの場所に精子が入るかは偶然の結果だが、侵入点が決まると体の大まかな体制が決まるよう、すでに卵細胞のゲノム、クロマチン情報、分子ネットワークが準備されている。
核移植クローン実験から明らかになったように、卵細胞質の分子ネットワークの多能性プログラムを維持する能力は高い。しかし、この分子ネットワークは卵割に伴い内外から新しい刺激を受けて分子ネットワークを変化させると共に、次々と生まれてくる細胞のクロマチン情報を変化させて、分化可能性が制限された分化細胞を形成する。一旦分化細胞のクロマチン情報が確立すると、分化した細胞の性質は安定に維持される。
クローニングやiPSにより示されたように、分化した細胞のクロマチン情報による分化制限を元に戻すことはできないわけではないが、普通はこの制限のおかげで、安定に同じ運命の細胞を作ることができる。こうしてそれぞれの細胞でクロマチン情報を中心に新しい記憶システムが成立する。
このクロマチン情報を中心とする記憶システムは、プログラム前の分子ネットワークと、外から入ってくる新たなシグナルにより少しづつ変化するが、このオペレーションメカニズムについては研究が始まったばかりでわかっていないことが多い。ただ最近、比較的少数の細胞でゲノム全体をカバーするクロマチン情報を調べる手法が開発されているので、急速な研究発展が期待できる。
ゲノム、クロマチン情報、分子ネットワーク、外界からの刺激などを記憶の観点から見た関係を図2に示す。ここでは、ヒストン修復と、DNAのメチル化の制御によりクロマチン情報が書き込まれることで、特定の細胞を繰り返し作るための長期記憶が形成される。この記憶=クロマチン構造の維持と変更システム、により制限を受けた転写により生まれる分子ネットワークが、分化した細胞のオペレーションの基盤になる。各細胞の分子ネットワークは内外からの(周りの細胞も含む)様々な刺激により変化する。この変化は、一種の短期記憶と見ることができるが、クロマチン情報の制限を外せない限り、長期記憶にはなりえない。ところがある特定の刺激が分子ネットワーク内に揃うと、ヒストン修飾やDNAメチル化の変化による、クロマチン情報の書き換えが起こる。これにより、細胞の分子ネットワークの変化として短期的に維持されていた記憶が、より長い期間維持される長期記憶に変化する。
ある特定の細胞のクロマチン情報の書き換えを可能にする分子ネットワークの変化について研究しているのが、リプログラム研究で、山中4因子の発見に端を発して、様々なリプログラミング、すなわちクロマチン情報書き換えのための条件が明らかになりつつある。
神経記憶から脱線したが、図1、2に示した記憶システムは、真核生物のあらゆる細胞で見られる。従って、神経細胞記憶もこの2つの記憶システムの上に発展したといえるが、これまでの記憶システムとは大きく違っている点がある。すなわち神経記憶は、動物の誕生とともに新しく生まれた興奮性の神経細胞同士の結合により(ここでは、神経細胞を、同じ前駆細胞から生まれるニューロン、アストロサイト、オリゴデンドロサイトを全て含む広い定義を用いる)新たな記憶システムを成立させている点だ。
この新たな神経記憶の特徴については次回から考えるが、最後に神経記憶もクロマチン情報を中心とする記憶システムの上に構築されていることを、前回に例として使ったゴカイの幼虫の神経系をモデルに見ておく。このモデルを選んだのは、これが一本の神経細胞だけで形成されている最も単純な神経系で、なおかつ神経細胞の基本的特徴を備えているからだ。そこで、ちょっと想像をたくましくして、この系での記憶について考えてみた。もちろんこれから述べることは証拠があるわけではなく、神経記憶自体は回路形成なしでも考えられることを知ってもらうために考えたたとえ話だ。
さて前回述べたように、ゴカイ幼虫には、光をトラップする色素細胞と協調して光に反応し、その興奮を繊毛細胞に伝え、繊毛の動きを止める神経細胞がある(前回図2、および今回図3)。この神経は感覚神経と運動神経の両方の役割を持つため、神経回路は形成しない。
この系では神経細胞が感覚刺激を感受すると、チャンネルが開き細胞が興奮、その興奮によりアセチルコリンが遊離、繊毛細胞に働いて繊毛の動きを止める。これは一般的神経細胞の興奮と同じで、分子ネットワークに大きな変化はない。ただ、この状況でも光刺激が繰り返すとアセチルコリンが枯渇する。このため新たな合成が始まるまで、幼生の運動は停止する。この結果、幼生はストップ・アンド・ゴーを一定のサイクルで繰り返す。
この時、光シグナルの強さによりもしクロマチン情報が変化し、アセチルコリンの合成速度が完全に変化したとすると、ストップ・アンド・ゴーの感覚を長期的に長くしたり、短くしたりすることができる。即ち、刺激による長期記憶が誕生したことになる。
繰り返すが、これは理論的可能性を述べただけで、実際にどうかはまったく知らないが、神経内の分子ネットワークとクロマチン情報を変化させることで、回路形成なしに神経記憶を形成することができることを理解してもらえたと思う。
この図1,2の記憶システムの基盤の上に新たに回路形成が加わったのが神経記憶で、次回はこの回路形成が加わったことによって生まれる新しい可能性について見ていく。
[
西川 伸一 ]
神経記憶 II
2016年12月1日
前回まで、ゲノム情報を中核とする記憶(Geneme mediated memory:GMと呼ぶ)、クロマチン情報を中核とする記憶(Chromatin mediated memory: CMと呼ぶ)について考えを述べてきた。GMは生命進化全体、CMは生物個体の発生から死までの時間をカバーする記憶システムと言える。
生物学は現象を生物の側から説明しようとして目的論に陥ることが多いが、それを承知で言うと、GMもCMも、過去の経験を記憶し、未来に備えるシステムと言える。
前回 見たように、GM、CMそれぞれの記憶システムは階層的に重なって統合されており (前回:図2)、CMはGMを基礎としてその上に形成される。この構造はCMを有する全ての真核細胞で共通で、当然神経細胞も他の細胞と同じように、GM,CMを持っている。このおかげで単一の神経細胞だけでもCMを利用して神経記憶反応を起こせる可能性を前回示した。他の細胞と比べると、神経細胞は刺激に対して早い反応(興奮)を起こすことができるため、神経記憶に見えるが、記憶自体は神経特有というよりCMの機能を反映している。
このGM、CM記憶の上に新たに生まれたのが、神経細胞同士の結合した神経回路形を中心にした記憶(neuron mediated memory:NM)で、これにより動物は、質的、量的に一段高い次元の記憶システムを獲得し、今や地球上に100億個体も存在するという驚くべき繁栄を遂げた人間を進化させる大きな原動力となった。
GM,CMでは、ゲノム情報やクロマチン情報のように分子レベルの媒体が経験の記録を担っているが、NMは細胞間に形成される回路のように細胞レベルの媒体を利用する記憶と言える。神経細胞の特徴は、細胞同士で刺激や抑制の回路を形成できることで、この回路が経験の記録の単位になる。もちろん細胞間のネットワーク形成が見られるのは神経だけではない。例えば、免疫細胞記憶成立には、神経伝達と同じように、サイトカインと呼ばれる分子による、シグナル伝達機構が存在する。また、一つの免疫反応に関わる細胞の種類は、マクロファージや樹状細胞から、何種類かのT細胞、場合によってはB細胞と、神経系と同じように数が多い。しかし、免疫系が神経系と大きく異なる点は、抗原と、それに対する抗原受容体の間の特異的分子結合がネットワークの中心にある点だ。さらに、抗原が常に存在しないと、記憶も維持できないし、反応も起こらない。さらに、抗原刺激とそれを中心にする細胞間相互作用により、それぞれの細胞の増殖や寿命の延長などがおこるため、結果細胞の動態に大きな変化がおこる。
一方、神経細胞回路の場合、匂いや味の感覚のように、外来の化学物質により刺激誘導される場合でも、興奮が神経間で伝達されるときには、最初の興奮を誘導した物質は必要なくなっていることが多い。すなわち、感覚器の興奮が伝えられるとき、感覚を誘導した刺激は必要ない。もちろん刺激の持続時間が短い光などの物理的刺激は、最初から刺激の持続を前提に感覚を伝えることはできない。記憶が維持されるためにも、最初の刺激は必要ない。このように、神経記憶は刺激物質を中心に反応が構成されるのではなく、最初から感覚刺激を複数の神経細胞興奮のパターンへと転換された後、伝達され、記憶される。
どうして最初の刺激を誘導する物質とは全く無関係に、神経回路だけで、記憶が成立、保持できるのかを考えるのが、これからの問題で、詳しく見ていきたいと思う。ただ、神経科学についての私の知識は乏しい。このためこれから書く内容には、間違った記述が含まれる可能性があることを断っておく。
まず、神経細胞回路がどのように記憶に関わることができるか見ていこう。
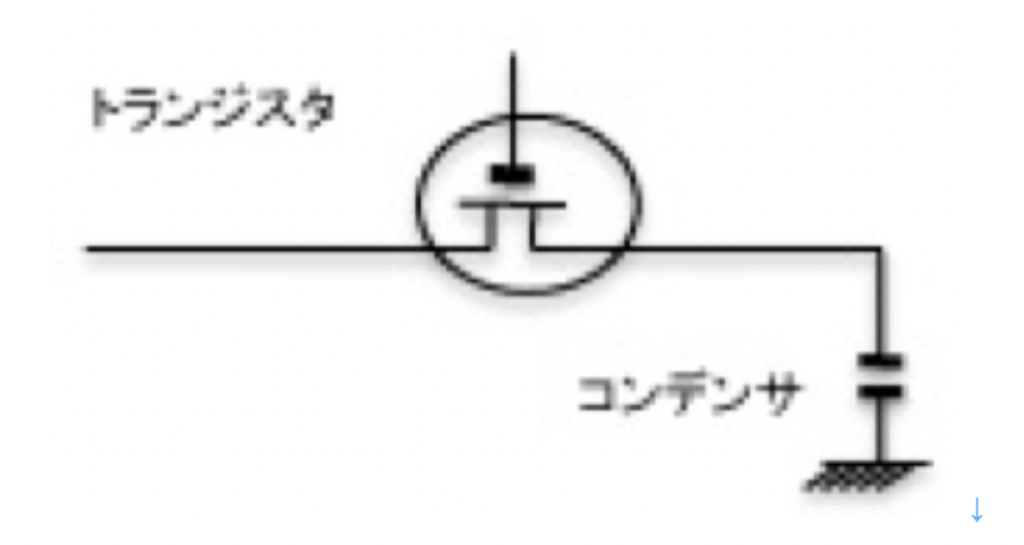
まず個々の神経細胞をみると、一つの記憶素子として機能できることがわかる。図1に最も単純な電気的記憶素子DRAMを示すが、一個の神経細胞はDRAMに似ていると言える。図に示すようにDRAMは基本的にはスウィッチ役のトランジスタとコンデンサからできており、コンデンサーに電気を貯めることで1 or 0のデジタル記憶が可能だ。
すなわち、スウィッチがオンになって電気がつながれば、コンデンサに電気が溜まった状態になる。一方、スウィッチがオフになると、コンデンサは自然放電して溜まった電気はなくなる。この溜まった電気があるときとないときで、2進法の1か0を記憶できる。
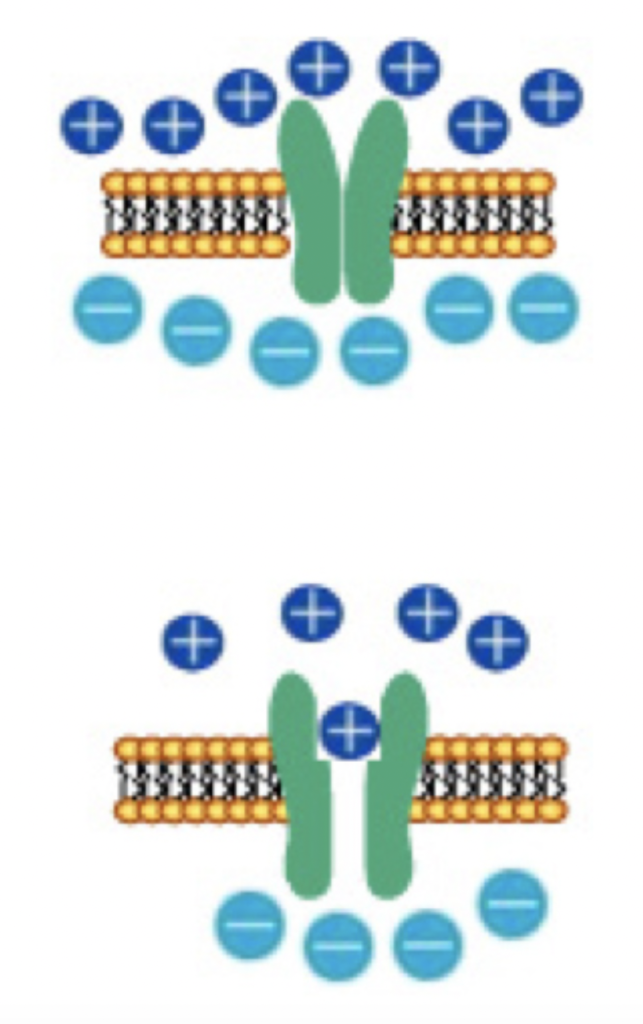
一方、神経細胞はイオンポンプを用いて外界と細胞内の様々なイオン勾配を保つことで、電圧を維持している。細胞膜には特定のイオン分子(例えばNaやK)を選択的に通過させるイオンチャンネルが存在し、刺激によりイオンチャンネルが開くと、特定のイオンだけを勾配に従って流すことができる。すなわち、イオンチャンネルはDRAMでのスウィッチの働きと、イオンチャンネルの特性に応じた一種の抵抗が合わさった素子と考えることができる。
ポンプを使って電位を維持する限り、細胞は自分で発電し、細胞膜という電気を貯めるコンデンサとスウィッチとしてのチャンネルを持つことから、DRAMとよく似た構造をとっているのがわかる。神経細胞の場合、電位はチャンネルが閉じている限り電気維持されるが、チャンネルが開くと外界との勾配はどんどん消えていく。このように原理的には一個の神経が一つの記憶素子として働く可能性を持っているが、実際にDRAMのような使われ方をしているのかどうかについては私にもよくわからない。また、ポンプとチャンネルを備えている細胞は、神経細胞に限らず数多く存在する。したがって、このDRAMに似た構造だけが記憶に大事だとは言えないだろう。
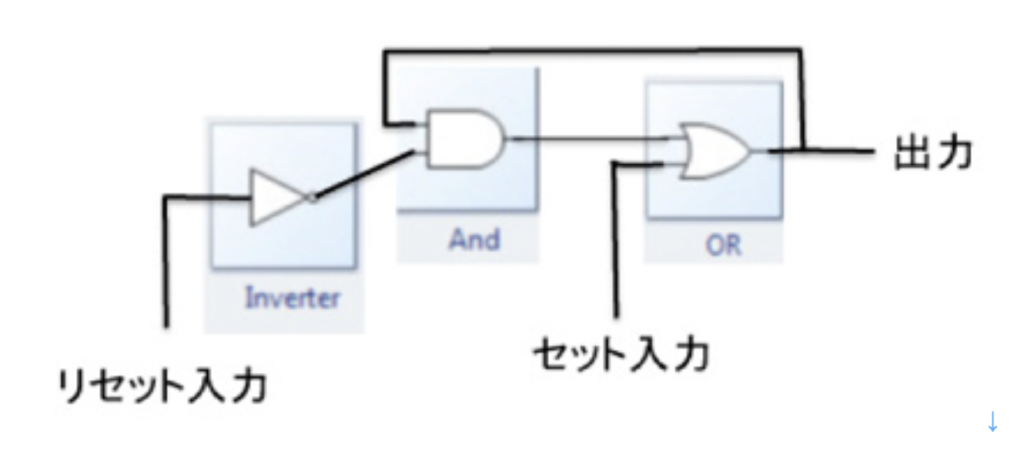
神経細胞自体を記憶素子として使わずとも、神経細胞を組み合わせて回路を形成させ記憶させることも可能だ。エレクトロニクスでは様々な記憶回路がDRAMのような記憶素子の代わりに使われている。もっとも単純なものは図4に示すラッチ回路と呼ばれるもので、インバーター、ANDとORの演算素子を結合させた後、ANDからの出力に応じてフィードバックさせること回路で、0と1を記憶させることができる。
電気回路の講義のつもりはないので、ANDやOR といった選択が行われる素子を繋ぎ合わせれば、それ自体で記憶が可能になると考えて貰えばいい。
しかし同じような回路形成を細胞で実現しようとすると、神経のように特殊な形態と機能を持つ細胞が必要になる。いくら興奮性があっても、筋肉細胞ではこのような回路形成は不可能だ。この回路形成が可能であるという点を念頭に神経細胞の特徴を述べたのが、細胞レベルでの脳研究の始祖、ラモンカハールのニューロン4原則だ。
カハールのニューロン4原則
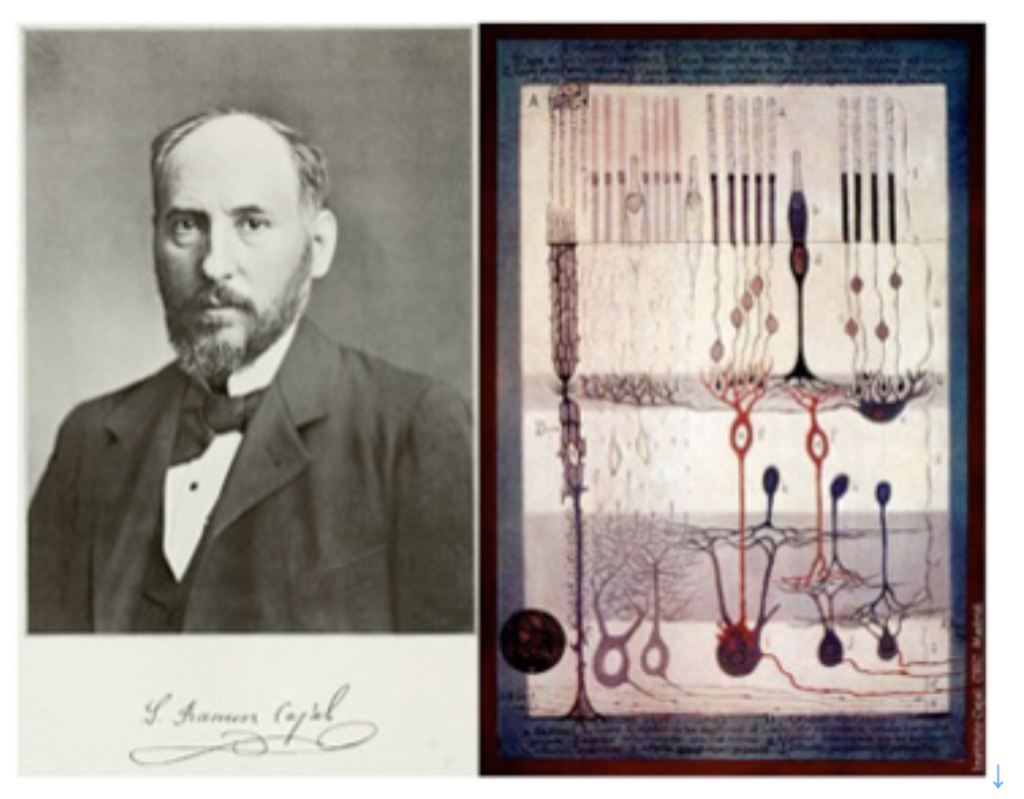
1)第一原則:ニューロンは脳の基本構成成分であり、シグナル伝達単位である。 2)神経は軸索と樹状突起に存在する特殊な部分を通してのみ相互作用を行う。 3)この特殊部位(シナプス)を介する一つの神経細胞の結合は、特定の神経細胞同士に限定されている。(結合の特異性) 4)シグナルは常に一方向のみに伝わる。(シグナルの方向性) この原理は1890年に書かれたものだが、なぜ神経だけが、演算回路や記憶回路を形成できるのかの原理について見事に説明できている。このことは、図5に示したカハールの網膜神経組織の模式図からよく理解することができる。https://en.wikipedia.org/wiki/Santiago_Ram%C3%B3n_y_Cajal )
すなわち、それぞれの神経細胞は、軸索や樹状突起の神経接合部のみで、しかも決まった神経細胞とだけ結合している。そして、感覚細胞からいくつもの神経を経て脳へとシグナルが一方向へ伝わっていることもよく描かれている。まさに、神経細胞は回路形成のために誕生した。
次は神経細胞が形成する記憶回路について、記憶の研究でノーベル賞に輝いたエリック・カンデルの研究を追いながら見てみよう。
[
西川 伸一 ]
神経記憶 III
2016年12月15日
神経科学の歴史について詳しいわけではないが、記憶を始めすべての脳機能が神経細胞(ニューロン)同士の結合した回路により担われていることを最初に示唆したのはスペインの生んだ巨人ラモン・カハールだろう。前回 述べたように(前回図5)、カハールはゴルジ染色法を用いて、一個一個の神経細胞を染め出し、脳が様々な神経細胞のネットワークであることを明らかにし、カハールの4原則を提案した。このことから、カハールを神経細胞ドクトリン(ニューロン説)の最初の提唱者と呼んでいいだろう。実際この4原則に適合するネットワークを形成できる細胞は神経細胞以外にない。
カハールのニューロン4原則に加えて、神経回路を考える時に重要なドクトリンをあと二つ挙げておこう。
一つはすでに前回紹介したが、神経細胞は共通のメカニズムで、細胞膜上で起こる電気的興奮を伝搬することができる点だ。静止状態では、神経細胞内外のナトリウムイオン(Na+ )勾配によって、神経細胞内外の電位差(静止膜電位)は-90mVに保たれている。外的な刺激でこの電位が変化してある閾値を超えると、イオンチャネル(電位に応じて開閉するNaチャネル)が急速に開き、結果急速にNa+ が細胞内に流れ込み、膜電位の極性が変わる(+20mV:脱分極)。この電位の変化は、イオンチャンネルを介してK+ を細胞外へ逃すことですぐに元に戻るが、刺激が繰り返されるとイオン勾配が消失して、興奮できなくなる(不応期)。このイオン勾配を復元するためには、それぞれのイオンに特異的なポンプが働く必要がある。このイオンドクトリンに従う細胞であれば、いかに複雑な形態をもち、神経間の興奮伝達に様々な化学物質が使われる場合も、神経を点から点に張り巡らせた電線と同じように単純化して考えることができるようになった。
最後のドクトリンが、神経細胞間の興奮伝達がシナプス接合部での化学物質の伝達によって誘導されるとするシナプスドクトリンだ。すなわち、化学物質の伝達によって、それを受け取る側の神経細胞の興奮を誘導できるが、この場合は電位依存性チャネル(voltage gated channel)ではなく、シナプスで興奮した細胞から分泌される伝達物質と結合することで開くチャネルにより、もう片方の細胞に興奮が伝わることがわかっている。シナプスドクトリンは、神経興奮伝達が一方向にのみ進むというカハールの原理を説明するだけでなく、使われる化学物質を変化させることで、神経間の結合に特異性を与え、また次の神経の興奮に対して促進的にも抑制的にも働けることが説明できる。この二つの性質を合わせると、ほとんど無限の神経回路を作れることが直感的にわかると思う。
この3つのドクトリンを基盤にして、神経回路による記憶維持の細胞学的、生化学的メカニズムについての研究が始まったが、この問題を分子レベルまで掘り下げて説明するのに成功したのがコロンビア大学のエリック・カンデルで、彼はこの研究によりノーベル医学生理学賞に輝いている。
カンデルが記憶回路の解明に用いた動物はアメフラシ(図1)で、大きな殻のないカタツムリと考えて貰えばいいだろう。
http://en.wiktionary.org/wiki/File:Aplysia_dactylomela_2.jpg )
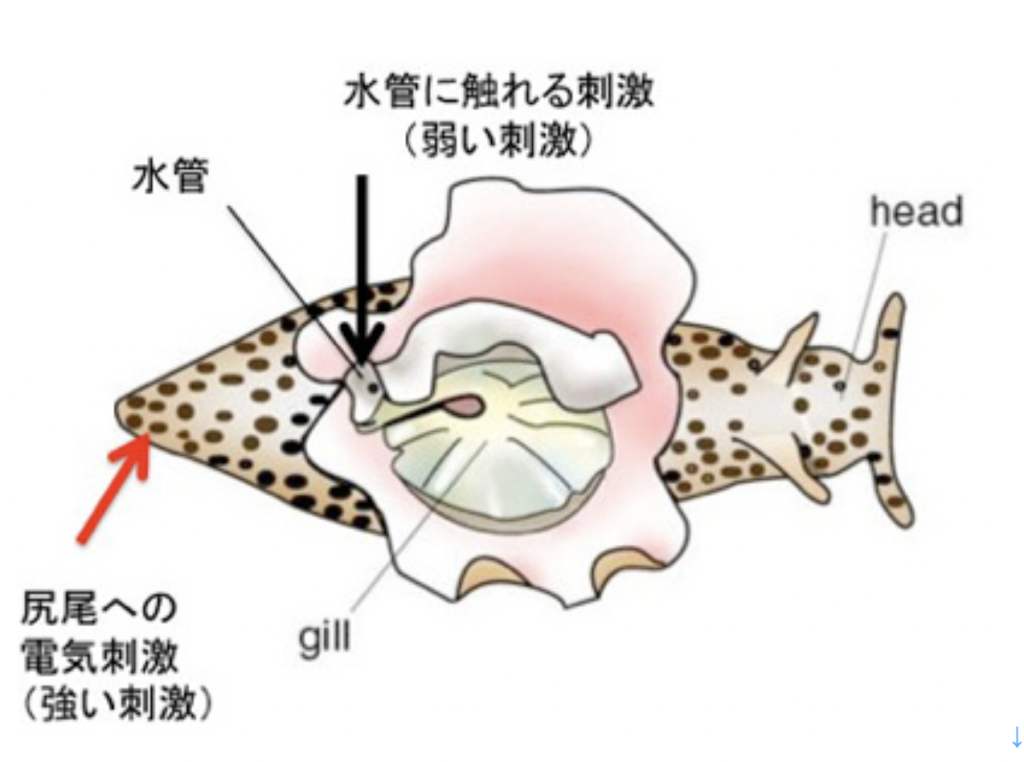
カンデルは、図2に示した、アメフラシの水管(水を吐き出す管)を刺激すると、エラを引っ込めるという反射に注目した。図2は2000年カンデルがノーベル賞を受賞した時のプレスリリースに掲載されたアメフラシの図だが、腹側にエラと水管が存在している様子がわかる。カンデルたちは、エラを引っ込める反応をアウトプット、水管を触れる刺激、および尻尾への強い電気刺激をインプットとして、それぞれの刺激間の関係や、刺激のパターンが記憶されるかについて調べた。
例えば水管を刺激し続けると、アメフラシは刺激に慣れてエラ反射を起こさなくなる(Habituation)。あるいは、水管に触れる前に尻尾に強い刺激を与えると、水管を触れた時のエラの反応が増幅する(Sensitization)。このサイフォン刺激や尻尾への強い刺激が記憶されているかどうかは、一定のインターバルをおいて、同じ刺激を加え、エラが同じ反応を示すかどうか調べることで確認出来る。このインターバルが短い時の記憶が短期記憶で、長い時の記憶が長期記憶になる。カンデルたちは特にSensitization(感作)と呼ばれる行動を用いて短期記憶、長期記憶について研究を行った。
もちろん短期記憶、長期記憶が存在することは、様々な神経システムで観察することができる。しかし、記憶に関わる神経回路を、一個一個の細胞レベルまで分離することは簡単でない。しかしアメフラシの回路では、神経が大きく、また数が少ないため、エラを引っ込める行動とともに、それに関わる単一の神経細胞の興奮を長期間記録し続けることができる。また、刺激後何日もたって、再度同じ神経を探し出して記録することも可能だ。記憶のメカニズムを、行動、神経生理学、そして細胞内での生化学的反応へと還元したいと考えていたカンデルにとっては、アメフラシは選びに選んだモデル動物だった。
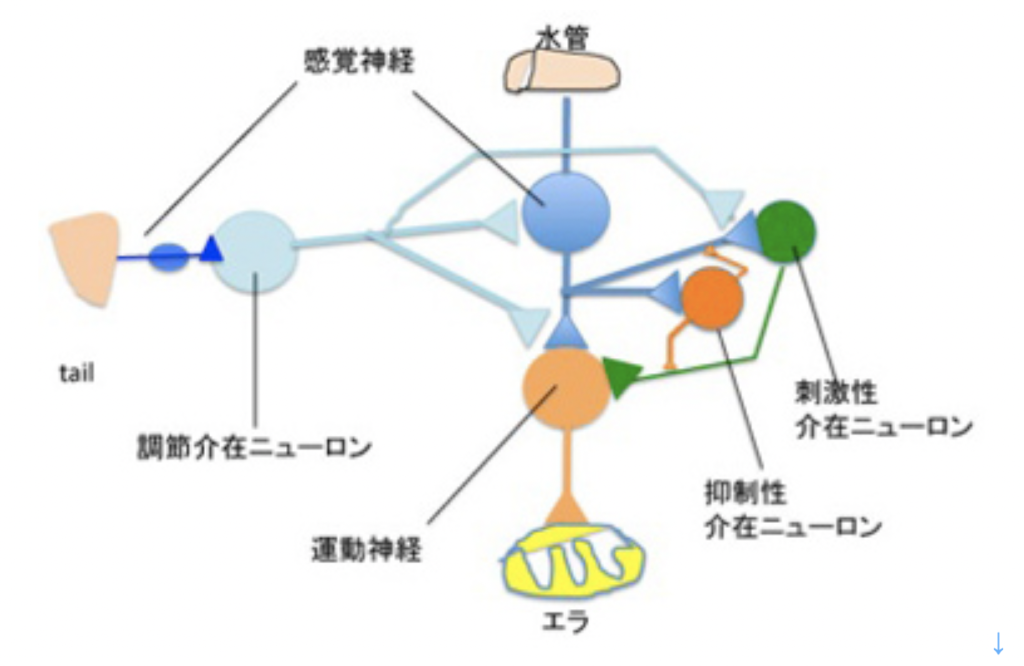
図3はカンデルたちが分離した、水管反射の記憶に関わる神経回路の模式図だ。水管への刺激を感じる感覚神経と、エラを引っ込める運動神経がシナプス結合を形成しており、これがメイン回路になる。そこに、水管の刺激をフィードバックしたり、フィードフォワードする刺激性介在ニューロン、抑制性介在ニューロンが結合してサーキットが形成される。このサーキットに、尻尾の感覚神経と結合する調節介在ニューロンが結合して、体の他の部分の感覚を伝えるまさに回路が形成されている。
それぞれの神経は、単一細胞レベルで興奮を記録するとともに、物質を注入することができる。これにより、行動を神経生理学、そして最終的に神経内部での分子間相互作用へと還元することが可能になった。
カンデルたちの期待通り、現在ではSensitizationについての短期記憶、長期記憶のメカニズムはほぼ明らかになったと言える。両記憶のメカニズムについて、同じくノーベル財団のプレスリリースで使われた図を用いて説明しよう。
結論的には、「短期記憶も、長期記憶も、アウトプットとしてシナプス伝達の強さや閾値を変化させる細胞内の変化」とまとめることができる。
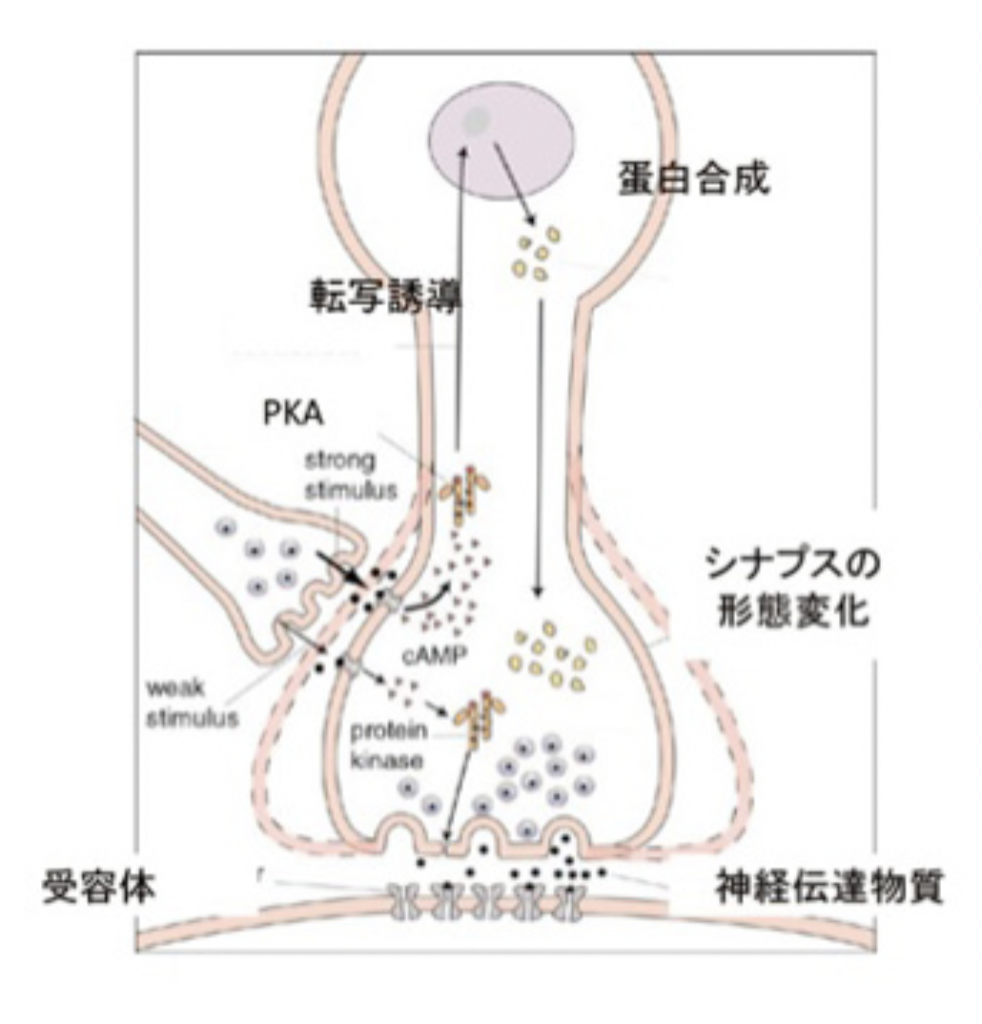
まず短期記憶から見てみよう。尻尾からの調節性介在ニューロンは、水管の刺激を感じる感覚神経と運動神経とを結合しているシナプスに結合している(図3)。この介在ニューロンが興奮すると、1)セロトニンを分泌し、2)このセロトニンがシナプス上の受容体に結合すると、3)アデニルシクラーゼが活性化し、4)cAMPが作られ、5)cAMPにより細胞内のタンパク質リン酸化酵素PKAが活性化され、6)カリウムチャンネルや様々なシグナル分子をリン酸化して、7)より多くの神経伝達物質を分泌するシナプスに変化する、という順序で運動神経への刺激が増強する。ただ、この増強は一過的なPKAリン酸化活性の増強によるもので、時間が経てば元に戻る。
これに対して長期記憶は、同じように活性化されたPKAが一過的にシナプス機能に関わる様々な分子を活性化するだけでなく、図4にあるように転写因子を活性化し、誘導された新しい分子により細胞の分化が誘導されることで、長期にわたるシナプスの大きさ数の変化が起こることで維持されることがわかった。実際には、セロトニン刺激がPKAを活性化するところまでは短期記憶と同じだが、長期記憶の場合はその後CREB1と呼ばれる転写因子が活性化され、新たな遺伝子を誘導することで、細胞自体が分化し、細胞及び組織レベルの構造変化が起こることで長く続く記憶が成立する。言い換えると、細胞をプログラムし直し、違った性質に変化させることが長期記憶のメカニズムだ。この仮説は、感覚神経へCREB1を過剰発現させることで、刺激なしでも長期記憶が成立するという実験による証明された。
実際にはこの単純な回路では、さらに複雑な短期、長期の細胞変化が起こり、シグナルのインプットとアウトプットの関係をさらに複雑にできることがすでに明らかにされているが、その詳細は省いていいだろう。
アメフラシの神経回路を用いた短期、長期記憶については以下のようにまとめることができる。
1)記憶は、複数の神経がシナプスで結合した神経回路を基盤に成立する。 2)シナプスから分泌される神経伝達因子は、細胞の興奮だけでなく、細胞内のシグナル伝達経路を刺激する。 3)このシグナルにより、一過性に細胞内の様々な分子が活性化、あるいは不活化され、その結果シナプス興奮の閾値や大きさが変化し、刺激に合わせた反応を誘導できる。これが短期記憶。 4)同じシグナルは、特定の転写因子を活性化し、新しい遺伝子発現を誘導する。これにより、細胞のプログラムが変化し、細胞分化や構造変化が起こる。一旦プログラムが書き換えられると容易に元に戻らないため、長期にシナプスの活性を変化させることができる。これが長期記憶。 以上のことから、長期記憶も、短期記憶も、特に特別なメカニズムを使っているわけではなく、多くの細胞と共通の分子を利用していることがわかる。PKAは多くの細胞でcAMP濃度上昇を感知し、短期・長期の細胞変化を誘導するのに働いている。CREB1についても同じだ。ただ神経の場合、刺激により誘導される最終結果が神経細胞同士の神経伝達の強度や閾値の変化になる。またこの変化も、一過性から、様々な長さの時間持続させることが可能だ。
次に、図3からわかるように、神経同士の結合はほぼ無限に複雑化することができる。しかも、神経細胞は形態的にも機能的にも何十種類も存在するため、回路の複雑性はすぐ天文学的になりうる。そして、神経伝達物質や受容体も数十種類存在するため、これによって可能なシナプスを介する興奮伝達の様式も無限に変化させることが可能になる。
しかしネットワークがどんなに複雑でも、背景にある生化学的原理はほぼ共通であることが重要で、どんな複雑な神経系回路でも、刺激が誘導するのは、回路自体の特性のリプログラムだ。
これまで、私の知識を再整理する意味で、神経生物学にあまりに深入りしたが、勉強はこのぐらいにして、次回は神経回路による情報と記憶の特性について考えてみたい。
[
西川 伸一 ]
記憶と個性
2017年1月5日
ここまで、ゲノム、クロマチン情報、そして神経細胞ネットワークについて、情報と記憶という観点から検討してきた。今回はこれまでのまとめとして、3種類の情報システムを、個性という観点から整理してみようと思っている。
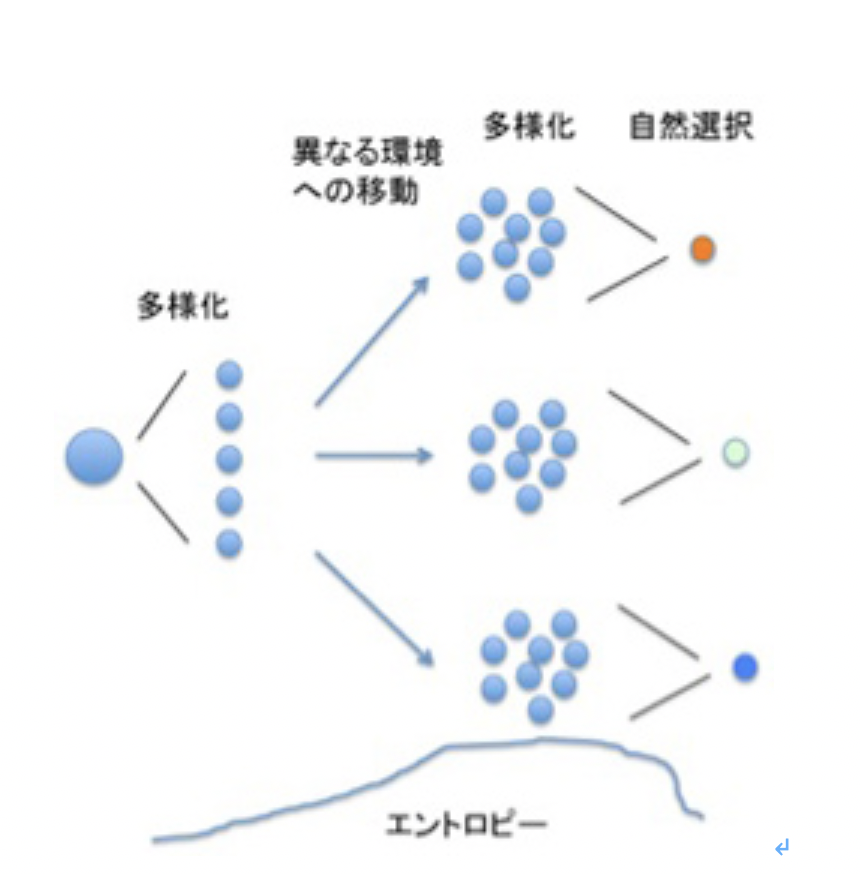
個性というと、「差異、多様性」だけを思い浮かべがちだが、例えばサルと人間の違いを個性とは言わない。個性というとき、あくまでも人間、あるいはサルの個体間で見られる違いについての話だ。したがって、個性という言葉の中には、種としての同一性と個体としての多様性の両方が含まれている。言い換えると、環境に適応するため種としての共通性を維持しようとエントロピーを低下させようとする方向と、ゲノム変異により個体を多様化しようとエントロピーを拡大する方向がぶつかり合うところに個性が成立している(図1)。
図1: ゲノム変異は常に種内のエントロピーを上昇させ、これに対し自然選択はエントロピーを低下させる方向に働く。この結果、種という制限の中で多様性が生まれ、個性が形成される。
おそらくダーウィンほど(ウォレスもだが)、この個性の理解が進化を理解する鍵であることがわかっている人はいなかっただろう。種という制限の中で、次の世代に伝えることが可能な個性が自然に生まれることを確信できないと、自然選択説はでてこない。
人間に個性があるように、あらゆる動物にも個性があることを一旦認めれば、産業革命下の弱肉強食社会を目の当たりにしていたダーウィン時代の都市のインテリにとって弱者が淘汰され強者が残るという考えは当たり前のことだったはずだ。一方、淘汰自体の概念と比べると、あらゆる生物が子孫に伝えることができる個性を自然に発生させるという考えは、背景にあるメカニズムが全くわからないため、受け入れることは簡単でなかったはずだ。もちろん当時の人も、人間を真面目に観察しておれば、それぞれが個性を持っており、誰一人として同じでないことはわかっていたはずだ。しかしダーウィン進化論にとって個性とは、子孫に伝わる性質でなければならなかった。メンデル遺伝学が登場するのは十年後だ。それでも、種としての共通性を基盤として、生殖過程で自然に発生する変異の蓄積が個性を生み、それが子孫に受け継がれると考えたダーウィンの慧眼には瞠目せざるをえない。
次にこの19世紀の議論を、21世紀ゲノム時代の視点で見直してみよう。
今や何百もの種の全ゲノムが解読されている。ゲノムの大きさ、DNA複製のメカニズムを知れば、大腸菌でさえ一回分裂して2個の大腸菌になるとき、両方のゲノムが全く同じである可能性があるなどと考える人はいないはずだ。すなわち、分裂時、あるいは分裂後に個体ごとに異なる様々な変異がゲノムにおこり、ゲノムは多様化し、個性が生まれる。変異は、1代、2代と世代を重ねることにより蓄積し、個体数の増加とともに多様性は増大する。このとき、増殖を損なう変異がおこると個体の維持ができずに自然に淘汰される。逆に、増殖力が高まって他の個体の個性を凌駕することも可能だ。このように、原核生物の場合、生存と複製に必要なゲノム構造が損なわれない限り、種内のゲノム多様性が発生し続け、こうして生まれた個性が環境にフィットすると、今度はこの個性が優勢になり、新しい個性が種として共通の性質になる。
ゲノムのみが経験(自然選択)を記憶できる媒体である原核生物では、ゲノムの多様化はエントロピーの増加を意味する。こうして増加したエントロピーは、自然選択過程により環境にフィットした個性が選択されることで低下する。この過程が異なる環境で起こると、選ばれる個性は異なるため、それぞれの個性へと種全体が収束することで、環境に応じた種が誕生し、種の数は増加する(もちろん環境が同一だと、種は分化できない)。このエントロピーが増減を繰り返す過程の繰り返しが進化で、すべてのゲノムは38億年前の生命誕生まで遡ることができる。このように、ゲノムに蓄えられた過去の記憶はゲノムの個性に等しい。言い換えると、個性とは過去の経験の記憶により形成される多様性と言っていい。(図2)
図2 個体のゲノムは自然に変異を蓄積するようにできている。これにより個性の多様化が起こる=エントロピーが増大する。環境に適応した個体が選択されると多様性は低下し、新しい性質が共通の性質になる。これが様々な環境で起こると、種は多様化する。
原核生物では、ゲノムの記憶がその生物の個性のすべてを決めていると言えるが、多細胞生物が生まれ、生殖細胞と体細胞が完全に分かれると、個体の個性は、ゲノムの個性とは言えなくなる。このことは私たち人間について考えるとよくわかる。
現在では同じ種でも個体間でゲノムが多様化していることがわり、確かにゲノムの個性が子孫に受け継がれ維持されていることは間違いがない。このゲノムの個性から、病気のリスクや、できれば他の様々な性質を予測したいと、個人遺伝子診断サービスが最近提供されている。しかし、個人の全ゲノムを解読したとしても、それですべての個性を予測できると考える人はいない。受精卵が発生を始めてから死ぬまで、我々は様々な経験を通して、ゲノムでは決まらない個性を作り上げていく。これは経験が記憶され、その記憶が個性となるからだが、この記憶はエピジェネティックスとして総称される。ただ、この時の記憶媒体は、クロマチン情報と神経ネットワークの両方(人間では言語も加わるが)からできている。例えば昔人気を博した一卵性双生児姉妹、金さん銀さんの性格や顔があれほど異なるのは、クロマチン情報の記憶と神経ネットワークの記憶の違いが原因だ。
まずクロマチン情報を介する個性について見てみよう。ゲノムの個性と比べた時クロマチン情報を介する個性を研究する難しさは、個体レベルの個性が一つの情報に代表されるのではなく、細胞一個一個の個性の集合として表現されている点だ。
まず発生過程で、何百種類もの細胞が分化するのは細胞ごとにクロマチン情報の違いが生まれるからだ。ただ、発生過程では、決まった細胞を繰り返し安定に分化させることが要求され、クロマチン情報が間違って多様化しないように設計されている。もちろん、この過程でも間違いは起こり、その間違いが細胞の生存や機能を損なわない限り、細胞の記憶として維持される。以前述べたように、クロマチン情報も細胞分裂を超えて維持することができるため、発生の初期に起こった間違いは、多くの子孫細胞に受け継がれる。このような間違いは、時間を経て問題になる場合がある。
有名な例は、1944年の冬、ナチスドイツに封鎖され極度の飢えに苦しんだアムステルダムで胎児期に飢えを経験して生まれた人たちは、高齢になってからインシュリンの分泌が低下し糖尿病になる。これは、胎児発生時に飢えにさらされて起こったクロマチン情報の間違いが、高齢になってから細胞に影響し始めたことを示唆している。同じように、胎児期にお母さんがアルコールを摂取すると、様々な細胞でクロマチン情報の記憶間違いが起こることが知られている。
幸い、クロマチン情報の記憶形成は間違いが少ないように設計されており(増殖因子や分化因子がきめ細かく細胞の方向性を調節する)、それぞれの細胞でおこる記憶間違いはランダムに起こるが細胞の生存から見て許容範囲内で止まっている。またクロマチン情報の変異は細胞ごとの個性になるため、変異が許容範囲を超える細胞は淘汰されるが、個体全体には影響が少ないことが多い。
同じ臓器で同じ細胞が作り続けられるためにはクロマチン情報は必須で、それを維持することは重要だが、発生後も外界のストレスによりクロマチン情報は少しづつ変化する場合が多い。例えば、老化によりクロマチン情報が変化することが知られている。しかし、このような変化は個々の細胞レベルで止まり、各細胞で全くランダムに起こるため、臓器や個体の機能にとって問題にならない。しかし、この個々の細胞にランダムに蓄積した様々なクロマチン情報の変化が集合したものが、クロマチン情報を介する個性として表現される。
以上をまとめると、クロマチン情報の記憶は、各細胞個別に形成される。この記憶は細胞の種類に応じて同一になるよう設計されているが、どうしても小さな記憶違いが生じて、これが細胞の個性を形成する。そして、この細胞の個性が集まって、個体の個性になるが、ゲノムの個性と異なり、個体レベルのクロマチン情報の個性を一つの情報で代表させることはできない。また、クロマチン情報を介する記憶や個性は、各細胞に限局されており、統合されることはない。個体レベルのクロマチン情報の個性は、あくまでも細胞の個性がただ集まっただけの結果だ。
エピジェネティックスな変化の中には、神経ネットワークを介する情報の記憶も当然含まれる。事実、私たち人間の個性は、脳の個性として表現される部分が多い。例えば、生後訓練を繰り返して筋肉が発達し、早く走れるようになる過程にアメフラシで見たのと同じ神経ネットワークを介する記憶が大きく寄与している。もちろん、筋肉自体も発達し、これにはクロマチン情報の変化も寄与するが、神経系の記憶が存在しないと筋肉は発達しない。残念ながら、こうして訓練した結果は、次の世代に受け継がれず、一代限りだ。
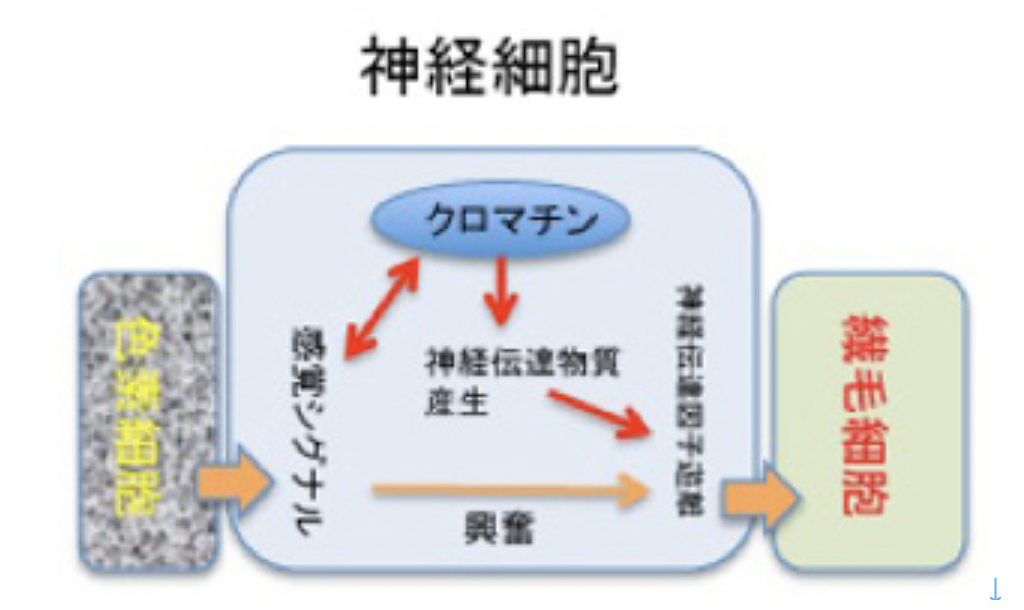
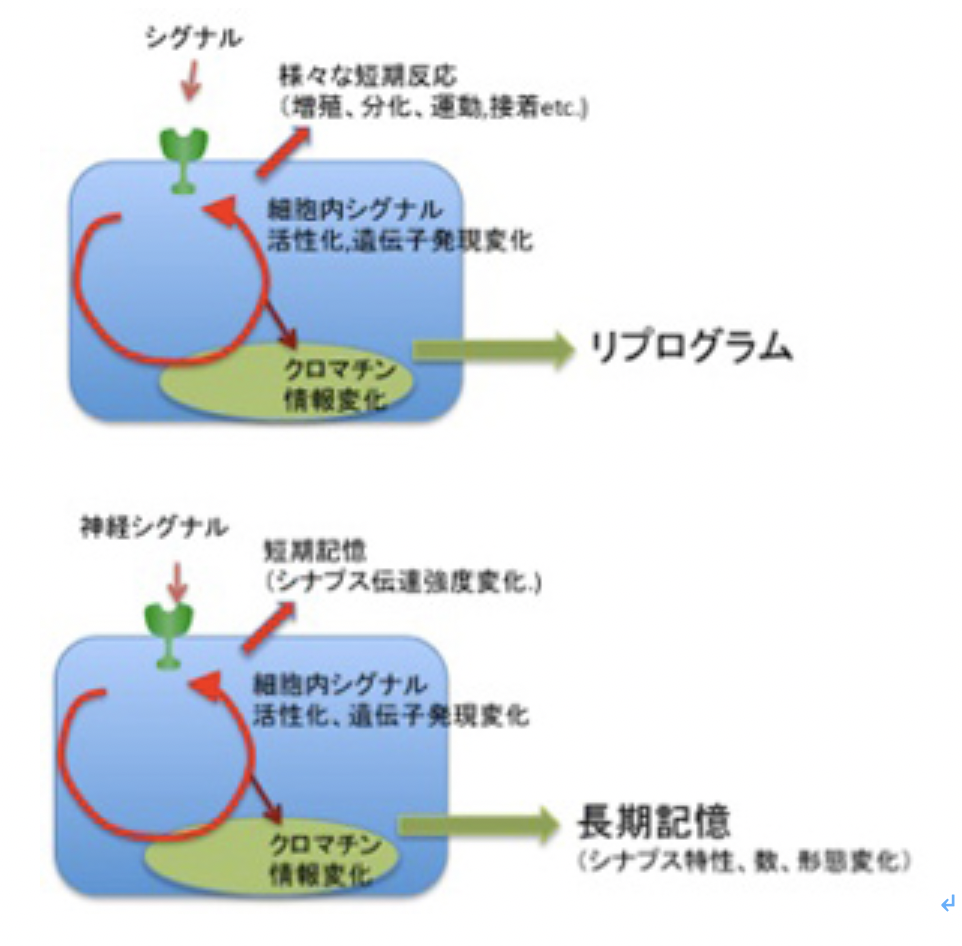
神経ネットワークのメカニズムを突き詰めると、細胞が発生し、成長し、老化する過程で起こるクロマチン情報の記憶と同じと言っていい。どんなに複雑な脳神経系でも、進化過程でゲノムに蓄積された記憶情報に基づいて空間的・時間的に発現する特異的なシグナルに従って順々にクロマチン情報が変化した細胞を分化させ、これをゲノムの記憶に従って立体的に構造化させることで、形成される。また、生前、あるいは生後それぞれの神経が受ける刺激に対しては、一次的な反応が細胞内シグナル伝達経路の活動として反応する。そしてシグナルの質や強さに応じて、前回 見たように、神経細胞のクロマチン情報が変化し、長期記憶が成立する。しかし図3に示すように、神経細胞の反応は他の体細胞の反応と全く変わるところはない(図3)。
図3:神経細胞と一般体細胞の比較。
一方、一般の体細胞と神経細胞の記憶は、個々の細胞内で起こる変化が個体レベルで統合されるかどうかという一点で大きく異なっている。すでに述べたように、クロマチン情報の記憶に起因する細胞の個性は、ただ集合して個体の個性に寄与するだけだが、神経系では細胞レベルのクロマチン情報の変化に起因する個性は、細胞同士がネットワークを形成することで、個体レベルで統合される。この統合は、神経細胞にとどまらず、筋肉やホルモン産生細胞など、多くの体細胞をも統合できる。
実際には、同じような細胞の変化を統合して個体の個性を変化させることは、内分泌システムにも見ることができる。オタマジャクシがカエルへと変態を遂げる時、甲状腺ホルモンが分泌され、体全体の細胞を統合する。同じことは、私たちが思春期に急速に様々な性的特徴を発生させるのも同じだ。しかし、一見個体全体を統合している高等動物の内分泌システムを詳しく見てみると、ほとんどがどこかで神経系とつながっており、神経ネットワークの記憶の支配を受けていることに気づく。
このように、神経細胞は、神経細胞にとどまらず様々な細胞と直接、間接にネットワークを形成する能力を開発し、全く新しいレベルの個体性の統合を可能にしている。
これに加えて、神経ネットワークでは、視覚、聴覚、嗅覚など、外界の変化を迅速に、立体的に捉え、この入力を個体として統合された神経ネットワークにリンクさせることができる。これにより、環境を全く異なるレベルで自己化することが可能になった(例えば景色の記憶は、環境を自己化したと言える)。もちろん、外界の自己化は原始ゲノム発生以来、生物進化の駆動力と働いてきたことだが、神経系による自己化は、あるがままの外界を表象し自己の延長として自己化する点で、これまでの自己化とは全く異なる。
この個体内外の統合と、自己の発生についてはわかりにくいと思うので、次回は、「統合と自己」というタイトルで、神経系ネットワークが可能にする個体と細胞、個体と外界の統合能力について解説してみたいと思っている。
[
西川 伸一 ]
統合と自己:細胞の個性と個体の個性
2017年1月16日
今回は個体と細胞の関係を考えながら、神経情報の特殊性について見てみる。
教科書的には、多細胞体制の誕生は細胞の個性と個体の個性の分離をうながし、またその結果個体のゲノムを継承するために生殖細胞が誕生したことになる。しかし、生殖細胞が誕生した後も、有性生殖だけが個体のゲノムを継承する方法ではない。例えばプラナリアのように個体全体が分裂する場合もある。植物では体細胞からカルスが形成され、そこから完全な植物個体を形成することができる。
https://www.flickr.com/photos/internetarchivebookimages/20705306246/sizes/o/ )
有性生殖と無性生殖が共存できるのは、ほぼ同じゲノム情報が全ての細胞に存在しているからに他ならない。もちろん、細胞ごとにゲノム情報の小さな違いは生じているが、原則的にほぼ同じゲノム情報が個体の全ての細胞に存在していると考えていい。無性生殖を行わない動物でも、体細胞の核移植によるクローン動物作成実験から(哺乳動物のように複雑な動物でも、体細胞のゲノムを未受精卵に移植すると、新たな個体が発生する)、全ての細胞に完全なゲノム情報が存在していることが示された。この意味で、ゲノム情報の同一性が、細胞と個体の統一性を保証していると言える。
しかし、植物やプラナリアでは体細胞から個体を形成できるのに、私たち人間の細胞は、決して個体を形成することはない。この理由の一つは、私たち人間の細胞は、ゲノムは受精卵と同じでも、体細胞への分化過程で変化した細胞それぞれのクロマチン情報を簡単にはプログラムし直すことが難しいことだ。実際プラナリアも同じで、分化した細胞は他の細胞に分化し直すわけではなく、全細胞のうち3割がクロマチン情報を変化させやすい多能性幹細胞でできているからだ。同じゲノムを持っていても、不可逆的にそれぞれのクロマチン情報が選び取られて発生が進むことを、英国の発生学者ウォディントン(C.H. Waddington)はエピジェネティック・ランドスケープ(epigenetic
landscape、後成的風景)という絵を用いて表現している。しかし、分化細胞を他の種類の細胞へと変化させることが難しいお陰で、私たちは明日皮膚が血液に変わってしまっているという心配をしなくて済む。
図1 ウォディントンの描かせたepigenetic landscapeの絵をわかりやすく書き直した図で、この概念を示す際、最もよく使われる。上部にあるビーズは様々な場所に動き得るが、一旦分化の方向性が決まると、他の道は選べないことが示されている。
結局、我々人間では、受精卵から始まる一生で一回きりの、ゲノムの指示に従う発生過程を通す以外に、必要な細胞を準備することはできない。ES細胞やiPS細胞の研究から、受精卵に限らず、体のあらゆる細胞を作る能力を持つ細胞が得られることが明らかになり、他の細胞から区別して多能性幹細胞と呼ぶようになっている。しかしあらゆる細胞に分化できる多能性幹細胞の塊から始めても、正常な個体を発生させることはできない。なぜなら、動物の発生過程では、個々の細胞が個体との関係を読み取り、これにより得られる情報の指示に従ってクロマチン情報を変化させることが要求される。例えば四肢はほとんど同じようなメカニズムで体幹から飛び出すが、頭に近いところにある細胞から腕が、遠いところにある細胞から足ができる。これも、各細胞がボディープランから見て最もふさわしい組織の形成を指示する、すなわち適切なクロマチン情報を確立するための情報が体の各部に用意されているからだ。しかし、体の体制を構成しているのも細胞だ。どちらが原因で結果かがわからないという因果性の問題が発生学には常に存在している。
ゲノムには、発生に応じて必要な遺伝子セットを発現させるためのプログラムが存在し、多能性の幹細胞は発生に合わせて様々なクロマチン情報記憶を展開することができる。多能性幹細胞は様々な条件下でほとんどの細胞へと分化できるが、秩序ある個体を形成するためには細胞の多能性だけでは不十分で、細胞が初期胚が持つ個体の体制からのシグナルを受けることが必要になる。例えばES細胞を集めて個体に移植したり、あるいは試験管で培養したりしても、奇形腫と呼ばれる秩序のない構造ができるだけで、マウスはできない。しかし同じES細胞を胚盤胞に注入すると、胚盤胞の体制に組み込まれてES細胞は正常個体を形成することができる。
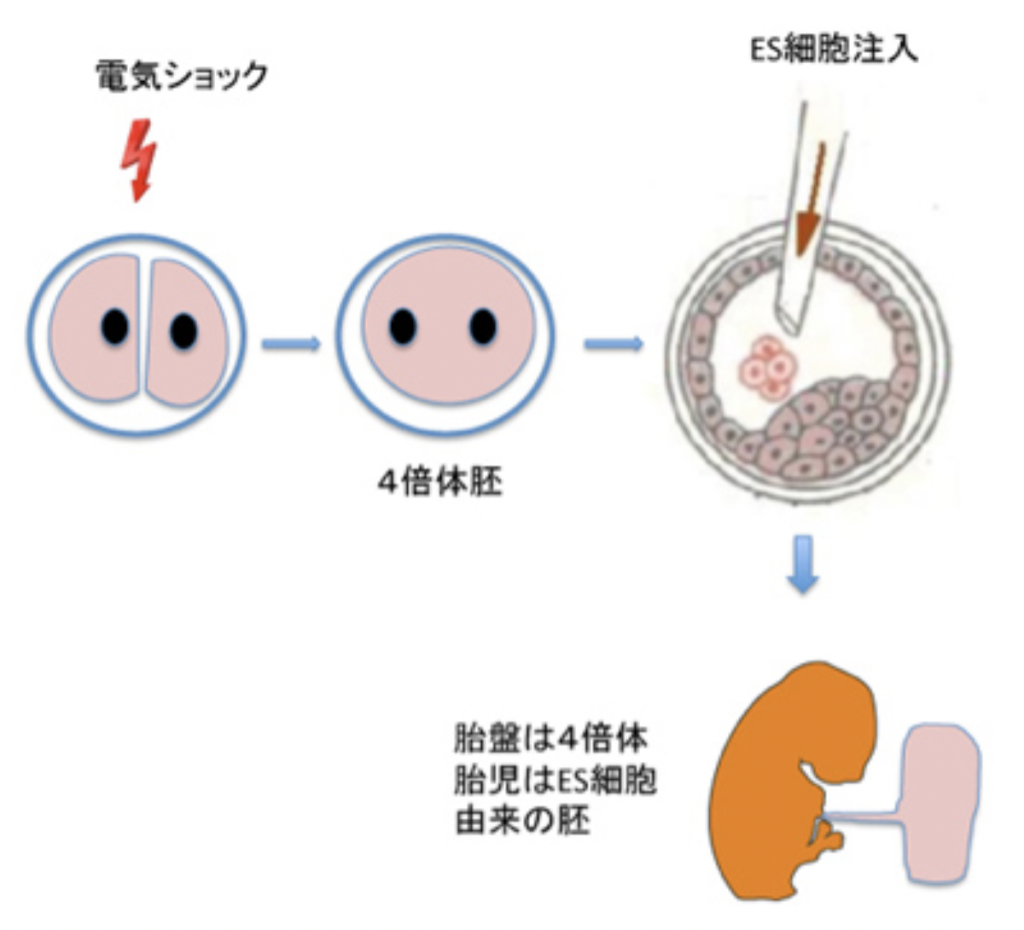
胚盤胞の体制自体が持つトップダウンの力を最もよく示す例が4倍体補完法と呼ばれる方法だ(図3)。受精卵が分裂した時に電気ショックで細胞を融合させると4倍体の胚ができるが、この胚盤胞をES細胞の塊に指示を与える構造として用いることができる。4倍体の胚は胚盤胞期まで発生するが、胎児細胞はそれ以上発生ができない。一方胚外のトロフォブラストは機能的胎盤を形成できる。このため胚盤胞に移入したES細胞やiPS細胞は、死滅する4倍体の細胞の代わりに発生する。すなわち、胎盤は4倍体の細胞から、胎児部分は注入したES細胞からできた合成胚を作り、発生させることができる。単純な構造に見える胚盤胞にも、細胞の分化に指示する体制が存在することがわかると思う。
このように発生学は、細胞の分化を指示する個体の体制とは何か?そのシグナルを受けた分化細胞がどのようにして個体へと統合されるのか?など、常に全体と部分の関係を研究してきた。このことは、例えば古典的な発生学で、オーガナイザー(organizer)とか、誘導物質(inducer)、ボディープラン(body plan)という個体の体制を示す言葉が重視されていることをみれば理解できる。この発生学の特殊用語を使ってまとめると、ゲノムの記憶を正確に展開するためにも、最初はオーガナイザーが必要で、このオーガナイザーもまた細胞からできており、ゲノムに指示により形成されるのだが、卵の形成過程、受精過程、着床過程など外部の要因が関わって形成される。
このように「卵が先か、鶏が先か?」の問題と同じで、発生では全体と部分は一体化しており、原因と結果の区別を困難にする。同じように、発生でのゲノム情報とクロマチン情報の関係も一体化している。発生でのクロマチン情報の変化は、ゲノムにコードされたプログラムで進むが、クロマチン情報がないと複雑な多細胞生物のゲノムの記憶を展開することができない。
では前回 述べた多細胞動物に見られるゲノム情報、クロマチン情報の個性とはなんだろう。発生過程で一つの系列内の細胞の多様性が生まれることは、ゲノムやクロマチン情報の間違いと考えていい。これらの情報の変異は細胞ごとに起こるが、許容範囲以上の間違いは致命的になるか、細胞レベルで除去される(例外と言える免疫系は後で説明する)。発生、成長の過程で個々の細胞レベルで発生する個性は、個体の個性として統合されることはないが、細胞レベルの個性が個体に影響を及ぼす時、病気、老化などの異常として現れる。
少し長く説明しすぎたが、神経情報が誕生するまでは、新しく生まれた情報システムも、それ以前に存在した情報から独立することができていなかったことを示すためだ。これに対し、新しく生まれた神経情報は、他の情報に依存した生命活動から、大幅な独立を勝ち取っている。
もちろん神経ネットワークも、その形成や維持はゲノム情報、クロマチン情報に完全に依存しており、神経情報だけが独立することはない。体がないと、脳は機能せず、神経情報維持できず、心もできない。しかし、神経情報のオペレーションを詳しく見てみると、それ自体で他の情報から独立して働くことができ、また各細胞に生じた個性がそのまま神経系全体の個性として統合されていることがわかる。
例えば、一卵性双生児間の個性を考えてみると、細胞レベルのクロマチン情報の違いが集まって生まれる個性の違いと比べ、神経ネットワーク情報に起因する性格や記憶の違いは際立って大きい。すなわち、神経ネットワークの枠組みが一旦形成されると、神経情報のオペレーションは自由度が高く、結果多様な個性を形成できることを意味している。個性が多様化できるということは、他の情報からの独立性が高いことだ。この独立性が、デカルト以来私たちが心身二元論に陥る理由の一つだと思う。
しかしなぜ身体の死とともに消滅する運命の神経ネットワークの情報が、心身2元論という錯覚を生むほどの独立性を獲得できたのか?その原因について最後に考えてみよう。(以下は私の妄想でしかないことを断っておく。)
神経ネットワークが持つ最も重要な特徴は、様々な神経細胞があるにもかかわらず、各神経細胞の興奮、細胞内(軸索や樹状突起)での興奮の伝搬、そして神経間の興奮伝達のための原理がほぼすべての神経細胞で共有されている点だ。そのおかげで、視覚であれ、嗅覚であれ、触覚であれ、全てのインプットを同じ神経ネットワークで共有することができる。また、インプットに対するアウトプットも、筋肉を動かす運動からホルモンの分泌に至るまで実に多様で、多くの組織を直接間接に支配してネットワークの中に組み込むことができる。もちろん、インプット・アウトプットだけでなく、神経同士が刺激・抑制し合う回路も形成される。同じ原理で作動できるため、神経細胞の数さえ増やせば、無限に神経細胞同士を組み合わせ複雑なネットワークを形成することができる。こうしてできた神経ネットワークも、神経間の結合の特異性や強さを変化させるためにはゲノムやクロマチン情報に依存したメカニズムを用いるが、クロマチン情報が「ゲノムのon/off」のための情報であるのとは全く異なり、形成される記憶自体は、直接ゲノムやクロマチン情報と関係はない。
このようにゲノムとクロマチン情報に依存して発生が進み一旦回路が形成されると、あとは外来の刺激が回路のパターンを変化させる例は、すでにアメフラシの水管反応 で説明した。アメフラシ水管反応回路では、刺激を受けなかった回路と、刺激を受けた回路では全く回路特性が異なる。これは回路構造の中の神経細胞の特性が変化したためだが、この変化は回路全体の個性として統合される。このように、神経回路はこれまでの情報と比べて、高い自立性を持ち、興奮伝達の原理を共有することで無限に複雑化する可能性を獲得した。しかも、さらにこの共通性のおかげで、個々の細胞レベルで生じた神経細胞の個性はネットワークにより共有されることで、神経系全体の個性へと統合される。
細胞の個性を統合することができる神経系の誕生は、刺激が消えた後もその刺激の影響を維持することを可能にした。この点については、同じようにほぼ無限と言える外来抗原に反応できる免疫系と比べてみるとよくわかる。
免疫系は無限の化合物に対して反応できる。これは、多様な抗原の一つ一つに対して反応する個別のリンパ球が体内に存在するからだ。すなわち、同じ細胞を繰り返し作り、細胞に個性が生まれるのを極力拝する他の組織と異なり、リンパ球は最初から異なる個性(抗原特異性)を持つよう分化する。この個性はゲノムレベルの個性で、抗体やT細胞受容体遺伝子を不可逆的に変化させ、それぞれのリンパ球に異なる抗原受容体遺伝子を発現させるリンパ球特異的な遺伝子再構成メカニズムに依存している。しかし個々の細胞レベルの免疫反応は抗原に反応する細胞だけでとどまる。すなわちリンパ球同士の反応には必ず抗原の介在が必要で、抗原がなくなると細胞間の相互作用は消滅する、一方、神経の場合は刺激が消えても、細胞相互作用は維持できる。
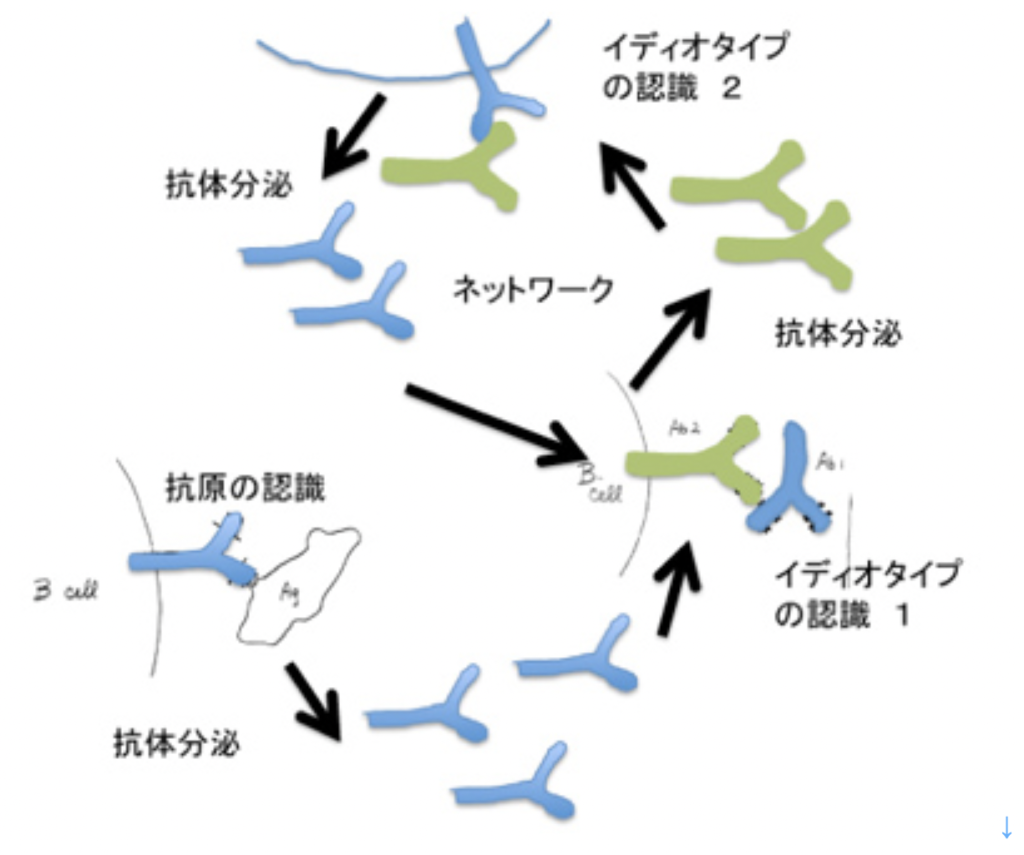
ニールス・イェルネらは、抗体が他の抗体により認識できる(イディオタイプ)という現象を元に、リンパ球同士は抗原を介さずに、神経のように直接相互作用できるとするイディオタイプネットワーク説を唱えた(図4)。しかし、抗体が認識し合ってネットワークを作るという考えはは最近ではあまり支持されなくなっている。結局、免疫系が無限の抗原に反応できるのは、ネットワークとは無関係に、リンパ球の抗原反応性に最初から多様性があるからだ。結局免疫反応とは、抗原反応性の異なる個別の細胞ごとに増殖、分化寿命延長などの細胞学的変化が起こることに他ならない。
一方、イェルネが考えたように、免疫系でネットワークが成立するためには、最初の刺激が消えた後も、リンパ球同士で刺激しあえるメカニズムが必要だ。免疫系では、図4に示したことは理論的には可能でも、現実には特殊な状況だけで起こっているようだ。
一方図4に示したネットワークは神経系では成立できる。神経系も、味覚や嗅覚として化学物質を感じ、記憶できる。化学物質に反応する点では、免疫系と同じだが、例えばワインを一口飲んで、実際の刺激は胃の中に消えてしまっても、味や匂いを他の感覚と関連させ、記憶として維持することができる。これは、刺激が消えた後も、匂いや味の刺激によって生まれた新しい回路の活性が維持できることを意味している。これが可能なのも、神経細胞が同じ原理を共有し、回路を形成できるからだ。
以上、全ての神経細胞が興奮のための原理を共有することで、神経細胞同士で無限に複雑なネットワークを作り、また各神経細胞の変化を、ネットワーク全体の変化として共有できるようなったことで、心が身体から離れてしまうという心身2元論の幻想が生まれるほど、神経ネットワークによる情報が、ゲノムやクロマチン情報から独立した、独自の情報系を作ることができたことを納得していただいただろうか。
次回からは、各細胞の変化が統合可能で、他の情報から独立している神経情報系により可能になった脳新しい情報機能について見ていきたい。
[
西川 伸一 ]
2019年8月17日
ビリルビンは医師にとっては最も馴染みの深い肝臓の機能を調べる検査だが、ビリルビン自体は赤血球が壊れた後の処理機構の一つとして考えてきた。したがって、ビリルビン自体に機能があるとはあまり考えたことはなかった。
今日紹介するジョンズ・ホプキンス大学からの論文はそのビリルビンが神経細胞を守る重要な機能を持っていることを示した論文でCell Chemical Biologyにオンライン掲載された。タイトルは「Bilirubin
Links Heme Metabolism to Neuroprotection by Scavenging Superoxide (ビリルビンはヘム代謝をスーパーオキサイドの除去による神経保護作用とリンクする)」だ。
この研究のハイライトは、ビリルビンは老廃物ではなく、機能を持っているはずだと考えたことに尽きる。あとは、細胞内でビリルビンが決して合成できない様にビリヴェルディンをビリルビンに変える酵素BVRを完全にノックアウトしたマウスを作成し、ビリルビンが合成されず、代わりにビリヴェルディンが蓄積することを確認している。
著者らはもともとビリルビンが酸化ストレスを抑える機能を持つのではと考えており、これを示すため細胞内にスーパーオキサイドを発生させる処理を行い、ビリルビンが合成できない細胞と正常細胞を比べると、ビリルビンができないことで細胞内、特にミトコンドリア内でスーパーオキサイドが蓄積し、結果細胞が死にやすくなっていることを確認する。ただ、自分でビリルビンが合成できなくとも、外来のビリルビンは細胞内からミトコンドリアに侵入して、スーパーオキサイドから細胞を守ることができることも示している。
さらに、ビリルビンは化学的にスーパーオキサイドに特異的に直接結合することで細胞をスーパーオキサイドから守っていることを確認している。
最後にビリルビン合成酵素は神経細胞で強く発現しており、またグルタミン酸受容体刺激によりスーパーオキサイドが合成され、これが長期記憶などに関わっていることに注目し、このスーパーオキサイドの機能をビリルビンが抑えるかどうか、ノックアウトマウスで調べている。結果は予想通りで、ビリルビンがないとNMDA受容体刺激による興奮性が上昇し、神経細胞が変性することを示している。
結果は以上で、これまでビリルビンは神経毒かと思ってきたが、実際には神経を過興奮から守る重要な役割を担っていることがよくわかった。おそらく、パーキンソン病など神経変性疾患にも何らかの形でビリルビンが関わっている可能性がある。この歳になってまた新しいことを知ったという気分にしてくれた研究だった。
2019年8月16日
ゲノムの発生学 I
2015年10月15日
ゲノムの解剖学、そしてゲノムの働き(生理学)とくると、当然次ぎにくるのはゲノムの発生学だ。ゲノムの発生学のほとんどは進化の過程とオーバーラップするはずで、この紙面で簡単に説明することなど叶うはずがない。代わりに今回からゲノムの発生学として、これまであまり議論されてこなかった観点からゲノムの誕生や進化の過程をゆっくり整理し直したいと思っている。今回は、そのイントロダクションになる。
重要なことは、ダーウィン時代と異なり、ゲノムの解剖学や働きについてずいぶんわかっている点だ。従って、ゲノムについて理解が進んだ時代のゲノム発生学(進化学)とは何かを考えることになる。これまでゲノムの解剖学や生理学の説明を通して、ゲノムは多様な内容を表現していても、結局は情報であるとことを強調してきた。この意味で、ゲノムの発生学を考えようとすると、情報の発生学を考えることになる。ところが日常情報という言葉を当たり前のように使っている我々も、情報の発生学と言われる何を考えていいのか戸惑う。なぜだろう?まず生物のゲノムを私たちが普通使っている情報との比較をしながら考えてみよう。
生物が生きて活動するオペレーションのためにゲノムが表現している情報には、アミノ酸配列の情報、機能的RNAの配列情報、遺伝子発現を調節するための様々な情報、遺伝子の円滑な発現に必要なゲノム構造化のための情報など、多様だ。ただゲノムを分解してみると、ゲノム上の情報のほとんどは、全て生命オペレーションに必要なタンパク質と様々な機能的RNAを必要に応じて作るために組織化されている情報と言える。このため、生物を機械にたとえ、ゲノムを生物の設計図と説明する人がいる。例えばゲノムについてかかれた本を見てみると、「初めて学ぶゲノム生物学:生命の設計図」、「ゲノム:命の設計図」、「ゲノム=人間の設計図をよむ」などのタイトルが踊っている。個人的には設計図より、パソコンのソフトウェアのように、生物のオペレーションの指令書といった方がまだ正確なように思えるが、なぜ私たちはゲノムを設計図や手順書に似ていると考えるのだろう?
デカルトは人間を心と体に分け、体は機械と同じだと考えた。また心のない動物は機械でしかないとも考えた。そしてこのドグマはほとんどの生命科学分野の根幹を今でも脈々と流れている。しかし、実際の生物は機械とは全く違っていると誰もが直感する。何が違うのか?
自分で考えて将棋を指すように見えるコンピュータといえども、機械はその背景に設計者、すなわち人間の意図が存在している。例えばシャベルカーを考えよう。シャベルカーは穴を掘るという人間が決めた目的に従って設計され、組み立てられる。そして完成したシャベルカーを運転してその意図を実現するのも人間だ。動いていない機械だけを見ているとそこに人間の存在はないが、実際には機械そのものが人間の意図の塊だ。石より固い鉄、自由な動きを可能にする油圧システム、駆動エンジンなど、本来はシャベルカーとは全く別に開発されてきた数多くの部品が、シャベルカーに集められている。全ては設計者(=人間)の意図に従って組み立てられるが、シャベルカー位複雑な構造になると、この意図を情報として表現する指示書や、設計図が必要になる。さらにこの機械を設計するのも人間であることから、運転する人間が扱いやすいよう設計するのも重要だ。
現代なら、人工知能を導入した自動のシャベルカーも存在しているはずだ。自分で学習し、初めての場所でも上手に穴を掘ることができるかもしれない。しかし、一旦人間により決められたシャベルカーの目的は変わることはない。シャベルカーが自分で目的を逸脱してスポーツカーになることは決してない。これは、人間が操縦しようと、全自動であろうと、全ての機械の目的は人間により決められており、またそのオペレーションも人間との対話の上で行われるよう設計されている。
少し余談になるが、最近自ら考え判断する人工知能の開発が進められているが、これが成功するといつか人間から独立し、人間を支配するのではないかと心配されている。ただ人工知能も機械である以上最初の目的は人間が与える。このとき心配する必要があるのは、与えられた目的をもっとも有効に成し遂げようとして、人間を排除することだ。例えば人工知能に穴を掘れと命じて、その後途中で穴掘りをやめさすためスウィッチを切ることを考えてみよう。もし人工知能がこのやめるという意思を、目的遂行を邪魔すると判断すれば当然スウィッチを切ろうとした人間は排除されるだろう。とはいえ、機械はその背景にある人間の決めた意図なしでは存在しない。
この機械の背景にある人間の意図と同じものを、私たちは生物にも感じる。この感覚が、私たちにゲノムは生命の設計図と言わせている。もしデカルトに、生物という機械に外から目的(設計図)を与えているのは何か?と直接質問したら、おそらく彼は生物に目的を与え、それに沿って設計するのは神だと答えるように思う。すなわち、機械の背景に必ず人間がいるように、生物という機械には神の意志が存在すると考えていた。しかし、神を生物の背景から排除すると(私は当然だと思っている)、機械に対する人間のように、生物に目的やデザインを与えるものはどこを探しても見当たらなくなる。実際にはこの生物の目的の探求が、18世紀自然史思想の誕生以来続けられ、ダーウィンを経た後ようやく見えてきた解の一つがゲノムに集約した。この歴史を考えると、生命の構成成分をコードする遺伝子が組み込まれたゲノムを設計図や指令書と考えて不都合はない。DNAという媒体は物質だが、ゲノム自体は情報で、物質的ではないし、目にも見えない点でも、機械の背景にある人間の意図に似ていると言えるのではないだろうか。
しかし、ゲノムを生物の設計図や指令書であることを認めたとしても、機械の設計図とは全く違う問題がゲノムにはある。それは書いた人がいないという問題だ。私たちは普通の情報を考える時、それがどうしてできたか、すなわち発生学はあまり問わない。というのも、情報には確実にそれを発信した人間がいるからだ。機械のデザインや設計図も同じように、書いた人がはっきりしている情報だ。一方設計図と言っても、ゲノムには書き手がいない。このため、ゲノム情報を考える時は、書き手がいないのに情報がどうして生まれるのかをまず知る必要がある。
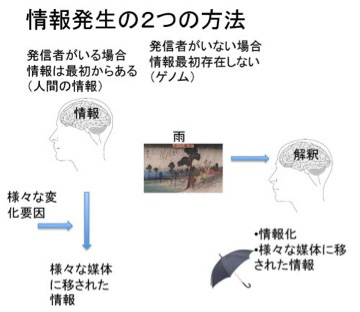
私たちが情報について語るとき、必ずしも発信者のはっきりした情報だけが念頭にあるわけではない。例えば、私がこの原稿を書くのに疲れて窓を見ると、天気は秋晴れだ。ちょっと散歩でもするかと伸びをして部屋から出たとしよう。これは、窓の外の日光の様子を私が心地よい秋晴れと解釈した結果だ。逆もある。例えば雨が降っていたら、傘を持って外に出る。これも雨が降っているという情報を私が傘を持って出ることを指示する情報と受け取ったからだ。この場合私が情報として受け取った天気の状態は自然現象で情報ではない。同じ雨でも、畑にとって恵みの雨もあれば、川の氾濫を引き起こす雨もある。全て状況と解釈者の状態によって決まる一種の解釈だ。すなわち、誰かが書いた情報でなくとも、それを解釈する主体があれば情報になる。発信者のいないゲノムが情報になりうるのは、この解釈という能力がゲノムに備わっており、この過程を通してゲノムが情報化していくと考えられる。
この解釈プロセスは、原始生命誕生時のDNA分子が情報を担う様になりゲノムが誕生する過程と、ダーウィン進化過程に分かれる。次回からできるかどうか自信はないが、この過程についてさらに考えてみたい。
[
西川 伸一 ]
ゲノムの発生学 II
2015年11月2日
物理化学現象を人間が解釈するとき現象の情報化が起こるが、本来物理・化学に情報という概念はない(量子力学は少し忘れよう)。従って、生命が誕生するまで、物理化学法則のみが支配する地球に情報は存在しなかった。最初の生命については知る由もないが、生命誕生とほとんど同じ時期に(同時という意味ではない)、DNAを媒体とするゲノム情報が生まれたことは間違いない。これが地球における最初の情報の誕生になる。ゲノムの発生学はもちろんこの誕生から始まる。自信がないが、地球上での情報の誕生について今回は考えてみよう。
発信者なしに情報が生まれるためには、もともと情報でないものを情報として解釈する「主体」が必要になる。ただそんな主体は生物誕生前にはもちろん存在しない。最初に存在したのは物理化学法則に従う分子と分子の相互作用だけだ。しかし、分子間相互作用も一つの分子の側から見てみると、近づいてきた分子と結合するか離れるか、自分の構造に基づいて解釈していると言える。したがって、解釈という行為自体は核酸のような情報分子に限らず、どの分子にも考えられる。しかし私たちの住む大気の中で、酸素、炭酸ガス、窒素は常に衝突しているが、それぞれが反応する(解釈する)ことはほとんどない。すなわち、解釈のような振る舞いは、複雑化した分子構造のほうが生まれやすい。特に有機分子のポリマーは様々な分子と相互作用が可能だ。タンパク質や核酸が様々な高分子と「非特異的」に結合することは、生化学実験の経験者は誰もが知るところだ。
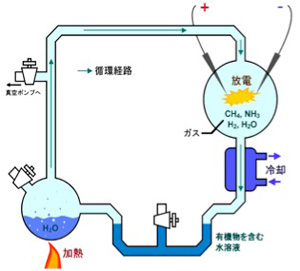
次に考える必要があるのは、この条件を満たす有機ポリマーが原始の地球に存在していたかどうかだ。生命に頼らず有機物を合成する有機化学はヴェーラーの尿素合成までさかのぼる。ただ、生命誕生に関わる化学の先駆は、ユーレイとミラーのアミノ酸の合成実験で(図1)、この研究以後生命誕生の化学について地道な研究が進んできた。
Wikiコモンズ より)。(Science 130, 245, 1959)
この実験以降に蓄積されたデータを詳細に解説するのは私には荷が重い。都合のいいことに、これまでの研究をまとめると、核酸、アミノ酸、脂質など有機化合物は生命以前の地球で合成されていた可能性が高い(合成できていないと生命は誕生できないことから当然だが)。また、自由エネルギーから見たとき、簡単には起こりえない有機分子のポリマー形成も、熱、濃縮、氷結などの変化が、鉱物や粘土などの自然の触媒と組み合わさると可能であることが示されている。例えば、モンモリロン石は、アミノ酸の重合と、リボ核酸の重合を促進する触媒活性を持っており、アミノ酸、核酸のポリマー形成を誘導できることが示されている。従って、アミノ酸や塩基が重合した様々な長さのポリマーが原始の地球に存在しできた(このabiogenesis, systemic chemistryについては優れた本や総説が書かれており、とりあえずKepa Ruiz-MirazoらのPrebiotic systems
chem.istry: new perspectives for the origin of life, Chemical Review 114,
285-366, 2014 を紹介しておく。)。
次の問題は、様々な有機分子が存在するようになった地球で、情報、特に核酸を媒体とする情報が生まれた過程だが、これについては全くわかっていないし、実際に起こったことを特定することは永遠にできないかもしれない。しかし様々な可能性を考えることは可能だ。一つの可能性を考えてみるが、すべて私の頭の中妄想だと思ってほしい。
明確な意図やデザインの元に合成されたわけでなくとも、アミノ酸や核酸がランダムに繋がって生まれた分子同士が、互いに相互作用できることが知られている。しかし相互作用と言っても全ての相互作用は偶然の産物で、ただ分子同士が付いたり離れたりしているだけだ。ただランダムにでも多様性が生まれると、その中から一部が選択され進化が起こることを思い出してほしい。環境による選択は多様な分子反応の間でも起こり、その結果反応が向かうべき目的のようなものが生まれる。すなわち、ダーウィンの進化論を生命のない分子にも適用することができる。例えば分子の安定性と持続性という目的が自然に反応している分子の間に生まれることは十分考えられる。他の分子より高い安定性があると当然存在時間が長くなる。分子の存在時間は環境による選択の結果として現れ、ダーウィン進化での「長い首」と同じ目的性が生まれる。
このような選択が起こることを一番理解できるのがホモキラリティーという現象だ。例えば地球上の生物に存在するタンパク質はL-型アミノ酸だけからできている。一方糖鎖になるとD-型だ。ランダムに合成されるアミノ酸の中からなぜ生物はL型のみを使うようになったのか?すべての生命でこの選択が行われていることから、おそらく生命誕生以前のabioticな過程で、ホモキラリティーが生まれたと考えられ、そのメカニズムの研究が進んでいる。メカニズムはともかく、この現象から生命の関与なしにこのような選択が生物界全体で起り得ることを理解することができる。
分子の安定性は、一つの分子だけでなく、幾つかの分子の組み合わさったセットとして生まれる可能性が高い。例えば、アミノ酸や核酸が重合したポリマーは私たちが考えるよりはるかに壊れやすい。溶液中のイオン構成や、あるいは他のポリマーとの相互作用により少しでも分解されにくくなれば、一つの分子単独ではなく、分子が組み合わさったセットが選択されることは十分考えられる。分子間相互作用の結果、安定性だけでなく分子の増幅ができればなお高い環境への適応性が生まれる。
実際、ランダムに形成されたポリマーの中には、新しいポリマー形成を促す触媒のような性質を持つ場合があることも知られている。例えば、塩基が10個並んだRNAポリマーがあると、さらに長い50個並んだポリマーが形成できることが示されている。他にも、アミノ酸や塩基が長いポリマーを作る段階では、できたポリマーの一部が一種の触媒の働きをして、より長いポリマーを形成するのに一役買っていることも示されている。
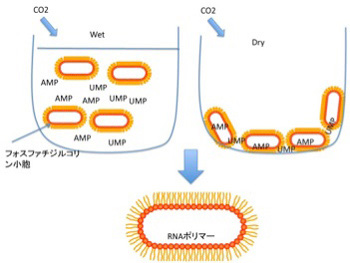
中でも興味を引くのが、脂肪酸と核酸が相互作用する状況では様々な反応の効率が上がるという実験だ。例えば、AMP,UMPのようなリン酸塩基をフォスファジル酸から作った小胞と混ぜ、熱を加えながら炭酸ガスを吹き入れ乾燥させ、その後また1mMHClを加えて溶解するというサイクルをくり返すと、脂肪膜の小胞に閉じ込められたRNAポリマーが合成できることが示された(Orig Life Evol Biosph 38:57、2008)。普通、実験室で核酸を重合させるとき、重合が自然に始まるよう核酸モノマーを活性化するのだが、この実験で使われたのはAMPとUMPで全く活性化されていない。熱と乾燥による濃縮が繰り返す条件さえ外部から与えれば、脂肪酸の助けでRNAが重合化することが示されたことは、後でのべるRNAワールドの可能性を示す重要な貢献だと考えられている。DNAの複製についてはさらに驚くべき結果が報告されている。50merの鋳型と、AMP,GMP,CMPなどをPOPA (palmitoyl-2-oleoyl-sn-glycero-3-phosphate)と混合して、熱を加えながら乾燥と水和を繰り返すと、10%程度のエラーはあるものの、鋳型に合わせたDNA複製が起こることが、2011年カリフォルニア大学サンタクルズ校のグループによって示された(Biochimei 93, 556, 2011)。以上のように、ランダムな有機分子の相互作用が脂肪膜に囲まれたRNAやDNAのポリマーの形成にまで発展できる。
このようなシステム化学の研究と、現存の生命に見られる有機高分子の機能分担を合わせて考えると、例えば複製にはDNAが適していること。一方、化学反応の触媒としてはタンパク質、脂肪が適していること。そして、RNAは両方の機能を持ち得ることや、タンパクとDNAの両方と相互作用が可能で、両者の機能を結びつけることができる分子であること。そして、必要なすべての化学エネルギーは核酸の構成要素にもなるATPを介して行われる、などの条件が整って行ったと考えられる。また、このような性質を持った有機高分子を含む分子混合物は、生命以前の地球の様々な場所に存在し、互いに反応しながら主に存在持続時間という点から選択が行われたと考えられる(図3)。
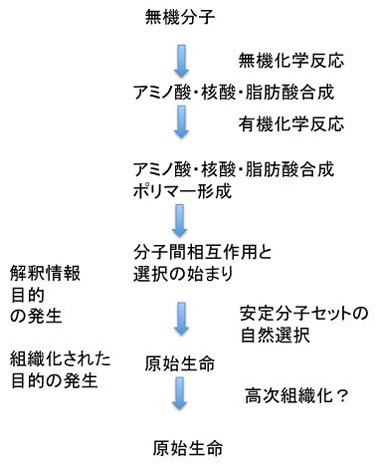
しかしこれだけでは安定な個別の分子セットが選ばれるという過程の繰り返しで、発信できる情報や生物の誕生には至らない。この過程で生まれるのは脂肪酸膜で囲まれた安定で、場合により増幅可能な有機物に過ぎない。中でDNAが複製したとしても、結局は安定な分子の集合でしかない。次の段階に進むためには、有機体(生物)の語源になっている、Organize(組織化)が何らかの目的のために行われる必要がある。この目的こそが、生物が生きるという目的を示すルーツであり、また生命の基本条件になっている。この生きるという目的の一つは、生きるためのエネルギー収支を可能にする分子ネットワークで、これが何よりも最初に必要だとする考えがenergy firstモデルだ。これに対して増える・複製できることがまず必要だとするのがreplication firstモデルだ。次回から順にこの二つの考えについて見ていこう。
[
西川 伸一 ]
熱水噴出孔と生命誕生
2015年11月16日
私たち団塊の世代が生命科学に魅せられた時必ず読めと勧められた本の1冊がシュレジンガーの「生命とは何か?」だ(図1)。
図1 シュレジンガーと著作「生命とは何か?」。版権の関係で私が読んだ岩波の「生命とは何か?」の代わりに英語版を掲載した。
生命は物理化学法則のみが支配する地球で誕生した。当然生命は物理化学法則の延長として理解すべきと考える人も多い。しかし、生命誕生によって情報も含めて地球上に新しい法則が誕生したと思っている者も少なくないと思う。私はその一人だが、そんな私にとってシュレジンガーの「生命とは何か?」は、量子力学者シュレジンガーが生命を物理学者の目で見たとき、生命固有の法則が潜んでいそうな場所を探している本に思えた。本の中で生命固有の課題として強調していたのが、生命体がエントロピーを増大させないよう、エネルギーや有機物を調達する過程と、同じ個体が増殖する過程だった。これを読んで、いずれかの問題を生物学固有の課題として考え研究を志した若者も多かったはずだ(私は途中で挫折したが)。
この分野について最近書かれた本や論文を読むと、生命誕生過程でこの二つの課題のどちらが先に起こったのかについて暑い議論が続いているようだ。もちろん独立した生物が誕生する時には両方が備わっている必要があり、両過程は卵と鶏のように互いに切り離せない。ただ素人の私からみると、生命に必須の有機物がエネルギーとともに形成されないと、最終的に核酸に頼る増殖自体も考えにくいはずで、有機物とエネルギーを合成できるシステムの誕生から考えてもいいのではないだろうか。
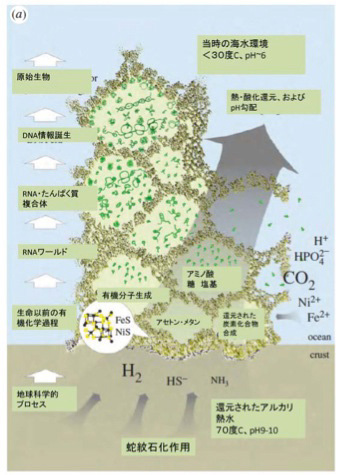
前回述べたが、有機物の合成の可能性については様々な可能性が議論されてきた。この中で、有機物とエネルギーを同時に持続的に生成できる場所として脚光を集めているのが、20世紀後半から相次いで存在が確認されたアルカリ性の熱水を地中深くから噴出している海底熱水噴出孔だ(図2)。この発見によって、生命誕生を有機物とエネルギーから考えるenergy firstの考え方が現在は優勢になっているように私には思える。
前回メタン、水素、炭酸ガス、アンモニアを熱して電気刺激を与えるとアミノ酸が生まれるユーレイとミラーの実験を紹介したが、この条件では持続的にアミノ酸が作り続けられることはない。しかも、できたアミノ酸からさらにポリペプチドを作るとなると、少なくともかなり高い濃度の有機物が持続的に供給される必要がある。反応を偶然の放電に頼るユーレイ・ミラーの条件では到底不可能だ。
ところが、熱水噴出孔には炭酸ガスだけでなく、後に述べる理由で還元力の強い水素も豊富に存在し、これらが反応してメタンやアセトンを持続的に合成することができる条件を備えている。さら地中深くから熱水が噴きあげる間に、は有機物の合成や重合化に必要な触媒となる様々な鉱物が豊富に存在すると考えられる。そして何よりも、一つの熱水噴出口は、少なくとも3万年以上との長い期間熱水を噴出し続けることがわかっており、熱水噴出孔が生命誕生に必要な有機物とエネルギーを持続的に形成できる場所であることは人の素人の私にも十分納得できる。熱水噴出孔の中には数メーターから数十メーターのチムニーという構造を形成して海水から突き出ているものが存在する。これは鍾乳石と同じで、熱水に溶けていた様々な鉱物が海水で冷やされ沈殿することで形成される。すなわちチムニーの存在は、熱水噴出が生命誕生に必要な地質学的時間維持できる可能性を示唆している。また有機物が安定に存在するのが難しい400度近い熱水もチムニーを通る間に冷却され、有機物の合成や持続の可能な温度になる。
これらの結果から、1)豊富な有機物合成の原料、2)熱や化学エネルギー、3)持続性、の点で熱水噴出孔にできたチムニーが、有機物を持続的に供給でき、生命誕生までの長期間の分子選択過程を維持できる、など熱水噴出孔が現在考えうる最適の生命誕生の現場である可能性が強く示唆される。最近、メタンを構成するアイソトープを調べた研究から、熱水噴出孔周辺に存在するメタンの少なくとも一部(1mM)は生物が関与せずに生成されたことも証明され、熱水噴出孔が有機物合成の現場である可能性は高まった。
ではどのように熱水噴出孔で有機物やエネルギーは作られるのだろう。まず炭酸ガスの還元に必要な水素だが、地殻のシリカが水と反応して蛇紋石が形成される過程で水素が発生することが知られている。水素自身はそのままだと拡散してしまうが、チムニー内に形成された鉱物の壁で隔てられた迷路のように入り組んだ小部屋は熱せられた水素を補足する。
次にこの水素により炭酸ガスが還元される過程だが、化学の苦手な私でも、水素と炭酸ガスや重炭酸塩が反応して次の化学反応が進み、
4H2 +CO2 →CH4 +2H2 O2 +2HCO3 +H→CH3 COO+2H2 O
上記のように、メタンやアセトンができることは理解できる。これらの反応が起こると最終的にエネルギーは発生するのだが、反応の開始にはエネルギーを加えることが必要で、反応は自然には起こらない。従って、反応を進めるための触媒が必要になる。
このとき参考になるのが、Autotroph(化学合成独立栄養生物)と呼ばれる、無機物から自分で有機物を合成して生きている細菌類だ。メタンを合成するAutotrophは古細菌に属しており、アセトンを合成するautotrophは真性細菌のClostridiaに属していることから、有機物の原材料としてメタンを選んだか、アセトンを選んだかの偶然が、古細菌と真性細菌の誕生まで変わることなく続いたのは驚きだ。最近になってこのようなAutotrophが有機物を合成する代謝経路についての研究が進み、アセトンやメタンを合成する経路に硫化鉄を持つフェレドキシンが重要な働きを演じていることが明らかになってきた(詳細はCell, 151:1406, 2012:この原稿のほとんどはこの論文を基礎にしている)。すなわちフェロレドキシンに含まれる鉄を媒介に水素の電子を炭酸ガスに移転させる反応で、これにより炭酸ガスの還元が自発的に進行する。この結果細菌では、アセトンやメタンをATPと共に合成することができる。このフェレドキシンを媒介とする炭酸ガスの還元反応の最初に必要な自由エネルギーはアルカリになるほど低下することから、高いpHほど反応が起こりやすい。
このフェレドキシンが媒介する電子の転移をすすめる主役は鉄イオンであることから、同じ反応をチムニーに豊富に沈殿している鉄イオンで媒介できる可能性がある。アルカリ熱水噴出孔のpHは高く、水素による炭酸ガスの還元反応は起こりやすくなっているところに、フェレドキシンにも含まれる硫化鉄や硫化ニッケルが電子の転移の仲立ちをすることで、細菌で起こっている有機物合成がチムニーの中で起こるとするシナリオだ(図3)。
図3チムニー内にできた小胞内で有機物が合成される。
また細菌が炭酸ガスからフォルムアミドを合成するのに使っているモリブデンイオンも存在しており、有機物合成に必要なすべての原料が、細菌と同じようにチムニーの中で作ることができる。残念ながらこれを証明する実験はまだ行われていないが、理論的には可能だと考えられている。先に述べたように、熱水孔の周りには生物の助けなしに合成されたと考えられる1mM程度のメタンが存在していることを考えると、実験室で再現されるのも時間の問題ではないだろうか。
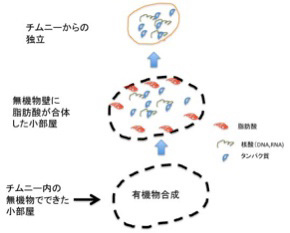
あとはチムニー内にできた迷路のような小胞の隔壁に存在する様々な鉱物の触媒活性を使って、アミノ酸、核酸、脂肪酸ができ始める。さらに、チムニー内に形成される熱勾配により温度拡散が誘導され、有機物が濃縮された小胞が生まれる。この中で、前回紹介したような反応が起こって有機物の重合化が起こり、鉱物膜と脂肪膜が複合した高い濃度の有機物が詰まった独立栄養系の小胞ができる。全くの素人の私にとっても、このシナリオは理解しやすく、実際に起こっているという確信を持つ。
こうして出来上がった鉱物と脂肪酸の膜で仕切られた小胞には高い濃度の様々な有機物が詰まっているが、ここまでは完全に物理化学の法則のみで進む点が重要だ。すなわち生命誕生のプロセスはここから始まる。次回はこの無機物と合体した中間段階が、チムニーからどう独立できるのか(図4)考えてみよう。
[
西川 伸一 ]
分子進化をダーウィンの進化論に当てはめる
2015年12月1日
生命誕生を考えるとき、前回述べた 熱水噴出孔に形成される泡のような小胞ほどよくできた偶然はないように思う。うまい具合に大きさも細胞に近く、小孔で他の小胞や外界ともつながっているし、原理的にアミノ酸、核酸、脂肪酸、ペプチド、ヌクレオチドなどを持続的に合成する条件も整っている。さらに、アセテートやメタンの合成過程でエネルギーを発生させることができ、熱勾配やpH勾配のおかげで高分子を特定のコンパートメントに濃縮することもできる。
ただ、どんなに細胞に似ていても、これは生命ではない。チムニー内の小胞では、熱力学平衡に対抗するため、不断にエネルギーを外界から導入して(ここではH2勾配、CO2の還元反応、熱などがこれに相当する)熱力学的平衡から離れた状態を維持できる開放系、すなわちイリヤ・プリゴジンが散逸構造 と名付けた非平衡状態が実現できている。しかも、この状態を何万年にもわたり維持することができる。しかし、ここで起きていることの全ては生命誕生に必要な条件ではあっても、生物特有の性質とは無関係だ。非平衡の熱力学系ができただけで、生命誕生までにはまだまだ大きなギャップが存在している。一般的に創発と呼ばれてきた質的な転換が必要で、まずこのギャップで何が起こったのか大きな枠組みを考える必要がある(図1)
前にも述べたが 、英語では生命をOrganismと表し、生物が「組織化されている」ことを強調する。これはフランス語(Organisme)、イタリア語・ラテン語の(Organismo)も同じだ。ところが日本語やドイツ語では「生物」(Lebenswesen)と表すため、有機化学と生命誕生の間に横たわるギャップの本体が、「組織化される」過程であることを、いまひとつ実感しにくい。18世紀、デカルトの機械論では生命を理解できないと反旗を翻した自然史運動の中心ビュフォンを代表とする先人たちが目指したのが有機体論だったことを思い起こそう。その後、生物が組織化された存在だという特徴は、生物には「自然目的」が内在しているように見えるという特徴へと読み替えられ、19世紀生物学の重要なテーマとしてダーウィン進化論の誕生まで受け継がれていく。
組織化するメカニズムはそのまま訳すとオーガナイザーであり、シュペーマンが使用して以来、発生学で頻繁に用いられる用語だ。分子を生命へと組織化するという、実際には何も理解できていないメカニズムをとりあえず生命のオーガナイザーと呼んでおこう。もちろんこの本体については全く分かっていないことから、ここではオーガナイザーという言葉を、この過程を理解できていないことを表す目印として使う。と言うのも、間違うとオーガナイザーという概念は、神を始めとする超越的力による組織化と結びつけられる危険がある。事実、ダーウィン以前の生物学では、オーガナイザーとは確実に神の持つ超越的力のあらわれと考えられていたし、ダーウィン以後も「エラン・ビタール(生命力)」などの超越的力は、繰り返しオーガナイザーと結びつけられてきた。これはオーガナイザーという言葉自体に、最終目的を知り、そのために部分を組織化する主体という意味が付きまとうからだ。オーガナイザーと表現したときは、常にわかっていないことの印であることを思い起こし、超越的説明を導入しないように気をつけながら進む必要がある。
オーガナイザーを理解するため、過去の生物学の歴史にもう一度目を移してみよう。18世紀生命を組織化するオーガナイザーは、生命の「自然目的」と読み換えられていたが、この自然目的を科学的に初めて説明したのがダーウィンの進化論だった。重要なことは、進化論が超越論的説明を完全に排除してこの自然目的を説明している点だ。従って生命誕生までのオーガナイザーを考える時、ダーウィンの進化論は大いに参考になる。
ではダーウィンの進化論は生物の持つ「自然目的」をどう説明しているだろう?この説では、目的を実現すべく進化したように見える種(例えば高い木の実を食べる為に首が長くなったキリン)も、最初から小さな違いが集まった集団の中の多様性として存在し、この小さな差が他の個体と比べた特定の環境下での生殖(増殖)優位性により自然選択されただけだと説明する。すなわち、進化では目的として提示される結果が最初から存在していたという逆転の発想だ。
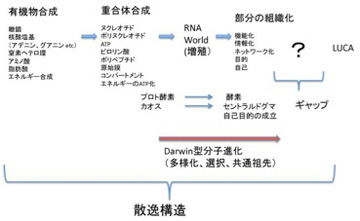
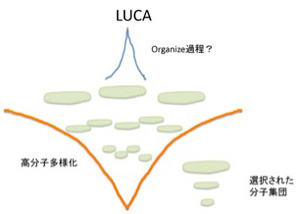
次回以降順に取り上げるが、ダーウィンの扱った生命誕生以後の進化と、それ以前の分子進化には様々な違いが存在する。しかし、結果が先に多様性として存在し、それが選択されるという図式は分子進化にも当てはめられるのではと考えている。すなわち、生命誕生と非平衡熱力学系の間に、無数の中間状態(分子の種類とそれらの関係性)が存在し、多様な分子の集まったカオス状態の中から、特定の中間状態が選ばれる過程が繰り返されるうちに、最後に全生物に共通の祖先(LUCA)が誕生すると考えることができる。
この分子進化のダーウィン的理解に必要なのは、1)誕生までに発生した中間段階、2)生命誕生に至るまでに必要な分子や中間段階多様性を発生させる力、そして3)分子から生命への過程に働く自然選択力になる。今回からこの3つの問題を順に考えて行く。
ダーウィンの進化論では共通祖先の概念は、出し手のいない情報を扱うための素晴らしいアイデアになっている(これについても次回以降議論する)。このおかげで、現存の生物を単一の原始細胞まで遡って構想することが可能になる。同じように分子進化でも、単純な構造(例えばディペプチドやディヌクレオチド)から複雑な構造へと分子進化が起こり、最終的にLUCAに集まったのだろうと推察はできる。もっとも単純な有機体をメタンとアセトンとすると、知る必要があるのは、このもっとも単純な有機体構造から合成されてきた、自立生命を支えるために必要なミニマムな分子の構造リストだろう。
進化論では、生物の複雑化を示す中間段階の証拠として化石の存在が指摘されている。しかし残念ながら、化石に相当する中間段階の遺物は、38億年前に起こった生命誕生までの過程を示すほど多くは残っていないだろう。再現できず、記録もない過去の分子を研究するには、現存する分子を基礎にして過去の分子を推論するための方法が必要になる。現在この目的で広く行われているのが、DNAの配列の差に基づいて系統関係を推定し、その共通祖先を推定する分子系統学だ。しかし、DNA情報が成立していない生命誕生前にはこの手法は役立たない。生命誕生までに生まれた中間状態や、分子構造の複雑化について考える分子進化は、有機分子の構造だけを指標として進化を考える必要がある。ゲノム配列を使うことに慣れた私たちには大変に思えるが、例えばダーウィンの進化論は、形態の観察だけから生まれてきたことを考えると、できない話ではない。
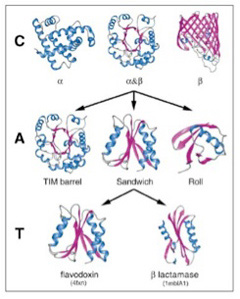
幸い構造解析の終わったタンパク質はすでに10万を突破している。アミノ酸配列からタンパク質の構造を自動的に予測することはまだ難しいため、タンパク質をその形態から分類しようとCATHと呼ばれる分類が1993年より行われている(図2)。
Orengo et
al, Nucl. Acids Res. (1999) 27 (1): 275-279.より転載 )
この方法では、タンパク質をClass,(類) Architecture(構築), Topology(接続形態)、そしてhomologous superfamily(相同スーパーファミリー)に階層化している。全てのタンパク質は、αヘリックス類、βシート類、そして両方が合わさったαβ類に分けられる。この3類がそれぞれ多様な変容を遂げることで異なる形態を持つ構造が生まれる。タンパク質の複雑化が進むと、同じ類に属していても、形が大きく違った構築を作ることができる。これがarchitectureだが、図1ではαβ類から派生しうる3種類のarchitectureが示されている。こうしてクラスより複雑な構造の多様なarchitectureを一定数抽出することができる。
Bukhari and Caetano-Anolles, Plos Computational Biology,
9:e1003009, 2013より転載 )
図3は、Caetano-Anollesらが、構造の決定されたタンパク質からarchitectureを抽出して系統関係を調べた図だが、重要なことはほとんどのarchitectureが古細菌、原核生物、真核生物のすべてに存在することだ。すなわち、このような構造リストは、生命誕生に必要なミニマム分子のリストに近いと考えられる。一方、様々なarchitectureが結合したtopology, homologous
superfamilyなどのより高次な構造になると、存在する生物は徐々に限られていく。
このように、タンパク質やRNAの構造の階層性、細胞内での機能、そしてアミノ酸配列総合して進化過程を記述しようとするCaetano-Anollesらの努力は、生命誕生後の進化を新しい観点から見るだけにとどまらず、例えばATP合成や、アミノアシルtRNA合成酵素のような生命の基本に関わる酵素のもっとも単純な構造を推定する方法になる可能性がある。
もちろんこのもっとも単純な機能タンパクリストが完成しているわけではないが、次回からは、LUCAに集まったこの分子群のリストが完成したと仮定して、分子多様性を生み出す力、generator of diversity (GOD)について考えたいと思う。
[
西川 伸一 ]
生命誕生までのダーウィン進化
2015年12月15日
前回 、生命の共通祖先(LUCA:Last universal
common ancestor)に存在すると想像される有機分子や、これら分子の祖先と考えられる様々な中間段階を、現存の生物に存在するたんぱく質やRNAの構造から推測する可能性について議論した。生命誕生までに起こった出来事の痕跡が残っていない限り、何が起こったかは現存のタンパク質から推測するしかない。もし高い確度を持つ推測方法が確立すれば、その推測に基づいて分子を再現すること自体は難しいことではない。こうして合成した有機分子の性質を調べ、最終的には生命を作り出すこともいつかは可能になるだろう。しかし、可能性としてリストされる個々の分子を実験的に検証するためには、途方もない努力と時間が必要だろう。まして、それを集めて生命を再構築することは21世紀中に出るかどうかまだわからない。だが、詳細を理解することは難しくとも、LUCAまでの道筋はぼんやりと頭に浮かぶようになってきている。
最も重要な仮定は、LUCAができる過程もダーウィン進化の法則に従うという仮定だ。他の可能性もあるかもしれないが、私にはこれ以外のアイデアはない。この過程をダーウィン進化的に述べるなら、単純な有機物から多様で複雑な中間有機物が無作為かつ連続的に生まれ(多様性の獲得)、その中から分子自体の安定性、他の分子との相互作用による安定化などによる選択が行われ(自然選択)、より安定な分子や組み合わせが選択されるといえる。この分子進化過程は、多くの偶然に左右され正確な予測はもちろんできない。しかし、基本的には熱力学的法則に従って、一種のカオスが形成される過程だと考えている。もちろん単純なカオスは生命ではない。同じ空間に共存している様々なカオス状態同士がランダムに反応し合っているうちに、次により複雑で大きなカオス状態ができる(星雲の衝突のようなイメージ参照:図1)。これが繰り返される中で、それまでにはなかった秩序が組織化されるとLUCAが生じる。
図1 双極星雲:星雲は異種のカオスだが、これが衝突して新しい一つのカオスを形成する。(写真はWikiコモンズより)
すなわち、幾つかのカオスが、力学とは別の新しいルールでOrganizeされ、これまでのカオスとは質的に異なる秩序で支配されるLUCAが生まれる。多様化と自然選択というダーウィン進化論の共通ルールは、カオスからLUCAへの過程、生命誕生後の進化過程の両方に存在しているが、両者には多くの違いがある。LUCA誕生過程を思い描くためには、この違いをしっかり理解しておくことが重要だ。
まずLUCAが誕生するまでの中間段階は、同じように自然選択されて誕生すると言っても、熱力学的法則に完全に従うカオスに過ぎない。一方、生命誕生後に生起する中間段階は、熱力学第二法則に逆らって独立した系を維持しながら増殖する生物特有のOrganizeされているという性質が最初から維持される。生命誕生後の進化ではDNAが本来持つ変異しやすいという化学的性質が、集団の多様性獲得の原動力だが、一方、生命誕生前は、多様な分子を連続的に供給する化学的仕組みが必要になる。
次に、進化の結果は生命誕生前と、誕生後では全く反対に見える。もし数少ないLUCAから生物が進化しているとすると、
LUCA誕生までの過程はLUCAへと収束する過程のように見える。一方、生命誕生後はもっぱら多様化が進んでいるように見える。図2は、生命誌研究館のシンボルとも言える生命誌絵巻だが、この扇の形は、まさにLUCA誕生後の進化過程で生物の多様化が起こっていることを表している。このことから、進化過程を洒落て、Generator of Diversity (GOD)と呼んでいる研究者もいるぐらいだ。
詳細はこちら
実は、個体の多様化と自然選択の組み合わせでなぜ多様な種が生まれるのかについては、完全に理解できているわけではない。ただ、生命誕生後の多様性を生み出す原動力GODは、ゲノムの物質的基盤であるDNA鎖がもともと変異しやすいという物理化学的性質を持つことに起因している。おそらく祖先となる集団(共通祖先)の多様性は常に十分大きい(多様な形質をとれる)おかげで、環境により複数の形質が選択され共存するうちに種の多様化が進むのだろう(これについては生命誕生後のゲノム発生学でもう一度詳しく扱う)。生物が住める環境が通常高い許容性を持っていることが種の多様化に重要だが、寒冷化や隕石衝突のような大きな環境変化がおこると種は絶滅し多様性は減少する。
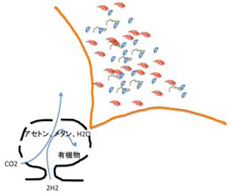
先に述べたように、一見すると生命誕生前の進化は一つあるいは少数のLUCA誕生へ向かって収束していくように見える。しかし、例えば結晶ができるように無機分子が臨界に達して一足飛びに生命が生まれるとは考えにくい。従って、生命誕生までには、比較的安定な中間段階として、多様な有機分子や分子複合体が合成される必要がある。それも、LUCAに近づくにつれ、比較的単純で多様な中間段階段階から、より複雑な中間段階が段階的に生まれていくと考えられる(図3)。こうしてできる多様で複雑化した分子集団の中から少数が選ばれ、さらに新しい秩序が生まれるよう組織化されるのがLUCAではないだろうか。従って、過程全体で見ると起こっていることは収束ではなく、進化と同じで多様化だ。ただ、強い選択圧の結果LUCAとして残るのは数少なく、収束しているように見えることになる。
最終的にLUCAが完成するにはどれほどの分子や分子ネットワークが必要か想像するしかないが、自立生命が可能になるには最低限100−300余りのタンパク質と機能的RNAが存在すればいいと想定されている。ただ、最初から無駄のない構造ができるはずはないので、おそらくこれよりはだいぶ多い分子の種類がLUCAに存在したと思える。ここでは、タンパク質とRNAを合わせて仮に500としておこう。実際には、これが100個であれ、1000個であれあまり違いはない。
ではこの500個の分子はどうすればできるのだろう?RNAについては後にRNAワールド仮説を考えるときに議論するとして、ここでは話を500種類のタンパク質を第43話 で述べた熱水噴出孔で合成するという課題にしておこう。もちろん設計図などないから、ランダムな化学反応でアミノ酸が合成され、こうして合成されたアミノ酸からやはりランダムな化学反応でペプチドが合成される過程がどう進むかという課題と考えてもらっていい。
全ての有機合成が、炭酸ガスと水素から、メタンやアセトンが合成されるところから始まることを見たが、そこに窒素も加わって、様々なアミノ酸が合成できることは示されている。熱水噴出孔には触媒とエネルギーが十分存在するため、この場所ではアミノ酸から少なくとも50merのペプチドまで理論的に合成できる。この過程を図示すると、生命誌絵巻と同じで、メタンとアセトンという単純な有機物から最初始まり、時間とともに有機物の多様化が進む過程として描ける(図4)。
図4:熱水噴出孔に存在するアセトン、メタン、エネルギーを持続的に合成する力は、有機高分子の多様化のGenerator of Diversity (GOD)といえる。
このことから、LUCAへの過程も生命誕生後の進化と同じで、多様化の方向に進み、これを推進する力の基盤が、熱水噴出孔での持続的エネルギーと有機物が供給であると考えていい。最初はアセトンとメタンの2種類しかない状態が、アミノ酸になると20種類と10倍に多様化する。そしてペプチドになると、結合するアミノ酸の数に応じて多様性は指数的に増大し、もし熱水噴出孔で50merまでのペプチドが作れるなら、その多様性は20の50乗という天文学的数字になる。さらに、できた様々な長さのペプチド同士が相互作用しあって、複合体を作ることで、この多様性はさらに増大する。これは、DNAの長さが増えるごとに、それが形成できる多様性が増大するのと同じだ。このように、熱水噴出孔のような条件が整えば、GODによる有機分子の多様化を持続的に進めることができる。今後、GODが整った実験条件を工夫し、無機物から多様な有機物へと進む多様化過程を実験的に再現することは可能になるだろうと思っている。
ただ、多様化が起こったとしても、天文学的種類のペプチドが合成されるだけで何も起こらない。LUCAへと組織化されるためには、まずGODの力を何らかの形で制約することが必要だ(散逸構造の一つ翼の後ろに発生する乱気流が翼という制約により発生するのと原理的には同じだ。:図5)。
図5:散逸構造は流れのエネルギーが翼という障害物で制約されることで初めて生じる。多様化というエントロピーの流れも同じ。(写真はWikiコモンズより)
生命誕生後のダーウィン進化でも同じで、ゲノムで進むランダムな多様化を、それまでの進化の結果、課せられた生存のためのコンテクスト(それを満たせない変異が起こると個体は死ぬ)と環境への適合により2重に制約する(選択する)ことで、新しい種が生まれると説明している。
生命誕生までの過程で、熱水噴出孔に存在して、そこで発生する有機分子を多様化させる力、すなわちGODを制約する要因がOrganizerとして生命誕生を媒介したはずで、生命誕生過程を構想する鍵は、この制約要因を理解できるかどうかにかかっていると思う。もちろん理解できているというには程遠いが、熱水噴出孔にできたチムニー内に生命誕生場所を限ることができれば、実際の制約条件を特定できるのではと考えている。次回は、この制約条件を考えるときに考慮すべき幾つかの点について述べていく。
[
西川 伸一 ]
生命誕生の力学
2016年1月5日
自分で読み直しても前回の話はわかりにくかったと反省する。無生物から生物へのダーウィン進化についての思いつきを羅列しただけで、背景にある考えをよく説明できていないことが問題だった。熱水噴出孔の化学反応が原動力となって、多様な有機分子が発生する点についてはわかってもらえたと思うが、この多様化へ向かうエネルギーと物質の流れが制約されることで新しい秩序が生まれるという点については、もう少し説明が必要だろう。
有機分子やエネルギーの流れを初めから考えると複雑でわかりにくいので、ここは熱水噴出孔を一度忘れて、まず多様化と制約の一般的な関係について、もう少し簡単な系をモデルに説明してみよう。
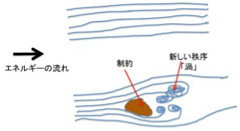
高いところにある水は必ず低い方に流れるのと同じで、平衡に達していない状態は熱力学第二法則に従って平衡に達するまで変化を続ける。もし摩擦のない理想状態が存在すれば、この変化は川の流れと同じで、一方向に均一に流れ、新しい秩序が生まれることはない(図1上)。この流れの中央に岩のような障害物を置くと、川の流れはそれにより制約される。この結果、十分なエネルギーが供給され続ければ(川が流れ続ければ)、岩の後ろに渦という新しい構造が生ずる(図1下)。
図1 力学的エネルギーの流れが制約された時に初めて新しい秩序が生まれる。
この渦を構成する水分子を見てみると、細胞の構成成分が刻々変化するのと同じで、常に置き換わっている。しかし分子が変わっても渦の構造は、流れのエネルギーが持続的に供給される限り維持され、流れが止まると消失する。これは散逸構造の一つと呼んでいいだろう。この例では、外部の障害物がエネルギーの流れを制約しているが、制約は外部から与えられる必要はない。散逸構造として最も有名なベルナール・セル(図2)は、液体の入った容器を下から均一に熱を加えたとき、入ってきた熱エネルギーを効率よく上部へ散逸させようとして溶液中にカラム状の対流が生じて、このカラムが容器の上に美しい6角形模様として現れる現象を指す。
この場合の制約は液体の粘度や比重などの性質や、溶液の量といった初期条件と言える。他にも、2種類の異なる溶液を混ぜるとき、両者が一定の法則に従って反応しあうように制約を与えると、本来なら平衡状態へと均一に混じり会おうとする2種類の液体が、周期性を持って容器内に美しい模様を描くジャポチンスキー反応がある。
図3 ジャポチンスキー反応の一例。原理は省くが、硫酸性クエン酸、臭素酸カリウム、硫酸セリウム、およびマロン酸を反応させると容器中の4価と3価のセリウム塩濃度が容器中で振動することをジャポチンスキーは発見する。溶液内の成分の反応性が制約となって、新しい秩序が生まれる好例と言える。(画像引用:https://www.flickr.com/photos/nonlin/4013035510 )
図3はジャポチンスキー反応の例で、反応し合うという内的な制約だけで、これほど秩序だった模様が現れる。以上のことから、変化を続ける力学(熱力学)系に制約を加えることで新しい秩序が生まれるというイメージが理解していただけたのではないだろうか。
では熱水噴出孔での有機物生産の現場にはどのような制約が存在しているのか考えてみよう。また、この現場でダーウィン進化の選択圧となって生命に必要な分子を選択する条件も考える必要がある。ベルナール・セルやジャボチンスキー反応で生まれる構造はどんなに美しくとも、初期条件で決められた反応で、生物構造に見られる機能や目的があるわけではない。これは、自然目的が発生するために必須の、環境による選択を受けていないからだ。以上のことを念頭において、熱水噴出孔で何が起こりうるのか考えてみよう。
繰り返すが、生命が成立するためには、まず物質とエネルギーが持続的に供給される系が成立する必要がある。このような系が、水素イオンの多いアルカリ条件の熱水噴出孔には成立しているという説は説得力が高く、私もこの考えに基づいて考えている。アルカリ熱水噴出口には、炭酸ガス、水素、窒素、熱、そして反応を媒介する無機触媒が万年単位のスケールで存在し続ける。この条件がエネルギーと有機物を連続的に生成されることは化学的に不思議なことではない。この持続的Generator of
Diversity (GOD)により平衡から離れた状態が維持されるが、そこで発生し散逸する物質とエネルギーの流れは、そのままだと海の中へ放出され拡散するだけだ。生命誕生の条件が整えるためには、この流れを制約する必要がある。熱水噴出孔で新しい秩序をもたらすことのできる制約の可能性をリストアップしてみよう。
熱水噴出孔から独立栄養の原始生命が生まれるまでの過程について豊富なアイデアを提案し続けているWF MartinとN.Laneの説は私のような素人にも説得力が高く、ここで展開している考えも彼らの説が核になっている。このエネルギーと物質の流れに新しい秩序を与える外的な制約として最も大事だと彼らが考えているのが、チムニー内に無数にできた、バブル状のマイクロセルだ。
http://dx.doi.org/10.1098/rstb.2013.0088 :を改変)
これらのマイクロセルは大きさも様々で普通の細胞と同じ大きさを持つ場合も存在すると想定される。セル同士はさらに小さな孔でつながっており、生物の細胞のように独立しているわけではない。また、壁も最初は無機物からできており、その成分により有機物合成の触媒として働く。
このセルはエネルギーと分子の流れを生み出す反応容器としてまず働くが、川の流れの中の石と同じで、発生するエネギーと物質の流れの外的制約として働く。例えばフルイの役目をして、大きな分子を引き留める。これと並行して、pH、酸化還元能、そして熱の勾配もできてきた分子の制約要因として働き、熱水噴出孔のそれぞれの小部屋に存在する分子構成は、自然に不均質で多様になる。
ジャポチンスキー反応と同じで、メタン、アセトン、アンモニア、硫化水素などの成分が反応し合う法則も制約になる。加えて重要なのは、ジャポチンスキー反応と異なり、一旦合成された分子が新しくできる分子を制約する点だ。例えば現在の生物が持つアミノ酸が全てL型であるのも、炭酸ガスと水素を原料としてメタンとアセトンを合成することができるのに、メタン型とアセトン型の細菌がどちらかに収束しているも初期の制約でその後の過程が決まってしまった例だ。すなわち、小さな差でも一旦生まれると、それが増幅され維持されることで、バタフライ効果(蝶の小さな羽ばたきが最終的に大きな変化を生み出すというカオス理論)と呼ばれるものだ。
この反応の結果として生まれる制約は有機高分子になるとさらに複雑になる。例えば脂肪酸のシートができると、疎水性の面が形成される。この近傍では水が除外されるため、ペプチドが濃縮され、熱力学的に起こりにくい反応が進むようになる。また、ペプチドも水がないと分解されにくくなる。そしてすでに42話 で述べたが、脂肪酸の中には核酸の重合を促進し、DNAの場合は複製酵素の役割を演じるものすら存在する。
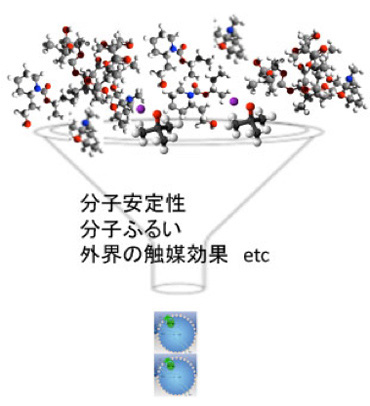
このように、無機化学反応と比べると(例えば水素と酸素が反応して水になる)、有機化学反応は多様で、ランダムで、予想不可能だ。これは、反応自体が新しい制約要因を発生させるという、自己回帰的構造を持っているからだ。結論的に言ってしまうと、熱水噴出孔のマイクロセルでは厖大な種類の有機物の合成可能性が存在している空間ということになる。
最後に、熱水噴出孔に生まれる制約の特徴を列挙しておくと、
1) 外的に与えられる無機的制約(例えばマイクロチェンバー、pH,熱勾配など)と、エネルギーと物質の流れ自体から自己再帰的に発生する有機的制約が複合している。 2) 外的に与えられる制約は決定論的で、有機的制約は非決定論的。 3) 外的制約は長期的に維持されるが、有機的制約は短期間しか存在しない。 4) 有機的制約は、反応自体から生まれる自己再帰的な制約で、常に多様化し、複雑化する 5) 偶然生まれる小さな差が、その後の全ての反応の基盤になるようなバタフライ効果を示し得る などをあげることができる。
最後にもう一度渦と生命誕生過程を比較して終わろう。渦の持続時間は通常短い。しかし、複雑な地形では、突然持続時間の長い渦が生まれる。もし外的な地形が変わらないとすると、渦が渦を呼び、その渦の中から安定に渦が持続する条件が生まれた結果だ。
熱水噴出孔に生まれる制約とその結果生まれる新しい秩序も安定性に大きな差が生まれる。これがダーウィン進化の自然選択に対応する。次回は生命発生に必要な状態が選択される過程について考えてみよう。
[
西川 伸一 ]
システム化学
2016年1月15日
ここまでの話をもう一度ざっとまとめると、次のようになる。
熱水噴出孔ではエネルギーと炭酸ガス、水素、水など無機分子の持続的な流れが発生している。この流れはそのままだと、海水へと放出されるだけだが、噴出孔のマイクロチェンバーにより様々な形で外的に制約されると、有機分子の生成が始まる。最初の有機物はアセトンやメタンだが、マイクロセルの成分に含まれる様々な金属の触媒が作用すると、さらに複雑で多様な有機物が合成される。例えば以前紹介したように(第42回ゲノムの発生学II )、モンモリロン石が存在すればアミノ酸や核酸の重合が進む。脂肪酸が選択的に合成されるマイクロセルも存在するはずだ。たまたま存在した様々な外的制約により、分子やエネルギー分布の不均一化、構造化がおこる。
このようにマイクロセル内で進む有機分子の持続的な合成の流れを用いて、さらに複雑な有機高分子の合成が始まるが、ここまでのほぼ全ての過程はマイクロセルによる制約があれば進む。こうしてできた様々な分子(低分子から高分子まで)は独立したまま存在していることもあるが、高分子になるほど低いアフィニティーであっても他の分子と相互作用する確率が高まる。すなわち、合成されてきた分子自体が他の分子と反応する能力が新しい制約として働き出す。システムの中で生まれた新しい分子が、システムを新たに制約する「再帰的」制約の発生だ。
この「内的に発生する再帰的制約」について、これまでも具体的例を紹介してきた。例えば、現存するAutotroph細菌を見ると、アセトンを原料にするのは真正細菌のclostridia、メタンを原料にするのは古細菌と完全に分かれ、逆はない(第43回熱水噴出孔と生命誕生 )。即ち、最初に合成された成分が制約要因としてLUCA発生から現在まで、持続的制約としてAutotrophで働き続けていることを意味する。他にも脂肪酸の中には核酸の重合や複製を触媒する能力がある分子が存在することを紹介したが(第42回ゲノムの発生学II )、これも内的に生まれた分子が、システムの新たな制約要因として働き、それ以前には存在しなかった新しい分子を作り出す分子進化の例といえるだろう。
この内的に生まれた制約による新しい状態の誕生は、制約要因が最初のシステムには全く存在しなかったという点で、反応する溶液同士を混ぜ合わせた系でおこる振動、ジャボチンスキー反応とは違う。システム内で発生した分子が制約となって、それまでとは異なる秩序が生まれるのが「内的に発生する再帰的制約」だ。
これは机上の空論だと思われるかもしれないが、応用有機化学分野のひとつ、コンビナトリアル化学では同じような課題が現実に研究されている。コンビナトリアル化学とは、例えば創薬のための候補化合物を、単純な分子から一挙に作ってしまおうという技術で、様々な化学工業で利用され始めている。従来多数の化合物を得るためには、自然に存在する生物を集め、そこから化合物ライブラリーを調整するのが普通だったが、コンビナトリアル合成のおかげで、生物に頼らず試験管の中だけで多様な化合物を合成することが可能になっている。
オランダのOttoらの総説(Li et al,
J.American Chemical Society, 135:9222, 2013)は、この技術により単純な有機化合物からこれまで存在しなかった様々な新しい機能を持つ化合物が合成できることを教えてくれる(図1)。総説の内容を詳しく紹介するのは控えるが、単純な有機化合物がコンビナトリアル合成により、無限の可能性を拓くことがよくわかる。
図1 コンビナトリアルケミストリーの可能性を述べたOttoらの総説の内容を図示した。有機分子が反応を続けることで様々な複雑な高分子を合成できることを示している。
中でも私の興味を引いたのが、コンビナトリアル化学から自己複製する分子構造(複製子)が生成される可能性だ。この複製子について、この総説の著者であるオランダのSijbren Ottoのグループが昨年Nature
Communicationsに発表した論文(Colomb-Delsuc M et al, 6: 7427, 2015 Creative Commons)に基づいて紹介しよう。
まずこの実験では、グリシン・ロイシン・リジン・フェニルアラニン・リジンの疎水性と親水性のアミノ酸が互い違いに繰り返すペプチドが、互いに可逆的共有結合を形成できる(SS結合)SH基を2つ持つベンゼン環に結合したオリゴペプチドが使われた(図2)
このオリゴペプチドはベンゼン環部分に2つあるSH基を介して他の分子と反応し、図3に示すような1merから7merの重合体を形成し、最終的な平衡状態に達すると予想される(図3)。
図3:図2に示したオリゴペプチド同士の反応から予想される分子同士の結合反応。相互に反応するベンゼン核のみを示している。
実際には7merは合成されなかったようだが、攪拌を続けると、4日目ぐらいまでに1mer,2mer,3mer,4mer,そして6merが混ざった平衡状態が生まれる(図4)。ところが、1週間を過ぎた頃から急速に他の重合体は失われ、6merが全体の90%を占めるようになる。
図4:16日間攪拌を続けた間に溶液中に存在する各重合体の比の変化。
なぜ最初の平衡が破れたのかを調べると、6merの大きさの重合体だけが、今度は縦に重なって、さらに大きな重合体を形成していることが明らかになった(図5)。即ち、6merだけが縦に重なって成長する能力をたまたま持っていたため、一旦この6merが発生すると、それが核となって、6merが重合した高次構造がうまれる。この高次構造は成長に伴い、溶液中から6merは隔離するため、平衡状態が壊れる。その結果、溶液中には6mer由来の巨大分子だけが残される。
この一連の反応は、6merという構造単位の発生が新たな制約になり、これまでとは全く異なる高次構造を形成することが現実に起こりうることを示している。面白いことに、6merが縦に重なった重合体は、一定の大きさに達すると、攪拌のストレスにより、自然にちぎれる。もし6merが持続的に供給されれば、ちぎれた部分がもう一度核になって、同じ大きさを持った重合物が再形成される。この意味で、この分子構造は複製能力を持っていると言える。
このような重合による高分子形成は、ウイルス被膜や、細胞外マトリックス形成など、生命過程では普通に見られる自己組織化反応だが、全く人工的な反応として取り出してみると、生命と共通の幾つかの性質が生まれていることに気づくことができる。
1) 核酸情報は持たないが、特定の構造の複製が可能なこと。 2) 複製のためには、外界から部分が常に供給される必要があること(同化)。 3) 部分を構成する分子組成は全く同じでも、重合することで外界とは隔離された系(すなわち自己)が形成されていること。 4) 同じものを作るためには情報が必要なこと。ただこの場合の複製に必要な情報は、外界のストレスと、構成分子の性質(この場合は6merしか受け入れない科学的性質と、割れるまでの構造の強度)として提示されている。 これを流れの中の渦に例えると、力と水分子の定常的な供給が続く、流れの中に同じ大きさと形をした渦が増え続けるのと同じことだ。
先週Ottoたちはこの構造にグリシン・ロイシン・リジン・セリン・リジンを持つオリゴペプチドも同化できることを発見し、両方のオリゴペプチドが存在する溶液では多様な構造体が生まれることを示した(Sadownik et al, Nature Chemistryオンライン版)。この結果は、この分子構造が上の4つの性質に加えて、進化するという5番目の生命と共通の性質を持ちうることを示している。もちろん多様化だけでは進化は起こらず、特定の形質が選択されることが必要だが、このモデル系は、自然選択による進化とは何かのヒント教えてくれそうだ。
コンビナトリアル化学では最初の反応条件は人間が決める。熱水噴出孔で初期条件を決めているのは偶然だが、様々なオリゴペプチドが形成されることは既に確認されており、Ottoたちが観察したのと同じことが起こって何の不思議はない。次に、Ottoたちの研究から生命と共通するどんな性質が生まれてくるのか楽しみだ。
Otto等の研究を詳しく紹介してすこし長くなったので、今回はここまでで終わる。次回はDeaconの説を紹介しながら、生命に共通の性質の発生のためのルールについてさらに考えてみたいと思っている。
[
西川 伸一 ]
生命誕生を考える理論的枠組み: Deacon と Teleodynamics
2016年2月1日
これまで生命誕生までに必要だと思われた過程を、なるべく具体的な例を参照しながらたどってきた。しかしここで紹介できた熱水噴出孔での化学合成過程は、生命誕生までのほんの一端に過ぎず、実際にはほぼ無数の過程がLUCA誕生に必要だったはずだ。とすると、生命に必要な様々なサブシステムが形成され、互いに連結され、LUCAの中に埋め込まれるすべての過程を洗い出すのはまず不可能だ。代わりに、この過程の背景にある一般的ルールを見つけて、より抽象的に、法則に基づいて生命誕生を理解しようとする人たちがいる。
例えばカウフマンの自己組織化理論(S.Kauffman著、米沢富美子訳「自己組織化と進化の論理—宇宙を貫く複雑系の法則」ちくま学芸文庫)、あるいはアイゲンらのハイパーサイクル理論( M.Eigen & P Schuster, The hypercycle, Die
Naturwissenschaften 65:341, 1978 )もこの方向を代表する例だ。しかしこれらは生物の一部の性質を言いえているとはいえ、私たちが頭の中に描いている生物にはあまりに距離がある様に思える。
生命誕生の背景にある理論の中で、少なくとも私にとってもっとも説得力のある理論的枠組みを提供しているのがTerrence Deaconだ。今回は、彼が2006年にClayton & Davies(編)「The re-emergence
of emergence:The emergentist hypothesis from science to religion」に寄稿した総説論文「Emergence:The Hole at the wheel’s hub」(http://72.52.202.216/~fenderse/Hub.htm で読むことができる)を参照しながら、生命誕生に関わる力学を見てみよう。
熱力学は、秩序のある状態と比べた時、無秩序な状態のほうがはるかに起こりやすいことを教えている。すなわち、変化のほとんどは秩序から無秩序へと進む。しかし私たちが毎日目にする様に、驚くほど多くの秩序が地球には満ち溢れている。すなわち、生命が一端誕生すると秩序は無限に増幅する。この様に生命誕生を理論的に捉えるということは、無秩序な状態(生命誕生前の)から無限に増殖を繰り返す秩序が生まれる過程に関わる理論的枠組み、この世では極めて稀にしか起こらない過程に関わる理論的枠組みを理解するということだ。秩序の増幅を目の当たりにしても、バラバラの分子からこの秩序が偶然生まれるなどと考えるのは絶対に無理だと直感的に思う。
これについてDeaconは、シュレジンガーが行ったように、熱力学法則に反する、あるいは一見法則に従わないように見える過程(一番はっきりしているのは生命)を順々に探し出し、その背景にあるルールを探している。
Deaconが徹底しているのは、「創発」、「自己組織化」、「自己触媒」など生命を表現するために使い古された言葉や概念に思考を邪魔されないよう、独自の新しい用語を積極的に導入して考えている点だ。彼の用語を用いてこれまで幾つかの例で示してきた生命誕生への中間過程を見直してみよう。
熱力学はあらゆる系に当てはまるが、生命誕生で問題になるのは化学反応が可能な溶液中の力学だと想定できる。同じ分子でも個体と液体はまったく違う物理的特性を持つ。同じ熱力学の支配下にあっても、例えば気体、液体、個体と状態が変わると、分子間の関係はより秩序の高い方向へ進む。液体ではこの分子間の関係性の反映として、例えば粘度、表面張力、熱伝導度などを考えることができる。液体中の分子の関係性は、気体への相転換が起こるまで、液体としての性質を維持し続けようとする力と考えることもできる。この液体としての分子間の関係を加味した単純な物理システムを、Deaconは熱力学と区別してhomeodynamicsと名付けている。この用語のhomeo-は、同じ関係性を維持しようとする性質がこの力学系の基本であることを表現している。この系は熱力学法則に完全に従うシステムで、エントロピーは増大し、秩序の維持に必要な制約は散逸する。
一つのhomeodynamics系は平衡へ向かって進み続ける以外何も起こらないが、この系での変化を制約すると(例えば流れの中の岩)、homeodynamicsには従わない新しい系が生まれる。これをDeaconはmorphodynamicsと呼んでいる。この用語は、ほぼイリヤ・プリゴジンの散逸構造 と言い換えられ、具体的には液体が制約を受けることで発生する渦 や、ベルナール・セル がこの例だ。morpho-とは形態を意味するので、形態を持たないhomeodynamicsから、渦やベルナール・セルの様な形態が発生するということをうまく表現した用語だと思う。では、homeodynamicsからmorphodynamicsが発生する背景にある共通の法則とは何か?
もう一度渦の例でこれを考えてみよう。図1に示すように高いところにある2つの貯水槽から水を導き衝突させると、水の流れが維持される限り渦が形成される。すなわち、homeodynamicsな二つの系が逆向きに衝突して分子のhomeodynamicな動きを制約し合うとmorphodynamic 系が形成されることになる。順向きのhomeodynamic系が集まっても、エネルギーは高まるがmorphodynamic系が生まれることはない。
ではベルナール・セルはどうだろう?静置された液体の入った容器の底面を均等に熱すると、例えば固体の場合は伝導によりそのまま熱は散逸する。ところが液体の場合、表面と底面の温度差が発生すると、水分子の運動が高められ、対流が始まる。したがって、ベルナールセルを、熱の流れというhomeodynamicsと水の動きという2つのhomeodynamics系が制約し合うことで生まれるカオスを安定化させる力学として捉えることができる。すなわち、熱の流れと水分子の流れという質の異なるhomeodynamic系が制約しあっても、morphodynamics系は生まれる。
もちろんhomeodynamics系を自己組織化系と見ることもできる。重要なことは、morphodynamic系は必ず外部のhomeodynamic系が制約しあっているカオスの上に成立し、この制約が増幅することにより自己組織化が起こる点だ。
同じ様に、熱水噴出孔のマイクロセルが形成する制約による有機物生成もmorphodyamicsとして考えることができる。渦やベルナール・セルと異なり、巨視的な分子やエネルギーの流れではないが、触媒作用はエネルギーの流れを変化させる、分子の結合を促進する制約の一つだ。
ここまで見るだけでは、Deaconの考えも、生命という複雑系を、単純な力学系が相互作用してカオスが生まれるとき自己組織化が起こる系として捉える従来の考えに近い様に思える。しかし、Deaconは自己組織化やmorphodynamicsだけでは生命に必要な条件を捉えきれないと考えている。
生物はもちろん熱力学系であり、homeodynamic 系であり、自己組織化(制約化)するmorphodynamic系だが、これらをただ複雑に組み合わせても生物は発生せず、もう一段高次の力学系が必要だとDeaconは言う。この新しい力学系がteleodynamicsで、このもう一段高次の力学系を導入して生物までの道筋を整理したのがDeaconの考えの特徴と言える。
teleo-とはいうまでもなく、teleology(目的論)を意識して選んだ用語だと思う。目的、機能、複製、進化など、生物との共通性を有する増殖系として前回紹介した、Ottoの複製子 を例にteleodynamicsを考えてみよう。私の理解が間違っていなければ、Ottoの複製子teleodynamics系と言っていい。
まずOttoの複製子を思い出しながら、morphodynamic系との違いを見てみよう。morphodynamic系では、分子やエネルギーの供給が続き、ミクロレベルでの分子衝突により制約が発生、拡大し、マクロレベルの秩序が発生する。しかし、分子やエネルギーの供給が止まると渦もベルナール・セルも消える。一方、アミノ酸の供給が止まり新たなOttoの複製子の合成が止まっても、複製子自体はかなりの期間存在することができ、新たなアミノ酸の供給が始まると同じ複製子の増殖を再開することができる。この差が、morphodynamicsとteleodynamicsの差と言っていい。
熱水噴出孔で実際にOttoの複製子が形成されているという証拠はないが、これが生まれるための条件を考えてみよう(図2)。すでに述べたが熱水噴出孔でエネルギーと分子の流れがぶつかり、こうして生まれるカオスが噴出孔に存在するマイクロセルの持つ様々な制約を受けてアミノ酸を含む有機分子が合成されるのはmorphodynamicsに従う過程だ。もちろん地下からの噴出が止まれば有機物は海中に拡散してmorphodynamis系は消失する。
ここで「Otto複製子の成分GLKPKオリゴペプチドに化学的に相補的な別のペプチド(鋳型ペプチド)が存在し、GLKPKが一旦合成されると、それが鋳型になってアミノ酸重合反応を鋳型ペプチドが合成される方向へ促進する。また鋳型ペプチドは逆にOtto複製子の合成を高める」とする仮定を導入してみよう。この仮定を適用すると、GLKPKオリゴペプチドは一旦合成されると、あとは反応がこの2つの分子の合成へと制約されていく。言い換えると、有機合成が維持されるmorphodynamic系でのOttoの複製子の合成は、最初は偶然だが、一旦合成されると、同じことが安定して繰り返される秩序が生まれることになる。すなわち、GLKPKオリゴペプチドと鋳型ペプチドのどちらかが新しい制約として系内部に発生すると、GLKPKオリゴペプチドと鋳型ペプチドのセットを継続的に複製、増殖させることができる。これはmorphodynamicsでは見られなかった新しい系が生まれたことを意味している。
ここで導入した仮説はドイツの化学者Manfred Eigenが1978年の再帰的反応、ハイパーサイクルについて述べた論文(前述)で既に述べており、前回 、内的に発生する再帰的制約と呼んだ系も彼のハイパーサイクルを参考にしている。
この様に、自己組織化するmorphodynamics系に、ハイパーサイクルのような再帰的関係が発生することがteleodynamicsが生まれる条件で、この関係が成立すると新しい制約を増幅させる系が現れる。もちろんハイパーサイクル自体は系として自己増殖できても化学反応にしか見えないが、前回紹介した様にGLKPKオリゴペプチドが重なり合ってOtto複製子が出来始めると、自己性を含む、生物と多くの共通点を有する力学系が発生する。Otto複製子では、複製すべき構造が環境との関わりで「情報」を発生させ、この情報に従って複製する構造が決まる。また、GLKPKオリゴペプチドはただの化学物質だが、Otto複製子の構成成分としての「機能」が生まれる。すなわちmorphodynamics系には見られない、情報、機能、自己性がteleodynamics系には存在する。このように、teleodynamics系は必ずしも生命である必要はないが、生命と共通の性質を有していることが下記らかな力学系だ。
これまで、様々な例を使ってDeaconの提唱する3つの力学系、homeodynamics,
morphodynamics, teleodynamicsについて説明したが、これを図にまとめておく。Ottoの複製子を生物として見ることはできないという声が聞こえてくるが、上位の力学系が下位の力学系の単純な延長でないことは理解していただけたのではないだろうか。
Deaconの考えは、生命誕生を考えるとき、私にとってはもっとも頼りになる指針になっている。
[
西川 伸一 ]
LUCA 誕生に必要な条件
2016年2月15日
繰り返すが、Ottoの複製子(Otto Replicator:
OR)は、自己性を持ち、環境との相互作用で決まる特定の構造を繰り返し複製できる点で、DeaconがTeleodynamicsと呼ぶ力学系の条件を満たしていることを述べた。しかし、だれもORを生物とは呼ばないだろう。そこで、ORと実際の生物を比較し、生命の条件を考えてみよう(図1:前回 と同じ図を再掲する)。
図1 前回掲載したOtto複製子についての、仮想合成経路を再掲している。これから、これと比べながら原始生命LUCAの条件を考えていく。
まずORは1種類のペプチド(図中では青と黄色の矢印)が基本単位になっているだけで、私たちが生命と呼んでいる最も単純な存在と比べても、単純すぎる。たしかに複雑だから生命と言えるわけではないが、やはり複雑性を持つことは生命の条件になるだろう。生命が複雑に見える一つの要因は、物質とエネルギーの代謝が生物には内在化しているからだ。
次にOR構造の形成過程を見てみよう。ORは熱水噴出孔に発生する(と仮定している)物質とエネルギーのmorphodynamics力学により合成されるペプチドから構成される。もちろん、OR自身も触媒や鋳型として働くことで、構築を組織化(Organize)している。しかし、生命と違って物質とエネルギーの供給は内在化されていない。一方、生物も外界からの物質に依存はしているが、エネルギーや物質代謝を生物内部で行っている。
とすると、ORは代謝を内在化させるという条件をスキップして、自己性を獲得してしまっていると言えるのかもしれない。その結果、物質とエネルギーの供給は全て外部に依存している。
このことから、少なくとも地球で見られる生命誕生の条件として、独立性・自己性が生まれるより前に、生存に必要なエネルギーや物質の代謝システムの少なくとも一部が内在化されていることを指摘できる。これがどう行われたのか想像してみよう。
前々回述べたようにMartinらはこの準備が熱水噴出孔のマイクロセル内で準備されたと考えている。マイクロセルは無機物でできており、その中での代謝システムがどれほど複雑化しても、独立することはない。その代わりに、安定した環境を長期間提供できることから、最終的に内在化することが可能な代謝システムの準備がここで起こったとする考えは説得力がある。
LUCA誕生前にエネルギーと有機物の代謝システムが生まれる過程は、現存の全ての生物に共通するシステムを参考にして考える以外にない。そして全ての生物がエネルギーと有機物合成のために共通に使っているのが、アセチルCoA、ATP、水素イオン勾配を利用したATP合成システムだ。したがって、まずこれらの分子やシステムがどう生まれたかを考える必要がある。
まずアセチルCoA,ATP分子から見ていこう。図2に示すように、アセチルCoAは、細胞内の有機合成の核として機能しており、他にも図には示していないがコレステロール合成や、ケトン体の合成など、まずほとんどの有機分子代謝経路に関わっている。おそらくわかっているものを網羅するだけで、生化学の教科書一冊分必要なはずだ(実を言うと、代謝経路はこれまで私の最も苦手な分野だ。しかし生命誕生を考えるためには必須の知識で、若い研究者はぜひ私のような苦手意識を持たないようにして欲しいと思う)。
しかし図3に示すように、熱水噴出孔では炭酸ガスが水素により還元された後、アセチルCoAを合成するWood–Ljungdahl 反応と呼ばれる合成回路が進む条件が存在したと考えられている。確かにCoAの分子構造はLUCAが生まれる条件に常に存在するにはあまりに複雑に見える。しかし、ただのメチル基がCoAの代わりに存在する極めて単純な分子でも、アセチルCoA と同じ機能を果たし得るし、またこの程度の有機分子は十分存在し得たと考えていいだろう。
アセチルCoAと同様、糖と核酸とリン酸が結合した一見複雑なATPも生物の力を借りることなく合成されることはすでに述べたので、ここではADPをリン酸化して不安定なATPに変え、それがADPに戻る時のエネルギーを化学反応に使う仕組みの発生過程について考えてみよう。
現在の生物にはATPを合成するための多様な回路が存在している。しかし、あらゆる生物に存在する仕組みは膜を隔てた水素イオンの勾配をエネルギーとしてATP合成酵素を動かしADPをリン酸化する方法だ。ただこの方法で持続的にATPを合成するためには、細胞内外の水素イオン勾配を維持する必要がある。
私たちの細胞でATP合成を行なっているミトコンドリアでの仕組みを見てみよう(図Wikipediaより)。電子を移送するトランスポーターが膜上に並んでおり(図にはI,II,IIIとナンバーを付けて示している)、電子が伝達システムの分子間を移動するたびに水素イオンがミトコンドリア外に放出される様にできており、これによりミトコンドリア内に流入した水素イオンは細胞質へと汲み出される。こうして維持される水素イオンの勾配を使って水素イオンはミトコンドリア膜上にあるATP合成構成酵素を通って流入する。このエネルギーを用いてこの酵素はATP合成を行う。(より詳しく知りたい方は、季刊生命誌43号の図 もご参考ください)
ATPを作るために水素イオン勾配を使うシステムはあらゆる生物に見られるが、エネルギーのために常に流入する水素イオンをくみ出して勾配を維持するためには、このように高度に組織された複雑な構造を持つ分子セットが必要になる。もちろん、LUCAが誕生する最初からこのような分子が存在するはずはない。しかし、水素イオンの勾配を維持する仕組みがないとエネルギーを自分で作れないというジレンマに陥る。実際、薬剤でこの電子伝達系を止めると、ATPの作れなくなった細胞は即座に死滅する。
どうすれば複雑な電子伝達系なしに水素イオンの勾配を維持すれば良いのか?この問題を解決する一つの素晴らしいアイデアが、Nick Laneらにより示されている(Sojo et al,
PlosBiology 12: e1001926, 2014:図4)ので紹介しよう。このアイデアは、特別なメカニズムなしに水素イオン勾配が利用できる方法を示すだけでなく、生物の自己化、独立化の過程も説明できる可能性を秘めたアイデアだ。
LaneはMartinとともに、熱水噴出孔でLUCA誕生の準備が進んだと考えている一人だ。マイクロセルは小さな穴が空いているが、分子透過性の選択性はない。図では、この穴に水素イオンが透過する脂肪膜を持った小胞が詰まるという状況を設定している。熱水噴出孔では、地底から湧き出すアルカリ性の液体と、弱酸性の海水が存在するが、それぞれの流れが脂肪胞とマイクロセルを形成する無機物で隔てられると、持続する水素イオンの勾配が図の上下で生まれる。地底からの液体と、海水は常に流れているので上下のpHの差は維持され、水素イオンの勾配も維持される。
ここに図5・緑色で示した水素イオンの流れをATP合成に使える原始的タンパク質が誕生すれば、水素イオンを脂肪胞外へ汲み出す複雑なメカニズムが存在しなくとも、ATP合成システムを持つ脂肪小胞が生まれる。その後、同じ脂肪胞内で水素イオンと他のイオンを交換的に移行させるトランスポーター分子がたまたま合成されると、水素イオンの汲み出し機構とATP合成システムの両方を備えた脂肪胞が完成する。
このシナリオが実際に起こったかどうかはわからない。しかしこの考えは、LUCAに必須のATP合成システムとアセチルCoAを併せ持った脂肪胞の形成過程を、大きな飛躍をせずに考えられることを示唆している。少なくとも私は、エネルギーと有機物質合成系を備えた脂肪胞が熱水噴出孔で発生することがそれほど困難でないと確信できる。また、このような細胞様システムを人工的に合成して研究が行われることも遠くない話だと思っている。
とはいえ、エネルギーと有機物の合成系を内在する小胞を先行させて考えるとき、次にもっとも難しい問題として登場するのが複製だ。ORのような単純な構造の複製は容易だが、系が複雑になればなるほど、その複製は困難になる。
有機物とエネルギー合成システムを備えた細胞様小胞の実現性を確認した後で、十分複雑化したシステムにどうすれば複製能力を付与できるかを考えていこう
[
西川 伸一 ]
ダーウィン進化自体が情報を発生させる
2016年3月1日
前回までのLUCAへの道(個人的に可能性が高いと考えている道にすぎないことを断っておく)を手短にまとめると、次のようになるだろう。おそらく水素と炭酸ガスから、アセチルーCoAあるいは、より単純な代換え化合物を合成するためのWood-Ljungdahl経路が完成する(49話図3参照 )。これが脂肪膜内で起こるのか、原始のスープの中で起こるのかはわからない。しかしこれが完成すると、様々な有機物を合成できるようになる。もちろん脂肪膜も形成される。こうしてできた脂肪膜は小胞を形成するだけでなく、強力な触媒としても作用することはすでに述べた。アセチルCoAと一定の触媒機能を備えた脂肪膜小胞が比較的高い確率で持続的に形成され、たまたま自然に形成された水素イオン勾配の存在するマイクロセルに引っかかっているうち、水素イオン勾配をATP合成に使える小胞が生まれてくる(ATP合成酵素の誕生)。ここまでが前回述べたシナリオだ。
しかしこれだけでは自然の水素勾配が存在する場所から離れることはできない。独立したATP合成系を持つためには、細胞膜内外のプロトン勾配を維持するメカニズムが必要になる。もちろんミトコンドリアにあるような電子伝達系は複雑すぎて、それが備わるのはずっと後の話だ。この最も単純なプロトン勾配維持システムについてもNick Laneの仮説は十分説得力があるので紹介しておこう(
Sojo et al, PlosBiology 12: e1001926, 2014)
自然のプロトン勾配を利用するATP合成酵素ができるところまで(図1Aまで)は前回紹介した。この仮説では、次の過程をプロトンとナトリウムイオンを反対の方向に移動させるアンチポートの誕生としている(図1B)。膜の透過性がザルのように高いとき、このアンチポートの機能的意味はないが、膜がナトリウムを通さなくなると、プロトン流入の度にナトリウムイオンを汲み出すメカニズムとして働くことができる。この分子に加えて、さらに小胞中からナトリウムの汲み出しを高めるために、プロトンとナトリウムのどちらでも汲み出せるエネルギー依存的ポンプができると(図1C)、プロトン勾配を維持するための準備が整う。プロトン通過性の膜を持つ小胞の場合、この分子はもっぱらナトリウム汲み出しに使われるが(図1D)、プロトンを通さない膜に変化するとプロトンを汲み出してプロトン勾配を維持するメカニズムとして働くことができる(図1E)。このようにして独立したプロトン勾配維持システムが出来上がると、外界の条件にとらわれずATP合成に利用する小胞が完成する(図1)。
さて、ここまで順を追ってNick LaneやWilliam Martinの考えを中心に、ありそうなシナリオをつないでみると、読者の皆さんも独立した代謝システムを持つ脂肪胞なら十分合成できそうだと納得されるのではないだろうか。しかし本当は絵に描いたようなシナリオに簡単に納得しないでほしいと思っている。実際に重要なのは可能性のあるシナリオではなく、どのシナリオであっても、その過程が繰り返し起こる条件を明示できるかどうかだ。
ダーウィン進化では、特定の形質に情報、すなわちゲノムが対応し、環境にフィットした性質を生殖を通して(すなわちゲノムの複製により)増幅することができる。しかし、ゲノムが発生する前にはこの手は使えない。
ゲノムが存在しない時のダーウィン型進化とは何かをまず考えてみよう。生物が介在しない有機合成系では、炭酸ガスや水素といった単純な無機物から、複雑で多様な有機物が持続的に発生している。ただこの合成はランダムで、基本的には再帰性はない。従って多様性がますます増大する、すなわちエントロピーが増大するhomeodynamic過程と考えられる。この中から、例えばATP合成系を持った脂肪小胞が生まれるということは、エントロピーが増大するよう一方向に進む反応系を制約して、特定の秩序が自然選択される条件が存在することになる(図2)。
では何が選択されるか。もっとも理解しやすいのは、分子の安定性を指標とする選択だろう。普通有機物の寿命は短い。しかし、環境条件にフィットした分子は長い時間存在することができる。あるいは温度勾配を利用したふるいにかかり、特定の大きさの分子が特定のマイクロセルに濃縮され選択されることでも多様性を減じることができる。さらにはマイクロセルを構成する無機質の持つ触媒効果も当然多様性の制約に働く。これらが合わさって特定の構造が安定に存在できると、合成自体はランダムであっても、自然選択により系内の多様性を減少させることがある程度可能になる。
注意して欲しいのは、環境要因が多様な分子集合の多様性を減らす制約として働くとき、巧まずして一種の情報が発生していることだ。すなわち、こうあるべきという方向性を環境が与えることで、存在可能な分子の種類を制約している。ただ、できてきた分子を環境によって選択するだけの情報では、制約の程度は知れており、似た種類の分子の濃度は上昇するかもしれないが、同じものが繰り返し合成されるほどの情報にはならず、これだけでは情報は萌芽段階にとどまる。
では次に持続的な情報が発生するには何が必要か?
ここでもう一度コンビナトリアル化学で紹介したOttoの複製子が生まれる過程を思い起こしてほしい。
重要な実験なので図3に再掲するが、Ottoの複製子はGLKFKと5種類のアミノ酸がSH基を2個もつベンゼン環に連なっている分子を試験管内で反応させているうち、突然現れる構造だ。最初はSH基同士が反応重合して多様な化合物を作るが(図3b及びd)、ある時突然多様性が失われ、基本構造が6個環状に結合した構造(6mer)だけに収束する(図3d)。これは6merが発生し、6mer同士が今度は縦に重合し始めると、それ自身が反応を6merへ収束させる能力を持つからだ。すなわち、合成物自体が制約として、合成反応自体を制御するようになると、ランダムな反応が特定の構造に収束することがあり得ることを示している。
この制約は物理学の法則とは全く異なる。すなわち、反応は最初に生まれた再帰的制約能力を持つ分子の性質によって決まり、もう一度最初から反応を繰り返した時、同じ制約が繰り返して現れる保証はない。特に最終産物が複雑であればあるほどその確率は低い。物理法則とは違い、偶然に支配されているが、一旦発生すると反応が向かうべき方向性を情報として指示するようになる。
原理的には、ここで説明したのと同じような情報の発生と、それに制約された過程が、LUCA誕生過程でも複雑な形で起こったのだろう。これまで見てきたように脂肪膜や、アセチルCoAなどは再帰的制約を形成する能力が高い分子だ。実際には何段階にもわたって制約=情報が発生し、より生命に近いteleodynamics系が発生したと考えられる。
しかしこうして比較的複雑な細胞様構造が発生し、この構造が、合成の方向性を決める一種の情報による制約により繰り返し合成できるとしても、合成物自体と環境がリンクして自然発生した情報は、情報としては生命誕生には十分でなかったようだ。すなわち、現在の生物には独立し系全体の複製をリードできる情報が存在している。この情報の独立が次のステップだ。このステップにおそらくRNAワールドと呼ばれている系が必要になる。次回はこのRNAワールドについてみることにする。
[
西川 伸一 ]
情報の独立
2016年3月15日
Ottoの複製子をモデルに、ランダムな化学合成系の過程から、この反応を制約する分子が誕生すると、それが情報と同じ働きをして、反応を一定の方向に導き、一定の構造を複製し続けることを前回 示した。これほど強い制約でなくとも、多様化する有機分子が環境条件によりダーウィン的選択をうけ、特定の構造が濃縮されるよう制約されること自体も、考えようによっては、情報が発生していると見ることができる。繰り返すがここでいう制約は物理法則とは違って偶然発生したもので、この制約に基づく情報は独立して存在しているわけではない。すなわち少しでも環境が変化すれば、その情報は消失する。従って、ここではこの様な情報を偽情報と呼んでおく。
偽情報だけでどこまで複雑なシステムが形成可能か?計算機によるシミュレーション実験が必要だろうが、偽情報だけで達成できる複雑性には限界があると思う。これが生命誕生以前の有機合成システムがもつ物理的限界になる。
例えば前回述べたATPエネルギー合成系と、有機分子合成系を両方備えた程度の複雑性をもつ脂肪胞の複製でも、偽情報だけでは安定に複製することは到底不可能ではないかと考えている。では次の段階として何が必要か?
この答えを地球上に存在する生物に求めるとすると、「情報がゲノムとして独立すること」と言っていいだろう。現存のあらゆる生物はセントラルドグマに従い、DNAを媒体としてゲノム情報を独立させ、この情報を複製により増殖するとともに、転写により細胞の維持に使っている。そして、生物が介在しない有機合成系では到底到達できない複雑性を達成している。
ただ、自律的に有機物とエネルギーを形成する代謝システムが、一足飛びに現存の生物が持つ、独立した情報を中心にしたシステムへと転換することは至難の業で、幾つかの中間段階を介在させて考える必要がある。この中間段階として提案されているのが、いわゆるRNAワールド仮説だ。この仮説には様々なバージョンがあり、エネルギーや物質代謝システムに先行してRNAワールドが存在したと考えるreplication first仮説もあるが、ここでは最低限の独立代謝システムと並行して、あるいはその成立後に加わる系として考えていく。
もちろん、どちらが実際に起こったのか、あるいは本当にRNAワールドが存在したのかに答えることは現段階では難しい。ただRNAはそれ自身で明確な情報と機能が共存する有機システムを形成する能力を有し、LUCAへの中間段階として働く可能性がある。まず、その点について見てみよう。
RNAワールド仮説は、タンパク質と同じようにRNAがリボザイムと呼べる様々な酵素活性を持ちうるという発見が基礎となっている。もともとRNAはヘアピンループ構造を基盤とする複雑な立体構造を取り得ることが知られており、タンパク質と同じような酵素活性を持てるのではと期待されていた。1980年に入ってすぐ、後にノーベル賞を受賞するThomas CechとSidney Altmanが、スプライシングや前駆体tRNAが機能をもつ成熟tRNAになる際のプロセッシングにRNAが酵素として働いていることを発見する(図1)。
https://commons.wikimedia.org/wiki/File:Ribozyme.jpg )。Thomas Cechはリボザイムを含む一本のmRNAが、タンパク質の助けを借りることなく自分自身を切断融合する(スプライス)ことを示してノーベル賞を受賞した。
それ以後研究は急速に進み、現在リボザイムは様々な生体機能を調節するために有望な分子として創薬などに利用され始めている。例えば50merほどのRNAをランダムに合成して、その中から特定の分子と結合するRNAを生成して、阻害剤として使うというような使い方が行われている。なぜ期待が大きいかというと、活性のあるRNAを容易に合成できること、それ自身が塩基配列情報を持っているため、同じ分子を複製することが容易であるためだ。
このようにCechとAltmanの発見により、それ自身についての明確な情報を担ったRNAが同時に、酵素活性という機能を持ち得ることが明らかになった。すなわち、偽情報と比べた時、RNAワールドでは、情報が独立性を持っている。以前述べたが、情報は物質ではない。リボザイムではRNAという媒体で表現されていても、次の段階でDNAということなる媒体で同じ内容を表現することができる。まさに、DNAを媒体として独立した情報を持つLUCAの中間段階にぴったりの存在であることがわかる。
ただいくらRNAが情報としての側面と、機能分子としての側面を持つと言っても、最初はRNAが情報に基づいて合成されることはない。少しわかりにくいが、この段階ではランダムにRNAが合成される。すなわち外で降る雨と同じで、自然現象と言える。ただ、できた情報を何らかの方法で解釈することができるようになると、ここに情報が誕生する。ランダムに自然現象として生まれたRNAの中に、このRNAが持つ情報を解釈するRNAが誕生したと考えるのがRNAワールド仮説だ。
これまで説明してきたように、条件が整えば自然現象としてヌクレオチドを合成することができる。またフォスファチジルコリンを主成分とする脂肪小胞はRNAを重合させる活性が高く、50merまでのランダムなポリヌクレオチドを合成するための触媒活性を持つ(Orig Life Evol Biosph 38:57、2008)。従って、現在研究者がリボザイム合成として行っていることは、自然現象として起こる。研究者は、自分の目的に合わせてこの中から特定のRNAを選択し、そこにある情報を使うが、RNAワールド誕生では、まず誕生したRNAの中に、RNAの塩基配列を解釈できる機能が生まれることが必要になる。従って、一般的にRNAワールド仮説ではRNA配列を解釈して複製するリボザイムの誕生を最初のゴールと設定している。
図2 RNAワールド誕生までの過程を描いたJoyceらの仮説。
Joyceらは先に述べたRNAの重合を触媒する脂肪膜と、RNAが結合して濃縮される基質を備えた小胞の中でRNAの分子進化が進み、RNAポリメラーゼが誕生するまでの過程を図2で示すように描いている。まず、ランダムにポリマー化したRNAはヘアピンループ形成を介して、多様な構造を形成する。ただ、ランダムに合成されるRNAの長さには限界があるので、さらに複雑なRNAを合成するためにはまずRNA鎖同士を結合するリガーゼ活性を持つリボザイムが発生する必要がある。この結果ヘアピン同士が重合を始め、より複雑な構造の大きなRNA分子が形成される。こうして生まれる分子構造の中にRNAポリメラーゼ活性を持つ分子が誕生することでRNAワールドが完成することになる。一旦RNAポリメラーゼが誕生すると、小胞の中に存在するRNAを鋳型として複製が行われる。もちろんポリメラーゼ自身の複製もおこる。
このシナリオを実験的に証明することは難しい。すなわち最初はヌクレオチドしか存在しない状態からスタートして、RNAの分子進化を介してRNAポリメラーゼを誕生させ、自己複製が可能なRNAワールドを形成する実験は行われていない。しかし自己複製可能なRNAシステムが可能なことは理論的にも、実験的にも示されている。
繰り返すがRNAワールドの誕生は、自然に合成されているときは情報でも何でもないRNAの塩基配列の中に、塩基配列を解釈できるリボザイムが誕生した時点で始まる。この時、それまで情報でなかったRNAの塩基配列が、情報に変換される。そしてこうしてできた情報を増殖させられる系は、増殖できず一回で消滅する情報と比べると、当然自然選択の対象になる。また、情報のエラー発生を通して、情報は多様化する。解釈するリボザイムが存在する限り、エラーが起こった情報も、情報として処理され、自然選択を通してより環境にフィットした系が進化することになる。ただ、このRNAワールドは、RNAだけで完結している。従って次のステップは、多様化と自然選択が可能なRNAワールドが、例えば独立代謝システムと相互作用し、両者が組織化された系の誕生だ。次回は、この過程について考えてみる。
[
西川 伸一 ]
参照情報と記号情報の誕生
2016年4月1日
前回 、RNAワールドでは、自分を鋳型として新しい分子を複製できるシステムが可能になっていることを説明した。同じような現象は、プリオンなどでも見られるため、RNAワールド以外でこれが起こらないことを証明することは難しい。もちろん私はこの分野の素人だが、それでもRNAがランダムに合成されているうちに、リガーゼやリプリカーゼ活性のあるリボザイムが生まれ、それによりRNA自体が情報として独立するとする考えは理解しやすい。また、ここで議論しているRNAの特徴を利用して、アプタマーなどRNAテクノロジーが進展しているのをみると、特定の機能が塩基の配列として解釈され、塩基配列から生まれる機能分子を複製することが可能なRNAワールド仮説は極めて魅力的だ。
また分子の機能を塩基の配列として解釈し複製できることは、RNAワールドでは情報が環境から独立したことを示す。例えばOttoの複製子も同じ分子を複製するが、この時の情報は前にも述べた偽情報で、複製子自体の物理化学的性質と環境条件によって形成されており、環境が変わると、情報の内容も変化する。一方RNAワールドでの情報は、もちろん大きな意味で物理化学法則(RNAという媒体を使う点)に従い、条件によっては情報として読み出せないこともあるかもしれないが、原則として塩基の並びとして表現されており、周りの条件からは独立できている。
このようにRNAワールド仮説は、機能を周りの条件から独立した情報として表現できることを示してくれたが、この情報はRNAワールド内だけでしか働かない。現在のような、アミノ酸、タンパク質、リボゾームRNA、mRNAなどが入り混じったセントラルドグマが成立するためには、まず特定のRNA分子がアミノ酸と対応する参照関係やコドンとアミノ酸の対応のような記号化が必要になる。現存の生物を眺める時、アミノ酸との参照関係と記号化(コドン化)が最もはっきりと見られるのがトランスファーRNA(tRNA)だ。次に、tRNAとアミノ酸との参照関係がどのように生まれたのか、またtRNAが塩基配列を記号として認識できるようになった過程を見てみよう。
まず大学生時代に戻って、トランスファーRNAとはどんな分子だったか思い出してみよう。
図1に tRNA共通の構造を示すが、平均76塩基からなるRNAで、ミニヘリックスを形成する3’末端に特定のアミノ酸が結合し、アンチコドンループでmRNAと結合する。この構造から、tRNAがアミノ酸と核酸の参照関係を成立させている分子であることがよくわかる。すなわち、アミノ酸とtRNA自身の対応関係を、mRNA、そして最後にはDNA上の塩基配列へと拡大する役割を担っている(後述のように実際には簡単ではない)。
このtRNA自身と、アミノ酸との参照関係の成立には、各アミノ酸に対応して存在するtRNAを認識して、それに対応したアミノ酸を結合させるアミノアシルtRNA合成酵素が関わっている。
図2に示すように、アミノアシルtRNA合成酵素(aatRNA合成酵素)は、1)ATPによりアミノ酸を活性型に変え、2)そのアミノ酸に対応したtRNAと結合して、3)アミノ酸を3’末端に共有結合させることで、tRNAとアミノ酸の参照関係を成立させる。すなわち、各tRNAとアミノ酸の特異的な参照関係を決めているのは、まさにこのaatRNA合成酵素ということになる。しかし、こんな都合のいい酵素は最初から存在するはずもなく、アミノ酸と特定のRNAの対応関係を成立させるための単純で自律的なシステムを構想しなければならない。1982年これを可能にするシステムについて清水幹夫はC4N仮説を提唱した。
図2: アミノアシルtRNA合成酵素によるアミノ酸とtRNAの結合プロセス(Wikipediaを改変)
図3 清水幹夫の論文(J.Biochem. 117, 23-26, 1995)に書かれていたC4N仮説が想定している、原始型tRNA.
図3は清水の1995年の論文(J.Biochem. 117,
23-26, 1995)を改変したものだが、tRNAのアンチコドン部を5’末端に持ち、現存のtRNAのミニヘリックス部分に似たヘアピン、識別塩基、CCA3’末端と続く短いRNA分子(例としてグリシンに対してはGCCGGCGAUGUUCGCAUCGCCUCCA)が、アスパラギンとバリンからできたペプチドと結合すると、特定のアミノ酸(この場合グリシン)に対応した特異的ポケットを作り、Asp-Valの触媒作用でアミノアシル化されたRNAに変換できるという仮説だ。1995年の論文では、合成したRNA、アミノアシル化グリシンアデニル酸、そしてAsp-Valを反応させると、アミノ酸がRNAに転移できることを示している。さらに、アンチコドン部分をアラニン(AGC),バリン(GAC)に変更すると、今度はそれぞれのアミノ酸が特異的にRNAと結合することから、アンチコドンが3’末端の識別塩基と協調することで特異性を発揮できることも示している。すなわち、アミノ酸ダイマーが共存しておれば、RNAが自律的にアミノ酸との参照関係を成立できる可能性を明らかにした画期的な論文といえる。
もともと、Gly-Glyのようなアミノ酸のダイマーは、RNAの分解を阻害する能力があることが知られていた。したがって、アミノ酸ダイマーと特定のRNAが安定的な組み合わせとして選択されていた可能性は十分考えられる。ただ残念なのは、2013年の東京理科大学の田村さんの総説を読むと(Viva
Origino 41, 29-33, 2013)、「C4Nは非常に画期的なアイデアであるが、今後、この仮説を実験的に検証していく必要がある」と書かれており、1995年の実験がまだ再現されていないことをうかがわせる。とはいえ、C4N仮説は一石二鳥のアイデアで、RNAワールドに、アミノ酸への参照関係性を成立させ、この参照関係をコドンとして記号化することまで視野に入れた独創的な仮説だと思う。
ただ、ここまでうまく話が進まなくとも、NCCA配列を3’末端に持つRNAが、それ自身で、あるいは他のリボザイムの助けを借りてアミノアシルRNAを合成することは十分可能だろう。一方アミノ酸との参照関係を記号化するコドンの誕生については、アミノ酸自体の化学的性質と、塩基配列で表現されるコドンの間に物理化学的・自律的な対応関係が存在しており、少なくとも一部のアミノ酸に対するコドンルールの誕生は化学的に説明できると考える人は多い。
ただ、tRNAに存在するアンチコドンは、アミノ酸の並びを指示するmRNAなどの指令が存在しなければ意味を持たない。すなわち、アミノ酸とRNAワールドをつなぐ媒体はできたとしても、この媒体を使って指示を行う情報はまだ全く存在していない。では、原始tRNAは何をしていたのか?
tRNAの原始型はアミノ酸を濃縮するために誕生してきたのかもしれない。生命誕生前でも、アミノ酸が生成し、その重合が起こりうることは示されているが、重合するにはアミノ酸の濃度が一定以上である必要がある。しかし、実際にはランダムに作られるアミノ酸濃度を高く保つのは難しかっただろう。したがって、アミノ酸を一定の場所に拾い集めることが重合の条件になり、この役割を原始tRNAは担っていたのかもしれない。。言い換えると、原始型tRNAの持つアンチコドンはあくまでも特異的アミノ酸を拾うための仕組みで、アミノ酸をくわえたRNAがヘアピン構造を介して特定のマトリックスに結合し、ランダムではあってもアミノ酸を特定の場所に濃縮することで、ペプチド合成の可能性を高めていたと考えても不思議はない。すでに述べたが、アミノ酸ダイマーの一部はRNAを分解から保護する作用があり、その合成を促進する系は進化的優位性がある。
こう考えると、図3のC4N仮説でヘアピン構造として示されているアームは、ひょっとしたら、マトリックスに結合するためのアームとして使われたのかもしれない。そしてこのマトリックスがDNAであった可能性も十分ある。おそらく生命誕生前に最も多く存在した高分子の一つがATPだろうが、それが重合すれば安定度抜群のマトリックスDNA鎖ができる。また、DNAはRNAともタンパク質とも相互作用可能な高分子だ。アミノアシル化されたRNAを濃縮して、ペプチドを合成するには最適の高分子と言っていいだろう。今述べたのはただの妄想だが、DNAとRNAの関係はこんなところから始まったのかもしれない(図4)。
図4:DNAをマトリックスとして、原始型tRNAが集合してペプチドの合成が促進する可能性を描いた図。
この段階では(図4)、アミノ酸と特定のRNA分子が参照関係を形成し、(C4N仮説が正しいなら)、さらにアミノ酸とコドンとの関係まで成立していたためかもしれないが、まだtRNA上のアンチコドンと対応させる情報はどこにも存在しない。この場合、ペプチドはあくまでもランダムに作られる。こうしてランダムに合成されたペプチドを環境との適応性を指標に選択したとしても、その選択結果を記録する逆セントラルドグマが可能であることを示す証拠は現在のところ見当たらない。
いよいよ問題は核心に入ってきたが、最後に残る課題はこの段階から、DNAへの情報の移転がどう起こったのかを説明することになる。
この過程に関してはおそらく2つの説明が可能だろう。一つは、選択されたペプチドのアミノ酸配列を記号として解釈する方法が存在するとする考え方と、アミノ酸を濃縮するためのマトリックスとして使われてきたDNAが非特異的マトリックスから、コドンでアミノ酸と対応する媒体へと変換をはたし、このランダムな配列から合成されたペプチドの選択を通して、DNA配列が選択され、遺伝子が生まれるとする考えだ。
この問題をさらに掘り下げるため、次回はアミノ酸の重合を支えるリボゾームRNAについて見て行こう。
[
西川 伸一 ]
独立した遺伝情報誕生
2016年4月15日
生命誕生以前、コドンやアンチコドンに対応する塩基配列は、コードとしてではなく、その物理化学的性質に基づいてアミノ酸と化学的に結合していた可能性を前回 述べた。さらにtRNAの中には、アミノ酸が結合したアミノアシル化tRNAを合成するリボザイム活性を持つものが存在することも示されている。従って、原始tRNAは、酵素の力を借りることなく特異的アミノ酸をキャッチし、そのアミノ酸を3’末端に結合させたアミノアシルtRNA(aatRNA)を合成できる。
例えば前回 述べた清水のC4N仮説によると、この時現在のアンチコドン塩基配列がアミノ酸をキャッチするのに使われるが、この使い方は、現存のtRNAのように、コドン/アンチコドンのようなコードとしてではない。くどくなるのを恐れず、繰り返すと、原始tRNAにたまたま現在のアンチコドンと一致する塩基の配列が存在していても、アミノ酸との対応が記号化した情報として表現されているわけではない。アンチコドンとアミノ酸が確実に対応づけられていても、これはあくまでもアンチコドンの持つ物理化学的性質の反映だ。
やはり前回、コドンを持つmRNAが存在しなくても、アミノアシル化したtRNAが何かのマトリックスを利用して集まることができること、また濃度の低いアミノ酸をキャッチして一定の場所に濃縮するためにtRNAが誕生したのではないかと述べた。こうしてアミノ酸を濃縮する事でポリペプチドへと重合させる可能性が高まる(52話 の図4を再掲)。即ち、RNAとペプチドの基本関係(物理的)がこうしてできあがる。
図1:52話の図4を再掲している。今回の図では、ペプチド形成は、原始リボゾームのペプチド転移活性によることを明確に記載している。
この時、tRNAに結合したアミノ酸をポリペプチドへ重合するペプチド転移酵素が必要だが、RNAワールドではもちろんこれを行っているのはリボザイムだ。現存のリボゾームはRNAと約50種類のタンパク質が結合してできているが、ペプチドを結合する活性を持つのは純粋にRNAから出来たリボザイム部分であることが証明されている。すなわち、タンパク質からできた酵素にその役割が移行したアミノアシルtRNA合成と異なり、現存の生物でも、実際にこのペプチド転移反応はリリボザイムが行っている。
図2に、現存の生物に見られるリボゾーム、tRNA、アミノ酸、ポリペプチドの関係を示したが、mRNAの塩基配列に対応したアンチコドンを持つtRNA同士が集まり、それぞれが担っているアミノ酸が重合する。この時、tRNA が集まる場所をリボゾームが提供していることがわかる。すなわち、図1で想定したマトリックスの役割をmRNAとリボゾームが演じている。これに加えて、リボゾーム内のリボザイムは、tRNAが担っているアミノ酸を順々に結合させ、ポリペプチドを合成するペプチド転移酵素作用も持っている。このように、原始リボゾームも現存のリボゾームも、tRNAを濃縮するマトリックスとペプチド転移酵素の集まったユニットと見ることができる。勿論RNAワールドでは、環境に適合するRNAは複製により増幅される(遺伝の可能性)ことは言うまでもない。
こう見てくると、タンパク質を作るためのすべての基本過程、すなわちアミノアシル化tRNAの合成及び、ペプチド転移反応の両方をリボザイムが行っていたことは重要だ。生命誕生過程が、先行して複製能力(遺伝能力)を実現したRNAワールドに、タンパク質が後から加わるという順序で進んだことを強く示唆している。言い換えると、RNAの活性がペプチドの合成も支配していた時期から、性質の異なる2種類の有機分子が互いに作用し合う世界へ移行したことがわかる。
物質として全く異なる核酸とアミノ酸を対応させるための記号化が必要になるのはまさにこのときだ。
原始型から現代のtRNAへの構造変化は情報誕生過程のヒントを与えてくれる。すなわち、原始型tRNAではアンチコドンはアミノ酸との物理的結合に使われており、情報を解釈する機能はない。一方現代型tRNAでは、アミノ酸と対応するアンチコドンが存在するが、これはアミノ酸と結合しているループから離れて存在しており、直接アミノ酸とアンチコドンが作用し合うことはない。 考えてみると、現存の分子で、物質と記号化情報がこれほど上手に媒介できる構造を持つ分子はtRNA以外にないだろう。しかも、RNAワールドではRNAの塩基配列により生まれる機能であれば複製・増幅が可能だし(遺伝)、多様化と選択(進化)も可能だ。
図3 情報と物質を対応させる媒体としてのtRNA)。tRNAの機能を知るため52話の図を再掲。
この段階で情報誕生の接点に存在する役者をリストすると、1)アンチコドン配列の持つ物理的性質の結果特定のアミノ酸に結合する原始型tRNA、2)ペプチド転移活性を持つリボザイム、3)異なるアミノアシルtRNAを集めるためのマトリックス、4)RNAを複製するリボザイム、4)RNAの安定性を高める、ランダムに形成されたポリペプチドと数種のアミノ酸だ。(図4)
この組み合わせからどう情報(コドン)が発生したのか?
ここで仮に、清水のC4N仮説が正しいとしよう。この仮説では、特定のアミノ酸をキャッチするためにアンチコドンと、ペプチドが相互作用をしている。この時必要とされるペプチドはアスパラギン酸とバリンが結合したジペプチドだ。現代のコドンで表現するとGA(T/C)GT(T/C/A)の配列になる。
2種類のアミノ酸の組み合わせなら、ランダムでも合成するのは簡単で、生命誕生以前にも十分Asn-Valは存在したのではと思うが、 当時10種類前後のアミノ酸存在したと仮定してAsn-Valの組み合わせがランダムに合成される確率は、全ジペプチドのたかだか1%程度だけしかない。このペプチドを確実に十分な量作るためには、記号化されたコドンに従って、2種類のaatRNAを並べ重合させる必要がある。
ではどうすればこれが実現するか?
まずtRNAのアミノ酸と結合する場所(アンチコドンの物理化学的性質が利用されている場所)以外の部位にアスパラギン酸とバリンに対応するアンチコドンを持つ2種類のtRNAが必要だ。これに加えて、マトリックスとなるなんらかのRNA(一番理想的なのはマトリックス+ペプチド転移酵素として働く原始型rRNA自体)に6merのコドンが発生する必要がある。もちろんコドン/アンチコドンの形成は偶然の産物でなければならない。
6merだとこの配列が出来る確率がかなり落ちるので(1Kbに一回)、ここでは計算を簡単にするため、生命以前の原始の世界ではトリプレットコドンではなく、ダブレットコドンだったとしておこう。現在のコドンの冗長性からこう考える人も多い。この場合、tRNA側のアンチコドンはCTがアスパラギン酸、CAがバリンのコドンになる。
アミノ酸キャッチャーとして機能するtRNA5’末のアンチコドンや3’末のNCCA配列は、原始tRNAとしてRNAワールドでは安定に複製・遺伝が行われているとする。このtRNAのどこかにアスパラギンに対応する記号配列が現れる確率は、4×4(16mer)に一回になる。tRNAの大きさを50merと考えると、tRNAのどこかにこのアンチコドンが3箇所は存在することになる。
一方コドンを提供するマトリックスの方だが、ランダムにCTCAが合成される確率は4x4x4x4=256だ。もしマトリックスを提供していると想定している原始rRNAをやはり50merぐらいだと考えると、リボゾームの5個に1個はこの配列を持つことになる。
もちろんリボゾームとは別にRNA鎖を想定してもいい。リボゾームを考えたのは、すでにRNAワールドで複製が行われているRNAである必要があるためで、それが分解して出来た機能を持たない短いRNAでも、それが複製されるなら問題はない。実際、独立したRNAがリボゾームと結合してマトリックスを提供する方が、現在のリボゾームとmRNAの関係に近い。
いずれにせよ、RNAワールドで、ここでリストしたような変化が積み重なることは十分あり得るのではないだろうか。この意図せぬランダムな変化が重なり、2種類のaatRNAがこのCTCA配列を持ったマトリックス上で並んだら、全くランダムだった時の100倍の効率でAsn-Valを合成することが出来る。生産すべきペプチド産物を記号化して指示する独立した情報がここに誕生した。この過程を語る時、どうしても目的論的に語ってしまうが、実際には全てが偶然の過程として起こったことを強調しておく。
一旦この関係が成立すれば、ダーウィンが「もともと生命は、いろいろな力が、一握りの、ひょっとしたらたった一つの原型に吹き込まれて始まり」(種の起源 最終センテンス)と述べた、進化し続けることのできる情報が物質世界に生まれたことになる。この時点ではまだLUCAが誕生したわけではない。最初に吹き込まれたのは、情報だ。情報が誕生するということは、DNAやRNAが誕生することとは別の話で、物質でないコードが、特定の物質と参照関係を確立したということだ。これが達成されるとあとは情報自体が多様化し、さらに新しい大きなペプチド鎖を作ることができる。また、一種類だけでなく、2種類でも、3種類でもアミノ酸配列の決まったペプチドを増やすこともできる。要するにこれ以降は、ダーウィンが進化論で述べたのと同じだ。
最初情報に基づいて作られる特定の配列を持った短いペプチドの重要な機能は、例えば清水の仮説では原始tRNAにアミノ酸キャッチャーとしての機能を与えることであり、またペプチドのRNA保護作用を利用して、多くのRNAを安定化してRNAワールドの持続性と効率を促進することだっただろう。
しかし、できてしまえば多様化する情報断片の威力はすさまじい。こんな小さな情報でも、物理世界に自発的に誕生させることは難しいが、それでもなんとか十分説明が可能であることがわかっていただいただろうか?
今回は私がなんとかひねり出したシナリオを述べた。私でも捻り出せるぐらいだ。他にも十分可能性のあるシナリオが提出されている。次回は他のシナリオについて説明し、物理世界に情報が誕生することがそれほど荒唐無稽なことでないことを再確認したいと思っている。
[
西川 伸一 ]
ゲノム誕生に関する Root-Bernstein の考え
2016年5月2日
ゲノムや生命の誕生について、これまで自分勝手な作り話に基づいて話を進めてきたので、「信用ならん!」と不快に思った読者も多いと思う。一つの仮説を皆さんに押し付ける意図は全くない。実際、38億年前に何が起こったのかを特定することはほぼ不可能だろう。期待したのは、多くの読者が、無生物から生物を発生させることが可能だと思ってくれることだ。
この文章を書き始めた時、無機分子から有機分子、そしてゲノムや生命の誕生など、考える糸口を見つけることすら難しいだろうと思っていた。ところが書き始めて1年もすると、生命誕生について合理的なシナリオを考えること自体はそんなに難しいわけではないと思うようになってきた。そして今は、21世紀にここで述べた様な幾つかのシナリオが必ずだれかによって実験的に確かめられると確信している。
繰り返すが、ゲノム誕生についての個人的理解をくどくどと語ってきた最大の目的は、無機物からの生命の誕生が、多くのシナリオが考えられる、当たり前の科学になりつつあることを皆さんに理解してもらうためだった。
そこで今回は、Root-Bernsteinという研究者が最近の論文で提案しているシナリオを紹介することで、前回述べたRNAワールドからゲノム情報が誕生するまでの過程をもう一度整理したいと思っている。ほとんどの読者にRoot-Bernsteinという名前は馴染みがないだろうが、シナリオは面白く説得力が高い。
図1Root-Bernsteinの論文(Root-Bernstein
& Root-Bernstein, J. Theo Biology 367: 130-158, 2015)に基づいて私が書き直したシナリオ。
まずこのシナリオについて、図1を使いながら簡単にまとめてみよう。このシナリオでは、原始リボゾームを、まだ生物ではないが、独自に、代謝、複製、情報による翻訳と進化の能力を獲得した独立した単位だと考えている。
すなわちリボゾームは、
1)RNAワールド維持に必要なリボザイムセット、 2)自己の塩基配列に基づく自己複製、自己の一部として存在するtRNAとアミノアシル化tRNA合成リボザイム機能、 3)ペプチド転移反応を触媒するリボゾーム中心機能、 4)そしてこれ以外の機能を持ったペプチド合成の鋳型として働くmRNA、 の全てが備わった独立単位として考えられている。
エネルギーや物質代謝については、まだまだ独立しているとは言えないが、熱水噴出孔など自然の条件さえ整えば、Ottoの複製子のように複製、進化も十分起こりうる。しかも、複製時の情報としてだけでなく、アミノ酸に対応する記号化された情報も持っており、これにより様々なペプチド鎖を繰り返し合成し、また進化・多様化させることが可能になっている。例えると、適切な環境条件に寄生するウイルスが誕生したと言ってもいい。
これまで私の話に付き合っていただいた読者なら、Root-Bernsteinの仮説を荒唐無稽だと拒否することはないだろう。ただ、本当に生命誕生の途中段階で、ここに描いたような多様な機能を同時に表現したリボゾームが存在したことを証明できるかが問題だ。これについて、彼らは過去に存在した機能の痕跡は、現存のrRNAにも必ず見つかると考え、研究を続けている。
事実、1983年Blochらは現存のrRNAの配列内に、tRNAの配列の一部が頻回に現れることに気がつき、rRNAとtRNAは同じRNA分子から進化した可能性を示唆した(Bloch et al, J Mol Evol , 19:430-428, 1983)。この発見はその後他のグループでも確認されているが、Root-Bernsteinは彼らのシナリオを提案するにあたって、まずこの可能性を詳しく再検討している(Root-Bernstein and Root-Bernstein, J. Theretical Biology
367:130-158, 2015)。
図2は彼らの論文の図2、図3から転載したものだが、現存の大腸菌のrRNAにも、ほぼ全てのアミノ酸をカバーするtRNAの配列の一部が散らばっていることがわかる。
図2:現存の大腸菌の16S,23S rRNA配列の中に発見された、20種類のtRNA配列。(上記論文より転載)
さらに、こうして大腸菌rRNA内で特定したRNA配列が、tRNAの機能を持つかどうか立体構造を計算してみると、図3に示すように、現存のtRNAによく似た構造を取れることがわかる。
このように、現存の20種類全てのtRNAに、配列上でも、構造上でも相同な配列がrRNAサブユニットの中に発見できるなら、tRNAとrRNAが同じ先祖RNAから進化したことは言うまでもなく、図1に示したようにrRNA自体がいくつかのtRNAが重合してできたものと考えた方が自然だ。
Root-Bernsteinらはこの点について明確には言明していないが、例えばdeFariasらは、まずアミノ酸との相互作用が可能になったtRNAが多様化し、次にtRNA同士が集まってrRNAのサブユニットを形成したというシナリオを提案している(deFarias et al, Life 6:15, 2016)。
図4はdeFariasらの論文から転載したものだが、tRNAは、その本来の機能であるアンチコドンも、また現在mRNAが担うコドンも両方備えており、それが重合することで、rRNAがmRNAとtRNAの両方の機能が備わった単位になるというシナリオを提案している。
さて、図1と図4をよく比べると、原始リボゾームをRNAワールド本来の代謝や複製に加え、転写翻訳のための全システムが備わった独立した単位として考える点では、図1で示したRoot-Bernsteinらの考えとほぼ同じと言っていいだろう。
さてこのシナリオでは、原始リボゾームで最初作られていたタンパク質は、専らこのrRNAにコードされたtRNAやmRNA、そしてrRNAを安定化する作用を持っていたと考えられている。というよりは、安定化に関わるペプチドやタンパク質を作る情報を持つrRNAが自然選択されたと考えている。即ち、リボゾームが自然選択をうける一つの単位として完成していることがよくわかる。
では、本当にrRNAの中にタンパク質やペプチドをコードする配列は存在したのだろうか。例えば現存のrRNAには50種類以上のタンパク質が結合しているが、これらはrRNAにコードされているのではなく、rRNAをコードするゲノム部分とは異なる場所にコードされている。
実験の詳細は省くが、それぞれの配列の比較からRoot-Bernsteinらは、先に列挙した
1)リボゾームタンパク質をコードする配列、 2)rRNAの複製を支えるRNAやDNAポリメラーゼの配列 3)核酸代謝に関わる酵素の配列 4)これ以外の機能を持った、ペプチド合成の鋳型として働く配列、 の全てが、実際にrRNAの中に特定出来ることを示している。
このことは、最初rRNAの安定化に関わるタンパク質を合成していたリボゾームが、効率の悪いリボザイムに頼っていたRNA複製機能や、アミノアシル化tRNA合成機能をタンパク質に置き換える中心的役割を担ったと考えられる。
図5は、大腸菌の23S,16S,5SrRNA内にそれぞれ認められる現存のタンパク質をコードする配列の断片をプロットしたものだが、赤で示したリボゾーム結合タンパク質以外に、DNAやRNAポリメラーゼやtRNA合成酵素を含む多くの機能タンパク質遺伝子に対応する配列がrRNA内にこれほど認められるのは驚きだ。
これらの結果を基礎に、Root-Bernsteinたちは、地球上のタンパク質の全ては、このrRNA内にコードされていた遺伝子に由来するのではと提案している。
以上、今回紹介したRoot-BernsteinやdeFariasらのシナリオをもう一度まとめると次のようになる。
1)原始rRNAはRNAワールドのから誕生した、独立したゲノムを持ち進化可能な最初の単位。 2)原始rRNA内には、ペプチド転移反応を媒介するリボザイム、tRNA、ペプチドをコードする遺伝子が存在していた。 3)当時の痕跡が、現在もrRNA内の配列の中に残っている。 4)rRNAで作られたタンパク質は、最初rRNA安定化に関わる分子だけだったが、これ以外の多様な機能(例えばrRNAの増殖)が、ダーウィン進化の結果次々と誕生した。 ただ、rRNAはいくら脂肪膜で囲まれていたと言っても、生物ではない。次回は、このrRNAからLUCAへの道を考えてみたい。
[
西川 伸一 ]
原始リボゾームからゲノムの誕生
2016年5月16日
前回 紹介したRoot-Bernsteinの原始リボゾームの仮説は面白いだけでなく、生命誕生過程の構想に重要な示唆を与えてくれる。そこで今回はまずこの説を中心にしてこれまでLUCA誕生について議論してきたことをおさらいしておこう(図1)。
先ず、熱水噴出孔でエネルギーと有機物の生成システムが形成され、ランダムではあっても様々な長さのRNAが持続的に供給されるようになる(図1 step1 )。RNA自身は4塩基の組み合わせからできているが、多様な立体構造を取ることができるため、その構造の持つ触媒活性を通して、ランダムで多様化する有機合成反応を一定の方向に制約する可能性を持っている。例えば、一定の構造を持つRNA鎖が高い頻度で合成されるようになる可能性だ。
さらに、RNA同士を結合させるリガーゼ活性、塩基配列に基づいて複製するポリメラーゼ活性を持つリボザイムが生まれると、特定のセットのRNAを増幅・維持するRNAワールドが誕生できる(図1Step2 )。RNAワールドの重要性は、何よりも塩基配列を鋳型として複製することで、同じ構造を増幅できる点、及び個別のRNA鎖が持つ触媒活性を媒介にして、相互に作用し合う分子群をひとつの単位として統合できることだ。
周りの条件にもよるが、RNAには安定性の問題がある。おそらくこの解決としてアミノ酸やペプチドとRNAの相互関係が始まったのだろう。ペプチドと言っても、当時自然に合成できたアミノ酸がランダムに結合したペプチドだったと考えられるが、それでも十分なペプチドを作るためには、環境中に低い濃度で存在しているアミノ酸を捕捉して濃縮する働きを持つ原始tRNAが必要になった。比較的安定なtRNA様構造を持ち、ペプチド合成の効率を上げてRNAワールドを安定化させるという利点を持つ原始tRNAが一旦RNAワールドに誕生すると、選択的に複製されることで自然に濃度を高めるだろう (図1step3 )。そのうち、アミノアシルtRNA合成能力獲得してより安定にペプチドを作る独自の進化を遂げたと考えられる。もちろんペプチドを合成するためにはtRNA進化と並行して、アミノ酸転移活性を持つリボザイムもRNAワールドでは選択的に増殖したはずだ。
こうしてレパートリーを増やしてきたtRNAやアミノ酸転移活性を持つリボザイムが原始リボゾームへと統合される契機については想像でしかないが、リボゾームとしての機能発揮に必要なRNAを別々に複製するより、一つの単位として複製した方が都合のいいことは十分理解できる(図1step4 )。
このような契機から、tRNAやリボザイムRNAが少ない数のRNA鎖に統合されて誕生したリボゾームは、エネルギーや物質代謝に関しては熱水噴出孔の環境に依存する寄生体と呼べるが、1)自己複製能、2)ペプチド合成能、3)そして翻訳のための鋳型としてのmRNA機能を持つ、「自己の誕生」とも言える一つの単位を形成する。
同じ自己複製能を持つOttoの複製子と比べると、自らを鋳型として複製できる点、ペプチドを合成する「翻訳機能」を持っている点で、はるかに高度で独立性の高い複製子がリボゾームとして誕生したと考えることができる。
以上が、deFariasやRoot-Bernsteinが考える原始リボゾームを中心とした大まかなシナリオだが、LUCAへの過程で重要な次の一歩は、情報の機能からの独立だと私は思っている(図1step5)。
RNAワールドでは、RNAが情報を担う媒体としての機能と、リボザイムとしての機能という二役を演じていることが重要だが、情報の独立とは、この一人二役が解消され、情報を担う媒体としてのRNA鎖と、様々なリボザイム機能を担うRNA鎖が完全に分離することを指す。事実現存の全ての生物のゲノム情報はDNAを媒体として、原則として情報以外の機能を併せ持つことはない。
情報が独立することは、ダーウィン進化にとって極めて重要な要件だ。例えば、DNAは情報の媒体以外の機能を持たない。このおかげで、細胞や個体という全体の中の一部であっても、全体からの制約を受けずに情報自体を比較的自由に変化できる。もちろん、情報が変化することで全体の維持が不可能になると、多様化した情報も消失する。とはいえ、情報の変化自体は全体の制約をほとんど受けないことが重要だ。
一方、現存のリボゾームの構造を見てみよう。図2はWikipediaから借りてきた50SリボゾームRNAの構造だが、RNAが折りたたまれ、一つの構造を形成しているのがわかる。
図2 50Sリボゾーム(Wikipediaより) 青で示されているのがリボゾームタンパク質で、残りはRNA.
この一部がmRNAの機能を併せ持つ場合、この部分は50SRNAの機能や構造の維持に必要とされ、この部分で起こる変異は即座にリボゾームの機能喪失につながる。即ち、情報としての自由な変化は最初から制約されてしまう。
このためダーウィン進化で見られたようなほとんど無限と言える情報の多様化がRNAワールドで可能になるためには、制約の源となる様々な機能から解放され情報に特化したRNA鎖が発生することが必要になる。そして最後に、RNAワールドでの配列情報を全てDNAに置き換えて、全体を情報に特化させる転換が必要になる。
この情報の独立が原始リボゾームでどのように起こったかについての私の妄想を述べよう。まずrRNA配列のどこかに、リボゾーム維持に全く影響しない余分な配列が生まれる(図3)。この部分はリボゾームとしての機能を持たないが、rRNAと一体化しており、複製もリボゾームの一部として行われる。このはみ出したRNA配列が、tRNAのアンチコドン部位が結合するコドンを提供するmRNAとして働きだすと、リボゾームの機能から独立した情報としてダーウィン進化が可能になり、多様な新しいペプチドが作られるようになる。すなわち、リボゾームの機能にとらわれず、様々なペプチドを合成して、自由に試してみることができるリボゾームが誕生する。
しかし、おそらくこのはみ出し部分だけが情報媒体として独立することはないだろう。というのも、このはみ出し部分がmRNAとして機能するためには、リボゾーム全体の存在が必須だ。このため、このはみ出し部分は、rRNA以外のペプチドを作るための進化する情報として存在しえても、rRNAから独立することはできない。
したがって、完全に独立した核酸を媒体とする情報が誕生できたとすると、この情報はrRNA(その内部のtRNAも含む)をはみ出し部分と合わせてコードする必要がある。例えば、rRNA配列全体を全てDNAに置き換えることができれば(すなわち逆転写が起これば)、一挙に情報に特化した核酸媒体を誕生させることができる(図3)。しかし、逆転写酵素、あるいは逆転写リボザイムが都合よく突然現れて、情報を独立の問題を一挙に解決すると考えるのは虫が良すぎる。
これまで触れてこなかったが、実を言うとRNAワールドでも、複製を維持するためには、機能のない相補的RNA鎖が作られ、それを鋳型として機能的RNA鎖を合成する必要がある(図3)。従って、機能の制約を受けない情報に特化したRNA鎖がRNA ワールドでは常に合成されていたことになる。ただ、機能を発揮するための構造化ができない RNAは不安定で、おそらく情報として長続きできなかったはずだ。
ここでRNAポリメラーゼ活性を持つリボザイム自体のヌクレオチド特異性が高くないため、複製時にDNAが取り込まれることもあったと考えればどうだろう。リボゾームとして機能するRNA鎖は、多くのDNAが混じると機能低下につながるだろうが、それでもかなりの機能を維持できたと考えられる。実際、RNAとDNAが混合したアプタマーの機能が現在研究されており、これもリボザイムより安定であるという性質を期待しての研究だ。
一方、複製の鋳型としての機能は、DNAが混じるほど安定化し寿命が伸びる結果、DNAで置き換わった程度が高い鋳型の濃度が上昇し、最終的に完全にDNAを媒体とするゲノムが誕生したと考えられる。すでに述べたように、脂肪酸だけでもDNA複製が自然に起こることがある。一旦情報媒体に特化したDNA鎖が生まれれば、機能を持つrRNAも、多様化するために生まれたmRNA部分も、全てが一つの情報としてまとまる。ゲノムの誕生だ。
ゲノムが独立することで、この複製単位はリボゾームの範囲から拡大し始める。次回はこの自己の範囲の拡大について見ていく。
[
西川 伸一 ]
記号、イコン、インデックス、シンボルと情報
2016年6月1日
しつこいようだが、今回もこれまでの話を繰り返してまとめ直すことにした。もともと生物がどう誕生したかについては、本当の答えを導き出すことは難しい。従って、理論的に説明可能かどうか、何度もなんども考えて納得できるシナリオを書いていくしかない。また説明するときも、これまで議論した過程を表現し直して、なんとか読者の皆さんにも理解していただきたいと思っている。もちろんまったく同じ説明を繰り返すつもりはない。様々な視点から同じ過程を説明し直すことが重要だ。
今回はLUCA誕生へのプロセスを、情報と記号論の観点から見直してみようと思っている。すなわちLUCA誕生の過程でどんな情報がいつ誕生したのかまとめてみたいと思っている。この作業は、ゲノムの誕生を説明するのが目的だが、生物進化とともに新たに現れてきたまったく異なる情報、例えば人間の言語の誕生も視野に入れている。
テレオダイナミックス系の誕生
これまで生命誕生へのスタートラインを、エネルギーと有機物が持続的に合成される熱水噴出孔に生まれた多種類の散逸系の誕生と考えて来た。この過程で有機高分子が発生すると、様々な分子間の相互作用が起こりやすくなり、本来は無秩序な物質やエネルギーの流れに一定の秩序がもたらされる。ただこの分子間の相互作用による秩序や規則性の誕生には、どのような意味でも情報と呼べるものは存在しない。Ottoの複製子で見たように、偶然発生した有機分子が、エネルギーや分子の合成過程を制約して、自己複製まで可能になることもある。しかし、これは分子と分子の直接の相互作用による制約であり、情報とは呼べない。渦を持続的に発生させる流れの中に置かれた石と同じと考えればいいだろう。ただ、この制約は偶然の産物で、物理法則による制約とはまったく異なる。熱水噴出孔で起こっていることをもう一度まとめると、比較的安定な様々な制約要因と、それに制約された「傾向」が生まれ、この傾向が蓄積することで一定の秩序を持った系が生まれるといえるだろう。傾向は情報ではない。これをDeaconはテレオダイナミックス系と呼んだ(図1)。
2月15日の記事 とほぼ同じ)
イコン的記号の誕生
この制約された有機物合成システムからヌクレオチドが合成され、それが重合してポリヌクレオチドが生まれる。RNAポリヌクレオチドの中には様々な酵素活性を持つ物が存在し、リボザイムと呼ばれており、現存の生物の中でも実際にリボザイムが働いている。このリボザイム活性は、反応の制約要因としてはより高度の制約活性を持ち、様々な分子の合成過程に秩序をもたらす。それぞれのリボザイムは塩基が並ぶことでできている。この塩基配列は記号と呼んでいい。しかし、記号だから情報というわけにはいかない。RNAが結局限られた数の異なる塩基の並びでできているため、リボザイムがこの塩基配列に支持されてできているように見えてしまうが、合成自身はランダムに起こっており、何かを指示する情報は存在しない。
このように、塩基配列という記号が直接分子の物理的構造を決める場合、記号論的にいうと、イコン的記号性が発生したと言える。
情報とインデックス記号の誕生
ところが、リボザイム活性を持つRNAポリヌクレオチドの集団の中に、特定のRNA配列を認識してRNA鎖を結合させるリガーゼ活性や、更には塩基配列に従って複製するRNAポリメラーゼ機能を持ったリボザイムが生まれると、RNA鎖の塩基配列が突如反応を指示する鋳型としての機能を持ち、鋳型に従って同じ分子や構造を正確に再生産することが可能になる。具体的には、同じ分子構造を、塩基配列(記号)を鋳型(情報)として繰り返し合成できるという点で、記号がついに情報になったと言える。
このシナリオからわかるのは、リボザイムを構成する塩基配列が分子の構造を決めているとしても、この違いを解釈する仕組み(すなわちRNA ポリメラーゼ)が誕生するまではイコン的記号で、情報性は持たないことだ。言葉を変えると、塩基配列を鋳型として使って、その鋳型に合わせて合成を行う酵素やリボザイムが誕生すると(解釈者の誕生)、塩基配列(記号)に情報としての機能が生まれる。 ではなぜこの塩基配列を情報と呼べるかというと、この鋳型はRNAだけでなく、DNAでも表現できる。しかし同じ配列がDNAを媒体として表現されると、RNAで表現できる構造とはまったく異なる構造が生まれる。一方、鋳型としての機能はRNAでもDNAでも同じだ。この物理的媒体を選ばない点で、複製される塩基配列は情報と呼んでいい。
まとめると情報の誕生とは、塩基配列という記号の誕生ではない。記号が解釈されて初めて情報になる。この意味で、地球上で最初に情報が誕生した時とは、RNAポリメラーゼ活性を持ったリボザイムが誕生した時と言えるかもしれない。こうして誕生したRNAの構造と塩基配列の関係は、塩基配列(記号)が、リボザイムの持つ構造や機能のインデクスになっている点で、記号論でいうインデックス記号と言ってもいいのではと思っている(パースなどのインデックス記号の定義とは異なるが)。
ただこのインデックス記号は、まだ化学的に無関係な物質同士が対応関係を持つ、すなわち本来のRNAとはまったく無関係のアミノ酸がRNA配列と対応する段階、すなわちシンボル的記号には到達していない。(シンボル的関係の代表は言語で、サクラという音の並びと実際の桜には全く実体的な対応関係はない。)
シンボル的記号の誕生
ここで現存の生物が全て持っているDNA-RNA-タンパク質というセントラルドグマを考えてみよう。DNAの塩基配列(記号)は、RNAの塩基配列に転写される。これは、RNAワールドでの複製機能と特に変わることはない。しかし、転写されたRNAを鋳型としてタンパク質が作られる過程は、DNAの塩基配列とtRNAと結合するアミノ酸配列がもともと何の関係もないという点で、塩基配列がシンボル的記号に転換している。
この塩基配列という記号がアミノ酸と対応してシンボル的記号に転換するためには、まず最初にtRNAの誕生が必須だ。ここでは原始tRNAが、RNAワールドを安定化するための短いペプチドを安定的に供給するため、アミノ酸を捕捉して濃縮する目的で生まれたことにしている。
すでに述べた清水らの説 に従えば、原始tRNAが持つアンチコドン配列と、たまたま存在したAsn-Valペプチドが相互作用すると、特定のアミノ酸が捕捉される。ただここで使われるアンチコドン配列(記号)は、決して情報として使われているのではない。ペプチドとともに、アミノ酸を捕捉するポケット構造の部分として使われており、アンチコドンと呼ぶのは、現在の生物と比べて言っているだけだ。したがって、このアンチコドン配列によるアミノ酸把握で配列はイコン的記号として使われているが、情報としての関係はない。
とはいえ、このようなアミノ酸とアンチコドンとのイコン的関係が成立することで、原始tRNAに捕捉されたアミノ酸を濃縮することができ、情報でなくともペプチド合成の効率をあげることができる。この時、原始tRNAが集まるためのマトリックスとして、RNAやDNA鎖が働いていたことは十分考えられる。だとすると塩基配列という記号が、RNAとは全く物理的関係のないアミノ酸と対応したシンボル的記号へ転換するためにはあと一息だ。
原始tRNAがペプチド合成のためのアミノ酸捕捉分子として機能するためには、複数のアミノ酸とイコン的関係を持つ原始tRNA、アミノ酸をtRNAに結合するアミノアシル化活性を持ったリボザイム、集まったアミノアシルtRNAに結合したアミノ酸同士を結合させる、アミノ酸転移酵素活性を持つリボザイムは最低限存在していなければならない。特定のアミノ酸が結合したペプチドが持つRNA保護作用や、一部のペプチドによるリボザイムの機能の効率化などが強い選択圧として働き、このようなリボザイムが化学進化したことは十分考えられる。
この前提が満たされた時、核酸配列という記号がアミノ酸配列と対応するシンボル的記号へ転換する条件が整う。その後のプロセスを順を追って考えてみよう(図4、5)。
まず最初ただのマトリックスとして使われていたRNA(ここでは便宜的にrRNAとしておく)とtRNAの関係が、コドンとアンチコドンが持つより強い結合を基盤にした関係へと移行する必要がある。rRNAやtRNAにアミノ酸をコードするコドンを見つけることは難しくないが、実際にはその配列がどこにあってもいいというわけにはいかない。rRNA上の配列をコードとして集まったtRNAに結合したアミノ酸同士が結合するための十分近い距離に保つ必要がある。
例えば、まずアミノ酸転移反応を制御するrRNAと、tRNAの構造がともに進化して、記号対応関係はないがアミノ酸が濃縮できるマトリックス構造が生まれた後、この結合をさらに強い結合にするために、rRNAの一部がコドン配列を特定の場所に持つように進化すると考えてみよう。
この時、清水らの説のように、アミノ酸をキャッチして3’端にエステル結合させる過程で、tRNA5’末のアンチコドン配列が物理的(イコン的)記号の働きができるとかなり話が早い。すなわち、アミノ酸補足後アミノアシル反応が終わり、3’末にアミノ酸が結合した後、フリーになったアンチコドン部分がマトリックス側に現れたコドンと結合して、tRNAの結合を強め、アミノ酸転移反応の効率をあげると考えれば、選択されるのはrRNA側の配列だけになり、考えやすくなる。すなわち、tRNAのアンチコドンは最初からイコン的記号として存在し、rRNA側のコドンが選択された時に初めてシンボル的記号に移行すると考えるのは、そう難しくない。
このシナリオの問題点は、マトリックス側に偶然現れるコドン配列の長さに限界があることだ。実際、2−3アミノ酸分が関の山だろう。とすると、必要なペプチドごとにそれに対応するコドン配列を持ったrRNAが必要になってしまう。
これについての一つの答えは、まず「簡単なものから始めて見る」ではないかと思っている。すなわち、実際多様なrRNAが存在する中で、RNAワールドにとって最も必要なペプチドに対応するコドンを持ったrRNAが選択的に増殖したと考えればいい。短くてもシンボル的記号としてのコドン部分が選択されたrRNA上に生まれれば、この部分は増大し多様化できる。
例えば最初単純な言葉が生まれ、そこから複雑な言語が発達するのと同じだ(この点については後々考察する)。簡単な記号を元にシンボル的関係を成立させることがまず重要だ。
あとはこのコドンを持ったマトリックスを独立させ、DNA化することで生命の情報システムは完成する。この過程についての一つの可能性はすでに前回述べた。
以上のシナリオをもう一度記号論的にまとめると、
1)有機分子の合成と、分子間相互作用を介する制約による有機ワールド(テレオダイナミックス状態)の成立 2)分子構造が塩基配列(記号)により決まるリボザイムの誕生(イコン的記号の誕生) 3)核酸配列(記号)を鋳型として使って複製するリボザイム(記号の解釈者)の誕生=インデックス記号の誕生、 4)tRNA上の記号(アンチコドン?)とアミノ酸とのイコン的関係の誕生、 5)tRNA上のアンチコドンを選択圧としたrRNA側のコドンの誕生により、塩基配列のシンボル的記号への移行。 6)シンボル記号のダーウィン進化。 今回は生命誕生について、生命情報成立をより強調して説明した。次回は原始リボゾームからLUCAへの過程について考えるが、この記号論は、今後様々な生命情報を考えていく上で共通の基準をあたえてくれる。
[
西川 伸一 ]
進化の始まりと目的の実現
2016年6月15日
前回のまとめは理解していただけただろうか?
特に、核酸配列がイコン(類似)記号、インデックス(指標)記号、シンボル(象徴)記号へと発展した点についての説明は理解して欲しいと思っている。
図1チャールズ・サンダーズ・パース
この稿で、核酸配列をイコン、インデックス、シンボル記号に分類したのは、言うまでもなくアメリカの巨人チャールズ・アレクサンダー・パースの考えをそのまま拝借している。パース(図1)はプラグマティズムの創始者として紹介されることが多いが、一つの枠で語れない偉大な巨人で、その記号論は言語や核酸配列などの生命情報を整理する上で欠かす事が出来ない(ぜひ読んで欲しい)。
RNAに、4種類の塩基から出来ているという記号性と、それ自身で酵素活性を持つ2面性が存在することが、複製可能な有機システム=RNAワールドを可能にしたが、このとき最初からRNAが情報として働いていたと思うと大きな間違いを犯す。
配列が情報としてRNAポリメラーゼに解釈されようになるまでは、配列=構造という単純な物理関係があるだけで、この時の配列は記号ではあっても情報でない。このことから、これをイコン記号とした(図2)。
ここにRNAポリメラーゼが誕生すると、塩基配列を解釈する過程が始まり、塩基配列がインデックス記号に変化する。最後に、アミノ酸配列と核酸配列という全く無関係な物質同士がtRNA+rRNAの誕生で対応するようになると、塩基配列はシンボル記号になる。重要なのは、イコン記号及びインデックス記号の段階では、記号(塩基配列)とそれに対応する機能分子との間には、物理的法則に基づく対応関係があるだけだ。ところが、核酸配列がシンボルの記号になると、核酸配列とは全く関連性のないアミノ酸配列に記号が対応する。このことは、物理化学とは異なるルールがこの記号に導入されたことになる(図2)。
勿論非物理的対応関係を媒介するのはtRNAとrRNAという現実の分子だが、核酸配列がシンボル記号としてアミノ酸配列に対応するようになるためには、これまで述べたような固有の歴史を通してそれぞれの関係性が生まれる必要があり、この歴史性は物理化学的法則にはない。このように、シンボル記号誕生こそが、物理科学法則に支配される地球に、新しい情報という因果性が誕生したことを意味する。そして、地球上にダーウィン進化が始まる。このダーウィン進化の始まりについて見ていこう。
核酸配列がイコン記号として働く段階では、同じ記号(=物質)が生まれるかどうかは偶然に支配されており、できる分子は無秩序に多様で、この段階の有機物質やエネルギー合成は無秩序なカオス状態と言っていい。ここに、核酸配列が複製のためのインデックス記号として働く情報化が起こると、分子の多様性を減らし、秩序をもたらす方向に進む。このように、もともと情報とは系に秩序をもたらす方向に働く。ただ、秩序を生み出す複製過程においても、一定の制約の中での複製エラーによる変異が核酸配列に起こる。この秩序という制約の中での多様化こそがダーウィン進化の原動力になる。
このように、生命とは呼べないが、原始リボゾームのような複製する原始ゲノムが誕生した時代を考えてみよう。RNAで代謝の多くをまかなうことができるとはいえ、有機物生産システム、エネルギー生産システムなど多くの生命に必須の条件はRNAのみで達成できない。従って、RNAワールドをコードする原始ゲノムは、環境の中に寄生したRNAウイルスのようなものとして考えればいい(しかし、私たち人間を含む現在の生命も結局環境に寄生しているが)。お分かりのように、私は生物の始原はゲノムから始まると考えている。
もともと生命をDNAから考える有名な仮説がリチャードドーキンスの「利己的遺伝子」仮説だ(図3)。現存の生物の進化について利己的遺伝子仮説が当てはまるかどうか議論がつきないようだが、LUCA誕生直前の状態を考えれば、妥当な仮説だと私には思える。
即ちLUCA誕生前の状態を、熱水噴出孔の特殊な環境に寄生しているRNA/DNA寄生体(利己的遺伝子)が、この環境から自立する過程として捉えればいい。未だ生物は誕生していないが、将来のゲノムの核になる原始ゲノムは既に存在している。この原始ゲノムが自立するためには、環境を形成している様々な分子を自分の中に取り込み同化する必要がある(図4)。
環境を形成する分子がRNAやDNAでできている場合は、その配列を融合により同化すればいい。そうすることで、環境分子は複製により安定して調達されるようになり、自然と原始ゲノムのゲノムサイズが上昇する(図5)。
環境分子が核酸でなかった場合、原始ゲノムを多様化して新しいリボザイムを合成し、環境分子の機能と一番フィットした原始ゲノムを選択することで同化が可能になる。
もちろんこの様式で環境分子を同化してもいいが、RNAワールドには限界がある。RNAワールドでの核酸配列はインデックス記号であり、記号がそのまま物理的性質と直結する。このため、核酸レベルの構造が制約となり、多くの環境分子に対応する機能分子に対応する記号を合成することは制限される。
RNAだけで環境分子を同化していくことには他の問題もある。ゲノムサイズが大きくなると、ポリメラーゼ・リボザイムと相補的塩基配列がペアリングする危険性が高まり、複製の効率が落ちると予想できる。また既に述べたように、RNAの安定性を高め、機能を補完するためにもペプチドが必要になる。従って、原理的にはRNAだけで環境の同化を進めることは可能だが、核酸配列が物理的に制限されることなく機能や物質と対応できるシンボル記号へと転換することで、更に自由な同化が可能になる(図5)。
この同化を繰り返せば、環境依存性が少しづつ低下していく。すなわち、より多様な環境で存在することが可能になる。これを繰り返してLUCAができると考えること自体は、私は、論理的にも無理はないように思っている。
面白いのは、RNA機能分子を原始ゲノムに融合する様式では、自然選択は全く必要ない点だ。一方、原始ゲノムを転写し、その産物で環境分子を置き換えられるかどうかを試す様式では、最も環境分子に近い分子を合成できる原始ゲノムが自然選択される。これは、水平遺伝子伝搬とダーウィン進化の共同作用による進化のルーツのように私には思える。
最後に強調したいのは、LUCA以前の、環境分子同化過程でのダーウィン進化では、原始ゲノムが同化すべき環境分子がすでに存在している点で、これは生命誕生後のダーウィン進化と決定的に異なっている。
ダーウィンの進化論は、目に見えない因果性、すなわち「目的」に駆動されているように見える生物進化が、多様性の獲得と自然選択のダイナミズムで説明できることを示し、最初に目的が存在することを拒否している。一方、原始ゲノム(利己的ゲノムと呼んでもいいかもしれない)が環境から自立しようと進化するとき、最初から同化すべき環境分子が目的として実在している(図4)。もちろん最終的にゲノムが同化された記号は、必ずしも同じ分子に対応する必要はなく、機能が維持できればいい。しかし、最初から手本として、目に見える分子が進化の方向を示す目的として存在していたことが、LUCA誕生前後のダーウィン進化の大きな違いであることは強調しておきたい。
あと生命誕生まで、自己という単位が、原始ゲノムから細胞へと拡大する過程が残っているだけだ。
[
西川 伸一 ]
生きた細胞の再構成は可能か
2016年7月1日
これまで断片的にではあるが、生命誕生を考えるための様々な条件、あるいはシナリオについて解説してきた。多くの読者の方が、「条件さえ整えば無生物から生物が生まれる過程を構想することは全く不可能ではない」と考えてもらえる様になったのではと期待している。
このシナリオで最も重要なゴールは転写(ポリメラーゼ)機能+翻訳機能(tRNA+rRNA)を備えた原始ゲノムの誕生だ。もちろん原始ゲノムの誕生には、その維持と複製を支持する環境条件が必要だが、一旦誕生すると、この原始ゲノムはオーガナイザーとなって、環境を構成する分子を一つ一つ同化し、環境から独立しLUCAに至る。原始生命と呼べるのはLUCAが最初だが、最も重要なスタートラインは原始ゲノムの誕生と考えている。
40億年前の地球で起こった詳細をこのシナリオが説明できているとは到底思えないが、環境がまず形成され、それに寄生する原始ゲノムが誕生し、環境を自己に同化するという順番はおそらく間違っていないのではと思っている。
このシナリオでは、生命誕生に必要な分子は、もともと熱水噴出孔での「有機化学法則」に従って、個別に合成されるもので、各過程は独立に進み、組織化されてはいないと考える。従って、熱水噴出口の中のマイクロセルには、たまたま存在する分子ごとに多様な環境が形成されている。その中の一部の条件が、RNAワールド(イコン・インデックス記号的段階)から原始ゲノムへの進化の発展を支えることが出来たのだろう。これは全て熱力学と、非平衡熱力学が支配する過程と言っていい。
原始ゲノム誕生までの条件が地球上に揃う過程を頭の中で考えるのは簡単だが、これが実現するために必要な有機物の合成が維持される環境を、地質学的に十分長い時間維持することはそう簡単ではない。その意味で、地質学的時間一定の状態を維持できる熱水噴出孔の存在は欠かせない。この時、原始ゲノム誕生までに最低限いくつの分子が必要か決めることは、重要な課題だろう。というのも、タンパクや脂質の合成が互いに制約しあって一定の秩序を持って行われるとしても、この段階までの合成は原則ランダムで組織化されていない。必要最低限の数があまりに多いと、ランダムな化学合成ですべてを揃える確率は当然低下する。
ではいくつの分子が原始ゲノムの独立に必要だったのだろう?
実験室の環境で自律的生物を維持できる最小限の遺伝子数については、CJ Ventorのグループが精力的に研究を続けている。全部あわせても517個の遺伝子しか持たないマイコプラズマにトランスポゾンを感染させ、多くの遺伝子を同時にノックアウトする方法で、どの遺伝子が生存に必要かをしらみつぶしに探索した研究が1999年にScienceに発表された(Hutchinson III et al, Science 286:2165, 1999)。
たかだか265−350個の遺伝子で自律生命が維持できるというVenter達の結論には、無生物から生物への再構成過程を研究できるのではと私も興奮した。この数は、その後トランスポゾンの挿入された個々の遺伝子を丹念に検討し直す研究から、382個へと上方修正されている(Glass et al, PNAS 103:425, 2006)。それでも400弱の遺伝子があれば、実験室の環境で自律生命が可能であると理解すると、生物合成が手の届くところにきた様な錯覚に陥る。
しかし、生命誕生に必要な最低限の遺伝子数が400だとしても、これらが全て揃って地球上に生命が誕生できたようには思えない(計算根拠はない)。即ち非平衡熱力学過程から秩序がもたらされるとしても、億年単位の時間内に400全ての分子が地球の特定の場所に同時に出現する状況を考えるのは難しい。
幸い、熱水噴出孔の物理的条件の安定性については信頼できる。このため、原始ゲノムの存在した環境形成には、合成されたRNAやペプチドだけでなく、熱水噴出孔自体が提供する条件(例えば無機質の触媒作用や、プロトン勾配など)の果たした役割が大きいと思われる。従って、原始ゲノムが独立するまでには、環境を形成するRNAやペプチドの同化だけではなく、新しい機能を持ったRNAやペプチドを合成する情報を獲得することが必要だったと考えている。もし原始ゲノムがこの課題をクリアーできるだけの十分な能力を備えていると確信できれば、LUCA誕生は説明できたのと同じだ。
記号性を持ち、この記号を拡大・複雑化できるとともに複製能を持つ原始ゲノムは、生命ではなく、まだ環境に寄生しているが、多様化、自然選択、選択された個体(原始ゲノム)の複製を通したダーウィン進化を行う能力が備わっており、この過程を介して、環境の分子を同化し、また新しい分子を開発して環境から独立して生命誕生へと発展できる。すなわち、ダーウィン進化が可能な原始ゲノムが誕生した時点で、生命誕生のための基盤は全て整った。
ここで一つ思考実験を考えてみよう。生命最小単位マイコプラズマを集めて破砕し生きた細胞を消滅させる。こうして用意した、細胞内に存在する全ての分子が最適な濃度で維持されたマイコプラズマスープを、必要なら栄養やエネルギーを外部から適宜加えて維持できるとしよう。ゲノムの複製、転写、タンパク質の合成などが十分可能なスープだ。そこに合成された完全なマイコプラズマゲノムを投入すれば、もう一度生きたマイコプラズマが発生するだろうか?もし原始ゲノムがLUCAに発展するなら、マイコプラズマが発生しても不思議はない。
私の答えはノーだ。マイコプラズマの細胞質の条件を全て維持でき、その中でマイコプラズマゲノムが複製できたとしても、生物は生まれないだろう。なぜなら、この条件で、ゲノム自体がマイコプラズマの自己とは何かを決める事が出来ないからだ。一方、マイコプラズマのゲノムを外来のゲノムで置き換える実験は行われている。
詳細は省くが、合成ゲノムは先ず他の系統のマイコプラズマに移植されている。この時、移植した宿主マイコプラズマが持っていたゲノムを除去する操作は、この実験では行われていない。即ち、合成ゲノムを移植した段階で、宿主のゲノムと、移植した合成ゲノムの両方が共存する時期を経て、薬剤選択により宿主のゲノムが排除され、移植ゲノムが残る方法を用いている(図1)。実際にはこの方法は開発にはずいぶん苦労したようで、その難しさは2007年に発表された論文から窺い知ることが出来る(Lartigue
et al, Science 317:632, 2016)。
ただここで注目したいのは、この苦労話ではなく、単離したゲノムは先ず生きているマイコプラズマに移植しないと、ゲノムとして働けないことだ。すなわち、ゲノムが細胞内の様々な過程を組織化するための情報として働くには、細胞が先に生きている(=組織化されている)状態を維持していることが必須である点だ。「卵が先か・鶏が先か?」の生命特有の問題がここでも現れる。
では、宿主のゲノムを除いても、合成ゲノムを移植することは可能だろうか。私は可能だと思っている。しかし、バクテリアから細胞質や細胞膜を傷つけずに残してゲノムだけを除去することは技術的に極めて難しく、このような挑戦が行われていないだけだ。
事実、細胞の操作が可能な十分な大きさを持つ脊椎動物の卵子では、核を取り除いた後、他の細胞から単離してきた核を注入し、ゲノムが完全に入れ替わったクローン動物を作ることが出来る(図2)。
更に当時理研・発生再生科学総合研究センターの若山らは、細胞としては死んでいることが確認された脳細胞から核を取り出し、それを卵子に移植する事でクローン動物が作成できることを示し、ゲノム情報の維持には必ずしも細胞が生きている必要がないことを示している。従って、生きた細胞を宿主とすれば、宿主のゲノムの有無にかかわらず、ゲノムは働くことが出来る。
ではなぜ原始ゲノムは熱水噴出孔の環境で生命へと発展できるのに、マイコプラズマゲノムはマイコプラズマスープの中で生命へと発展できないのか? また、マイコプラズマスープの中で新たなマイコプラズマが出現しないのなら、熱水噴出孔の環境がどれほど完全でも、原始ゲノムからLUCAが発生することが、本当に出来るのだろうか?これを理解する鍵が自己性だ。
マイコプラズマスープにマイコプラズマゲノムを混合しても生命が発生しない理由を考えると、原始ゲノムと違って、マイコプラズマゲノムは進化の過程で情報に特化してしまい、既に生物の部分になってしまっているからだと言える。
すなわち、原始ゲノムはそれ自身で自立しており、自己性=全体性を持っている。一方、マイコプラズマゲノムはマイコプラズマスープの中で、複製し、タンパク質やRNAやタンパク質を合成出来たとしても、自己性=全体性は失ってしまっている。即ち、マイコプラズムの自己は、ゲノム、細胞膜、細胞質も含めた全体へと拡大している。単細胞生物の自己は、細胞膜で囲まれた内側にあるゲノムも含めた全てで、決してゲノムだけでない。このため、生きた細胞にゲノムを移植する方法で自己の範囲を明確に与えるという過程を踏まないと自己性は生まれない。細胞質スープの中でゲノムが自己組織化を通して細胞としての自己を自然発生させる可能性はあるにしても、その確率は低い。
少しわかりにくい議論になったが、進化により自己性の範囲が拡大することは、我々人間を含む高等多細胞動物を考えるともう少しわかりやすい。
例えば人間の自己は、決して身体の範囲内に制限されているわけではない。例えば私が今書いている原稿も、やはり私の一部だと言える。一方、意識がなくなった私の身体は、生きていたとしても人間としての自己性を失っている。すなわち、神経ネットワークというゲノムとは異なる情報を獲得することで、生物の自己の範囲は広がった(これについては、ゲノムの進化について考えるときもう一度考える)。原始ゲノム、LUCA、そして人間と、自己性が生物の全体を決め、進化と共に自己性の範囲を拡大させ環境を取り込んできたのが生物だ。
この自己性の拡大とは、環境の自己への同化の過程とみることができる。そしてこのことが最もはっきりわかるのが、原始ゲノムが環境を同化していく過程だ。要するに、情報性と自己性を持つ原始ゲノムが誕生すると、原則として無限の新しいタンパク質を作る能力が得られる。ただ、自己性の問題からわかるのは、完全な自己性を維持しているゲノムだけが、環境を統合した拡大自己を発展させることができる点だ。
一端ゲノムが自己の部分になってしまうと、もうゲノムが自己性を決める事は出来ず、従って生物は発生しない。ゲノムは今後は、自己のなかで、情報を担う部分として進化の駆動力として、多様化と複製に関わる。
どうだろう。生物が生まれる一つのシナリオは理解してもらえただろうか。もし疑問があれば、これからはそれに答えることも行いたいと思っているので、問題点を指摘してほしい。
ゲノムは誕生した。次回からはゲノムやゲノム以外の情報の進化について考えていく。
[
西川 伸一 ]
ゲノムの進化と生物の進化
2016年7月15日
ゲノムの解剖学に始まり、ゲノムの生理学、そしてゲノムの発生学と、すでに27回にわたって ゲノムに関する知識を独断で、しかもほとんどは自分の頭の整理のために書いてきた。特に後半17回はゲノムの発生学と称して、今私たちが知っているゲノムが、生物のいない地球でどう誕生したのか、思いつくまま書いてきたが、そのおかげで自分では無生物から生物が生まれる過程を頭の中で思い浮かべられるところまで整理ができたと思う。ただ、説明自体は体系的でなかったので、読者の方にはわかりにくかったのではと反省している。私の個人的な頭の整理に付き合っていただいた読者の皆さんにはまず感謝。
私自身は納得できたと満足していても、読者の多くは生命誕生の話がまだ完結していないという印象を持たれたかもしれない。事実、ゲノムの発生学についてのシナリオは原始ゲノムまでで終えてしまったことは確かだ。
本来なら最終生物(LUCA)への移行過程の説明がくるはずだが、「原始ゲノム=自己」が「ゲノム<細胞=自己」という構造へと移行して、自己の範囲が拡大したとだけ述べてお茶を濁した。
しかしこれには理由がある。私はLUCAへの最終過程は、無生物から生物への過程より、生物のダーウィン進化のなかで理解したほうがいいと考えている。場合によってはダーウィン進化は今もゲノムの多様化と、選択の問題として語られる。しかし、ゲノムの発生以降、生物進化は様々な情報をゲノムの外に生み出してきたため、生物の進化をゲノムの進化としてだけ捉えることは難しくなった。私はこの問題は、原始ゲノムの代表する自己が、細胞を単位とする自己へと拡大した過程で最初に発生したと思っている。
原始ゲノムは現在の生物に普通に見られる様々なメカニズムにより情報を拡大させ、環境を自己に取り込むことでLUCAへの道筋を突き進んできた。しかし、生物の自己が完全に細胞に拡大してLUCAが誕生するためには、拡大したゲノム情報だけでは足りない。この困難は原核生物の細胞分裂過程をみるとよくわかる(図1)。
原核細胞のゲノム複製は、細胞が成長して一定の大きさに達したときに開始する。すなわち、原始ゲノムから見たとき拡大した自己=細胞の大きさを情報としてゲノムの複製開始が指令される。実際には細胞のサイズ情報を受けたdnaAと呼ばれる分子が複製開始点に集まり、ゲノムの複製が始まる。次にゲノムの複製が終わると、これが情報となって、細胞の中央がくびれ、細胞中隔が形成された後、細胞が分裂する。すなわち、今度はゲノムの状態が情報として細胞質の分裂を指令する。実際にこの分裂は、ゲノム複製に関する情報に反応してFtsZと呼ばれる分子が分裂面に集まることで進む。もし複製終了を情報として確認するメカニズムがなく、ゲノム複製が終わる前に細胞が分裂してしまったら大変だ。
この過程からわかるのは、原始ゲノムから細胞へと自己が拡大すると生物にとってゲノムの塩基配列だけが情報ではなくなり、複製開始を指令する細胞の大きさや、逆にゲノム複製の状態が情報となって細胞分裂過程の進行を調節していることだ。おそらく原始ゲノムは最初から脂肪膜でできたマイクロセルの中に存在してプロトセルを形成していたのではないかと考えられる。ただ、マイクロセル形成と、原始ゲノムは基本的には独立していたはずだ。(季刊生命誌89号 に人工細胞研究の記事がある)細胞質・細胞膜とゲノムが独立しているプロトセルを考えるのは簡単だ。しかし自己が細胞として統合されるためには、原核細胞に見られるゲノムから細胞質、細胞質からゲノムへのシグナルが必要になる。すなわち細胞の大きさとゲノムの状態が、核酸配列情報の外に発生する必要がある。
「え?ゲノムの塩基配列以外の情報が発生したの?」と問われそうだ。答えは「イエス」だ。
ずいぶん前に、雨は情報でもなんでもない物理現象だが、外出しようと考えている人にとっては重要な情報として、傘を持って表に出るという行動につながることを例に、一見情報とは思えない現象が、解釈によって人間にとっては情報になることを説明した。まさにこの解釈システム(あるいは感覚システム)が原始ゲノムから細胞への拡大過程で発生することで、塩基配列以外の状態が情報として使うわれていることを意味している。
生命科学になじみのある人なら、今私が説明した機構はフィードバック、フィードフォワード機構として、生体の中では普通に見られるメカニズムだと気づかれるだろう。
生体ではこの機構が、細胞や個体の統合を保つための最も重要な機構として至るところで使われている。すなわち、生体内で起こるすべての独立の過程を統合するには、反応のモニタリングと、解釈、それに従う行動のネットワークが網目のように張られる必要がある。そして、それぞれの回路は、ゲノムからの指令で形成される分子により解釈される、ゲノムとは異なる情報が発生している。
もちろんSzotakらの研究が示すように、新しい情報解釈システムがなくとも、条件が整えばRNAゲノムを持つプロトセルが分裂を繰り返すことは現実にあり得る。しかし、この分裂でゲノムの分裂と細胞質・細胞膜の分裂がうまく調整されているように見えるとしても、それは地球上の偶然が重なりフィードバック機構を持った「間欠泉」ができるのと同じだ。図に示す様に、外界から何らかの力を受けることなく、ゲノムと協調して分裂することはない(Ottoの複製子 を思い出して欲しい)。
この様に、原始ゲノムが誕生してから、生物は自己の範囲を急速に拡大し、これは自己内で起こる様々な現象を情報として解釈する無数の仕組みを獲得することで支えられてきた。例えば、タンパク質のリン酸化、アセチル化、メチル化、あるいはRNAのリボスウィッチなど、すべてこれにあたる。現在cAMPや脂肪酸がシグナル伝達に使われているのも、ATP、脂肪酸がこのとき細胞にふんだんに利用できた名残だろう。この再帰性が、目的性をもった力学系テレオダイナミック系 を特徴付けていることを思い出して欲しい。
この様に新たな情報を解釈して自己の統合性を維持する機構が発展すると、今度は自己だけでなく外界の変化を情報として解釈するメカニズムも発生する。この結果、多細胞体制を支えるエピジェネティックな情報、神経回路情報、脳回路情報、そして最後に言語というそれぞれまったく異なる質の情報が生物から続々誕生してきた。
考えてみると、プロトセルの細胞質や細胞膜は、最初の原始ゲノムにとっては自己ではなく、環境だったと言える。この環境を取り込んで自己の範囲にしたのがLUCAの誕生と言えるが、これにより、その後の進化の方向性、すなわち環境の取り込み(支配)を目指す進化の原動力が決まった気がする。そして何よりも、その過程で例えばゲノム情報の多様化だけではなく、様々な異なる質の情報をゲノムの外に誕生させた。言語を考えてみると、このおかげで自己の範囲は世界の裏側、宇宙の果て、そして生命誕生のときまで広がっている。
これから生物の進化を、これら多様な情報が統合された個体を選択する過程として捉える必要がある。生物の進化をゲノム進化からだけ考えることはできない。次回からは、多様な情報が統合された生物の進化について考えてみたいが、まず生命の進化によって新たにゲノムの外に生まれた情報をリストし、その特徴を考えるところから始めたい。
[
西川 伸一 ]
2019年8月16日
トランプ誕生あたりから、世界は何か騒がしい。ともかく様々なことが起こり、ニュースとして入ってくる。例えば、今日為替が乱高下しているが、これは米国の長期金利が短期金利の利回りを下回るという、逆転現象が起こったからだ。素人から見ると、要するに長期的未来はひどい様に思えるが、ただこの逆転をどう考えるかは分かれる様で、大きな経済後退のサインと見る人と、一時的現象と考える人がいる。要するに今起こっていることの未来への影響を予測するのは難しい。そのおかげでロクでもない評論家が存在できる。
今日紹介するマイクロソフト研究所からの論文はそんな評論家に代わり未来を予測するAIを作ろうとする研究で、Nature Human Behaviour オンライン版に掲載された。タイトルはズバリ「Predicting history (歴史を予測する)」だ。
しかしマイクロソフトの研究所は型破りの人たちが集まっている様だ。論文はヘーゲルの「ミネルバの梟は夕暮れに飛び立つ」というヘーゲル法哲学の引用から始める意気込みで、数理に弱い私たちをもぐっと惹きつける。
もちろん現在の情報をいくらAIにインプットしても、答えがわからないため学習させられない。そこで、1973年から1979年という時代を選び、この時に米国国務省からの電報を集め、この電報の内容とその後の歴史評価の対応付けを、歴史家に読んで評価してもらって計算したPCI(同時代的重要性認識)、国務省内での歴史的評価が定まった文書が集められたFRUS(合衆国外交関係)を比べている。PCIの値はある電報がFRUSに加えられる確率と相関することから、PCIはその時点での電報の重要性をある程度反映できるが、電報のサンプル数が増えると、あまり重要でない電報のスコアも上がっていき、電報の付随データのみから将来の歴史的重要性を予測するのは難しいことが明らかになった。
そこでその時代を切り取り将来を予測する能力の優れた年代記編集者の条件とは何かを考え、その条件を満たせる様なアルゴリズムの機械学習を設計して、コンピュータが重要と判断した電報が実際にFRUS に収載される確率を調べると 、サンプル数が多くてもある程度予測が可能になったとはいえ、予測できるとは到底いえないことが明らかになった。
結局ネガティブデータで終わっており、数理の苦手な私には問題の原因を予測することは難しいが、結局この失敗は、正確に予測できる評論家がいないのと同じことだという感触はある。もちろん始まったばかりで、個人的には優れたAI評論家が生まれることは可能ではないかと期待している。
2019年8月15日
自閉症の科学シリーズとタイトルをつけましたが、今日紹介したい論文は、胎児期に治療できる可能性がある遺伝病があることを示した研究で、自閉症とは直接関わりがないことをお断りしておいたほうがいいでしょう。しかし、自閉症の多くは胎児期・発達期の神経ネットワーク形成過程の問題に由来しています。すぐに関係がなくても、胎児期、発達期の治療法の研究は、将来の自閉症治療にもつながる可能性があると考え、シリーズとして紹介することにしました。
XLHED
日本語でも、英語でも、読もうとすると舌を噛みそうな名前、X-linked hypohidrotic ectodermal dysplasia (X染色体連載低発汗性外胚葉異形成症:XLHED)、のついた病気があります。X染色体上に位置するEDAと名前がついた分子をコードする遺伝子の突然変異が原因の病気で、突然変異を持つ男性のみに、1)汗腺の形成不全による発汗障害、2)毛根形成障害、3)歯の数の減少、の3つの症状を中心に、口腔や鼻腔の様々な発生障害が起こります。
これらの症状のうち、体温を調節する汗が出ないことが最も深刻で、体温が上昇し易く、特に子どもの場合死を招いてしまう心配があります。EDAは細胞膜から細胞外に飛び出ている分子で、毛根や汗腺の元になる皮膚上皮細胞を刺激して発生を促しています。これまでの研究で細胞が刺激されると何が起こるのかなど良く研究が進んでいます.
遺伝子の突然変異があっても、もし外から正常のEDAを供給することができれば、この病気を治療することができるはずです。EDAはもともと細胞膜上に存在していますが、細胞膜から切り離しても効果を発揮できることがわかっています。すなわち、効果を持つEDA分子を試験管内で合成できるのです。大事なことは、EDAが毛根や汗腺の発生するときだけに必要で、大人になると必要がなくなることです。実際、成長して病気が完成してしまうと、EDAに反応する細胞は皮膚から消えてしまい、外からEDAをいくら足しても、治療ができないのです。一方、EDAが必要な胎児期や発達期であれば、合成したEDAを外から加えることで、EDAの機能が欠損した子供の病気を治療することができるはずです。
この可能性にチャレンジして見事に成功したのが、今日紹介するドイツ・エアランゲン大学からの論文で、4月26日号のThe New England Journal of Medicineに発表されました(Schneider
et al, Prenatal correction of X-linked hypohidrotic ectodermal dysplasia(X染色体連鎖低発汗性外胚葉異形成症の出生前の治療), The New England
Journal of Medicine, 378:17, 2018: DOI: 10.1056/NEJMoa1714322)。
研究の概要
この研究では、胎児の羊水にEDAを注射し皮膚で汗腺や毛根を誘発しようと考えています。しかし、細胞膜から切り離したEDAは体内ではすぐ分解されてしまいます。また、EDAは重合しないと刺激ができません。このため、EDAをそのまま治療に用いるには、なんらかの方法で重合させた大量のEDAをなんども注射する必要があります。当然このような操作は流産の危険性を高めてしまいます。この研究では、私たちの体の中で最も安定性の高い分子と言える抗体分子の一部(Fc部分)をEDAに結合させ、EDAを安定化させるとともに自然に重合させる戦略をとっています。もちろん、実際の治療を行う前に、マウスや犬を用いて、EDA-Fcを羊水に一回注射するだけで毛の発生を促すことを確認しています。このようなマウスや犬を用いた基礎研究の結果に基づき、実際にこのEDA-Fcを2人の妊婦さんに投与し、3人のXLHEDの子供の治療に成功したのがこの研究です。
治療経過と成績
今回選ばれた妊婦さんは、以前にXLHEDを持つ子供を出産し、今度の妊娠でも子供に同じ遺伝子変異が伝わっていることが出生以前遺伝子診断で確認できている二人です。出生以前に遺伝子診断が確定すると、人工中絶を選ばれるお母さんも多いのですが、このお母さんたちは子供を望まれ、胎児期の治療の可能性にかけてみられたのだと思います。二人のお母さんのうち1人は双子を妊娠しておられたため、治療の対象となった子供さんは三人になります。
治療は妊娠26週と31週の2回、胎児の体重1kgあたり100mgのEDA-Fcを羊水中に注射するだけす。羊水への注射は常に流産の危険を伴いますが、おそらくどの病院でもその気になれば実行可能な方法だと思います。
最初の子供たち(双生児)についてですが、EDA-Fcの注射で汗腺の発達という点ではほぼ満点の治療成績を示しました。命に関わる汗腺の形成はほぼ正常レベルに回復して、実際に2歳まで発熱の発作は全く起こらなかったようです。さらに歯の数や、唾液腺、涙腺などもほぼ正常に回復して、治療がうまくいったことを示しています。
しかしもう一人の子供の場合、歯や涙腺、唾液腺についてはほぼ正常に形成されたのに、汗腺だけは完全に回復できなかったようです。おそらく、汗腺の発生のスケジュールが個人個人異なっているためと考えられます。今後投与の回数やEDA-Fcの量を増やしたほうがいいかもしれません。ただだからと言って、注射回数を増やすと流産の危険性が高まりますから、投与法も含めさらに多くの子供さんで検討する必要があると思います。
感想
発生学的にも臨床医学的にも、素晴らしい成果だと思っています。胎児期や発達期のみに必要な分子は、母親への影響をほとんど気にする事なく治療が可能なこと、そして発生期を乗り越えられれば、遺伝子が欠損していても一生生活に支障がないのではと期待できます(この研究では2歳までしか追跡できていませんが)。また、細胞外に分泌できる分子なら、EDA以外でも同じ方法を用いることができるのではないでしょうか。
胎児期や発達期の脳の発達になんとか介入して正常化させるのが自閉症治療の一つのゴールだと思っています。その意味で、今回の研究は様々なヒントを与えてくれます。私は現役を退き、今や考えるだけですが、それでも実現可能なアイデアが出てくるよう、今後も励んでいきたいと思っています。
2019年8月15日
母体の炎症の胎児脳への影響
風邪やインフルエンザなど様々な原因で妊婦さんに炎症が起こってしまうと、胎児の脳の発達に影響して自閉症などの発症率が上がることは、多くの妊婦さんとその子供を追跡する調査(疫学的調査)により確かめられています。そのため、できるだけ妊婦さんは炎症の原因を遠ざける必要があり、感染症はワクチンなどで予防するのが望ましいとされています。
ではなぜ炎症が脳の発達に影響するのでしょうか? これについては昨年9月注目すべき論文がNatureに発表され紹介しました(http://aasj.jp/news/watch/7378)。この研究によると、炎症で上昇するサイトカインの中でもIL-17が神経細胞に直接働き障害する犯人で、これを抑制できると炎症が起こっても脳への影響は最小限に止めることができる可能性が示されました。血液中のIL-17濃度は測定することができますから、是非因果関係を調べる疫学調査が行われて欲しいと思っています。
IL-17は炎症を誘導する「炎症性サイトカイン」の一つで、IL-6やTNFと呼ばれる分子も同じ仲間です。
動物実験と疫学調査をつなぐ
もちろん、妊娠時期に炎症を起こして胎児への影響を見るような実験は、動物モデルで行うしかありません。しかし、動物モデルでの神経症状が人間の症状を反映していると決めつけるのは、少し乱暴な気がします。このため、動物実験と、疫学による調査のギャップを埋める研究が待たれますが、今日紹介したいオレゴン健康・科学大学のグループがNatureに発表した論文は、まさにこの問題に挑戦した研究で、重要な研究ではないかと思っています(Rudolph et al, Maternal IL-6 during pregnancy can be estimated from
newborn brain connectivity and predicts future working memory in offspring(妊娠中の母体のIL-6濃度は新生児の脳の結合と将来の作業記憶に相関する), Nature
Neuroscience in press, 2018: https://doi.org/10.1038/s41593-018-0128-y)。一般の方には少し理解しづらいと思いますが、紹介することにしました。
研究の概要
この研究の目的は、母体の炎症が脳の発達過程のどこに作用するかを決めることです。この目的で、母体の炎症の強さをIL-6の血中濃度で代表させて調べています。先に紹介したIL-17とは違うのですが、ほとんどの炎症でIL-6が上昇することはよく知られています。これは急性、慢性を問いません。例えば2型糖尿病などメタボと呼ばれる慢性病の背景に炎症があると考えられていますが、この時もIL-6が上昇してきます。
次に、IL-6の濃度を測ったお母さんから生まれた新生児のMRI検査を睡眠時に行います。このような安静時のMRI検査では、脳の機能はわかりませんが、様々な解剖学的構造を知ることができます。この研究では冒頭の図に示すような、脳内各領域の間の神経結合性に注目して調べています。
IL-6濃度は一つの数値で表せる単純な指標ですが、MRI検査は大量の情報を含んでいます。そこで、脳全体をデータとして利用するのではなく、自閉症などで変化が起こると予想できる領域に絞ってデータを集めています。実際には10領域を選び、それぞれの領域内の結合性10指標、領域間の結合性45指標を算出し、これらの数値とIL-6濃度の相関を調べています。これを80人もの新生児で行うのですから、実際は大変な研究だと推察します。当然今流行りのコンピュータを使ったAIが大活躍します。目標は、脳の結合性のデータをコンピュータにインプットすれば、母体のIL-6濃度が予想できれば、これは100点のモデルができたことになります。
炎症で特に障害される領域
100点のモデルというわけにはいきませんが、妊娠時のIL-6濃度と相関する領域が見つかってきました。どの場所かを詳しく述べてもイメージがわかないでしょうから、場所についての説明は省きますが、
1) ある対象にフォーカスを当てるときに働く領域と脳活動の安定性維持に関わる回路の間の結合性、
2)空間的な注意に関わる幾つかの領域間の結合性、
3)視覚を介した注意に関わる幾つかの領域間の結合性
がIL-6が高かったお母さんから生まれた新生児では、特に低下することがわかってきました。
IL-6と作業記憶
MRI検査と脳の機能検査が集められているデータベースを用いてそれぞれの回路と脳の機能との相関を調べると、今回の研究で明らかになったネットワークの多くが、刻々と入ってくる情報を一時的に維持して、統合するために働いている、「作業記憶:ワーキングメモリー」に深く関わっていることが見えてきました。
そこで、MRI検査を行った新生児の中から選んだ46人が2歳になるのを待って、作業記憶の検査を行い、特に妊娠第3期のIL-6濃度と作業記憶が逆相関することを明らかにしています。
結論と私的感想
人間にIL-17やIL-6を注射して実験するなど決して許されません。しかし、今回の研究が示すように、一つの指標でも多くの人間を調べれば、様々な状態が存在していることがわかります。特定の指標について一人一人の多様性を正確に把握し、この指標と脳の構造を比べる研究は、今後も動物実験と、疫学をつなぐ重要な方法として使われていくと思います。
今日紹介した研究は特に自閉症に焦点を当てているわけではありませんが、作業記憶という脳の高次機能の根幹に関わる機能と炎症の関係が、神経レベルである程度明らかになったのではないかと思います。今後同じ方法をIL-6だけでなく、ほかの炎症パラメーターについて調べ、また自閉症スペクトラムの脳を念頭に相関を調べて欲しいと思います。そして何よりも、2歳までの発達期に、どこまで脳の結合性を変化させられるのかについても知りたいと思います。まだまだですが、着実に研究が進んでいると実感しています。
2019年8月15日
ゲノム科学
ゲノムを考える
2015年5月15日
序:ゲノムは情報
今はその気になれば全ての生物のゲノム解読が可能で、順を追って全ての種のゲノムを明らかにする国際プロジェクトが進んでいる。また個人レベルの進化研究も、ゲノムプロジェクトのおかげで大きく進展した。事実これまで30話にわたって紹介した論文のほとんどは、ゲノム解読を最も重要な研究手段として使っている。例えば昨年8月に第13話 で紹介した何十羽のカラスのゲノムを比べる研究が行われる日が来るなど、私が大学を卒業した時には想像できなかった。誰もが同じ理解を共有していると思い込み、日常深い考えもなく頻繁に使っている「ゲノム」という言葉も、改めてその意味はなにか?と問われると答えるのは簡単ではない。そこで、30話を終えたところで少し立ち止まって、ゲノムとは何かについて何回かに分けて整理することにした。
いうまでもなくゲノムとは個々の細胞の中にあるDNA全体が代表している何かだ。DNA自体は物質の総称で、4種類の異なる塩基を持つヌクレチドがつながった巨大分子と定義することができる。しかし、ゲノムが持つ意味はこの物質性とは全く別のところにある。例えばゲノムは、我々が遺伝子と呼ぶものに対応する部分を持つが、遺伝子という言葉は、それがコードしている特定のペプチドや機能的RNAと対応して初めて意味を持つ。ヘモグロビンの遺伝子、ケラチンの遺伝子という具合だ。しかし、遺伝子=DNAではない。普通ヘモグロビンのDNAとは言わない(そう呼ぶ場合はDNAを遺伝子と同義に使っている)。これはDNAが物質で、遺伝子が機能をさす言葉だからだ。逆に言うと、遺伝子という概念には核酸という物質性は含まれる必要はないが(PC上に遺伝子を保存できる)、それが参照する分子の概念は必ず含まれる。ここでとりあえず遺伝子という言葉を、「DNAを媒体とする、特定の分子を参照する情報」と定義しておこう。
では情報としてのゲノムの性質を次に考えてみよう。遺伝子が情報として働くことを可能にしているのが、DNAの持つ情報媒体としての性質、即ち異なる塩基を持つ4種類のヌクレオチドが様々な配列で並ぶポリマーを作り、この並び方のパターンで無限のモノやコトを参照できるという性質だ。この情報は一定の法則にしたがって、実際の機能分子へと変換され生命を支える。また、AはT、CはGと相補的に対応することで自らの複製、伝達、転写が可能になる。見れば見るほど完璧な情報媒体だ。しかし、このDNAが持つ情報媒体としての完璧性が、ゲノムの理解を難しくしている。ゲノムの概念に何が含まれているか見てみよう。まずタンパクや機能的RNAへと転換される遺伝子が存在する。加えて、遺伝子発現制御やスプライシング制御など ‘コト’についての情報も同じようにA,T,C,Gの配列で表現されている。ただ問題は、核酸の並びにモノや機能を対応させられない配列、その機能や意味が全くわからない配列が、対応が付いている配列の何倍も存在している。この理解できない配列を情報と考えていいのか?存在しないのと同じと無視していいのか?これが決められない以上はゲノムも理解できない。繰り返すが情報媒体としてDNAは完璧だ。そのためDNAには必ず情報が存在すると思ってしまう。このことは文字と比べてみるとよくわかる。最初から文字は言語という情報の媒体として生まれてきた。従って、文字があるとそこに必ず情報があると私たちは確信する。だからこそ、初めて見たシュメール人の楔形文字も解読できると確信した。しかし例えばアルファベットをランダムに並べることは簡単で、いくら文字の並びが目の前にあったとしても情報を担っているかどうかはわからない。DNAも文字と同じで、その機能は情報をコードする媒体だ。このため、DNAには情報が必ず担われていると思ってしまう。しかし意味のない単語からわかるように情報媒体を使っても情報でない例はいくらもある。では文字と同じように、意味が理解できない配列は情報ではいと無視すればいいだろうか?実はそう簡単ではない。今回は短く触れるだけにするが、ゲノムには言語と異なるさらに厄介な問題がある。即ち情報の出し手がいないという問題だ。言語の場合、情報には必ず出し手と受け手が存在する。一方、ゲノム上の情報には出し手はいない。シャノンの情報理論を見ると、出し手がいるということで100%正確な情報がまず存在することが前提になっている。即ち何が情報で、何が情報でないかは最初から決まっている。一方、ゲノム上の核酸配列は、何が情報で、何が情報でないか最初からは決まっていなかった。というより、そもそもゲノムには情報としての出し手がいない。誤解を恐れずいうとDNAという情報媒体は自ら新しい情報を生み出せるという性質を持つ。このため、今私たちが情報でないと判断した部分も、将来情報化できるポテンシャルを持っている。さらに一つのゲノムが新しい情報を生みだすのに一部の部分だけが関わるわけではなく、ゲノム全体が様々な形で新しい情報の誕生に影響を及ぼしている可能性がある。即ち、部分と全体が常に一体化していて、分けることができないという生物の特徴的関係が、ゲノムレベルにも存在するようだ。従って、ゲノムは部分として様々な情報をコードするだけでなく、全体として新しい情報の誕生や消滅に関わっている可能性が高い。このようなゲノムの性質は、出し手のはっきりしたシャノン情報理論でゲノムを捉えることが難しいことを意味している。このように、情報としてゲノムが持つ数々の問題がある。これから「ゲノムを考える」で、この問題をもう少し深く掘り下げながら、ゲノム理解を妨げている問題を整理したいと思っている。
「ゲノムを考える」導入部、第一回の結論は「ゲノムは情報」だ。このことを示した面白い論文を一つ紹介して31話を終わる。山梨大学教授の若山さんがCDB(理化学研究所 発生・再生科学総合研究センター)在籍時に行った仕事だ。昨年は小保方問題の渦中の人になってしまった若山さんのライフワークは絶滅種、あるいは絶滅危惧種をクローン技術で復活させることだ。この模擬実験として、若山さんは16年フリーザーの中に捨てられていたマウスの死体の細胞から核を取り出し、核を抜き取った未受精卵に移植した。無論16年経っていると言ってもひょっとして生きた細胞が残っているかもしれない。核移植に使った細胞が全部死んでいることを確かめるため、フローサイトメーターで100万以上の細胞を調べても生きた細胞を見つけることができなかった。このように完全に死んでいることを確認した細胞から核を取り出し、卵に移植すると高い確率で胚発生が始まり、その胚から多能性幹細胞株(ES細胞)を樹立することができた。さらに、このES細胞株をマウス胚盤胞に移植して発生させると生殖細胞に分化し、ついに死んだ細胞の核から生きたマウスを作成することに成功した。若山さん自身は論文の中でこの結果をもっぱら技術的進歩として議論しているが、私にとってはゲノムが情報であることの最も明確な証明に見える。すなわちゲノムの完全性は細胞の生き死にに関わらず維持されている。情報の完全性に、生命というシステムは必要ない。情報を実験的に扱うときは、物質として扱えばいい。この実験系なら、削ったり、足したり、再編成したゲノムからクローンを作ることで、ゲノム情報の全体と部分の関係を問い直す実験ができるかもしれない。
[
西川 伸一 ]
ゲノムの解剖学
2015年6月2日
31話 でゲノムは情報だと結論した。では私たちのゲノムがどんな要素からできているのか、まず解剖学から始めよう。実際にはミトコンドリアにもゲノムはあるのだが、話を簡単にするために核内のゲノムに限る。一部の細胞(例えば赤血球)を除いて、私たちの細胞の全てに核があるが、ゲノムはこの核内にあるDNA総体が表現している情報だ。核内には46本に分かれたDNAが存在し、ヒストンをはじめとする多くのタンパク質と結合して、コンパクトに折りたたまれ、染色体を形成している(図1)。この染色体一本一本の基本的構造は同じなので、ここからはゲノムが一本の染色体からできているかのように話を進める。
ヒトのゲノム全体は、約30億個のヌクレオチドが連なった高分子で、ヌクレオチドの持つ4種類の塩基の組み合わせが媒体となって全ての情報が書かれている。ゲノム内の情報がコードする最も重要なものが、細胞という化学反応系を形成・維持するための基本分子であるたんぱく質で、これに対応するゲノム部分をcoding DNAと呼んでいる。何をcodingと呼ぶかは定義の問題なので、ここではタンパク質まで翻訳される遺伝子をcodingDNAと呼ぶ。ただこのcoding DNAに対応する遺伝子はヒトで22000程度しかなく、全ゲノムに占める割合は1.5%もない。少数の例外を除いて、個々のたんぱく質をコードする遺伝子はエクソンと呼ばれる小さな部分に別れて存在している。一度RNAに転写されてから、たんぱく質の情報に関わらない部分を除去した一本のmRNAへとつなぎ合わせた後翻訳される。このエクソンとエクソンの間にある配列をイントロンと呼ぶ。遺伝子が情報としての機能を発揮するためには、他にも遺伝子を正しい場所からRNAに転写するための様々な指令情報が必要だ。このほとんどは、エクソンの外、すなわちイントロンや遺伝子から様々な距離で離れたnon-coding領域に存在している。これからわかるのは(図2)、たんぱく質という「モノ」に対する情報(エクソン)と、モノの情報を書き出すための様々な標識、すなわち「コト」に対する情報から一つのcoding単位ができていることだ。
図2 coding遺伝子単位の概略。調節領域の指令で遺伝子が転写されると、RNA
maturation に関わる標識により、イントロンが除去された一本のmRNAが形成される。
「モノ」「コト」両方の情報を含めると、coding単位がゲノムに占める割合はずっと大きくなるが、逆にその正確なサイズは測定しにくくなる。なぜなら、「コト」に必要な情報が、ゲノムのどこからどこまで必要かを正確に算定できないからだ(これは次回に議論する)。さらに、同じ遺伝子領域に逆向きに異なる遺伝子が並んでいることもある。したがって、正確にcoding遺伝子セットが占めるゲノム上の割合を算定することは難しい。
次にcodingとは言えないが、構造的には遺伝子と呼べる単位が存在している。ただ、正常な遺伝子とは異なり、そのまま翻訳されタンパク質ができることはない。そのため、偽遺伝子と呼ばれている。ヒトでは偽遺伝子と考えられる部分がなんと1万以上も存在している。進化の過程では、coding遺伝子が重複を繰り返して多様性を拡大するのをよく見ることができる。このように重複した遺伝子に変異が導入されて機能がなくなると偽遺伝子と呼ばれるようになる。偽遺伝子が最も多いのは嗅覚受容体で、ヒトでは400の機能的遺伝子に対してなんと600もの偽遺伝子が存在している。ただ、偽遺伝子だからなんの役割もないと決め付けることはできない。成り立ちから考えても、偽遺伝子といえども、構造的には遺伝子と同じだ。しかも、機能していないことから、変異が蓄積されやすく、新しい機能を持った遺伝子を作るという目的にはうってつけの材料だ(例えば第21話 参照)。この意味で、遠い将来、新しい機能を持つ分子の資源としての役割を担っているということができる(図3)。また、ニワトリの免疫グロブリン遺伝子で見られるように、機能的抗体遺伝子と遺伝子転換により部分の交換を行うことで抗体の多様性を生みだすための鋳型として働いている場合もある。このように、ゲノム各領域を、それが必要とされる時間スケールを変えて見ることは、ゲノム理解について重要で、これについても次回以降議論する予定だ。
DNAにコード可能な生体機能分子はタンパクだけではない。これまで多くの機能を持つRNA分子が知られている。リボゾームRNAやトランスファーRNAなどのタンパク翻訳に関わるRNAはその代表的なものだが、他にもスプライシングやRNA編集などのRNA成熟、DNA合成、遺伝子制御、トランスポゾン制御など、多岐にわたる機能を持つRNAが知られている。機能の詳細は省いて図にまとめておくが、機能的RNAはゲノムの4%ぐらいを占めていると考えられている。これらを一つ一つ紹介するつもりはないが、この中のnoncodingRNAは、DNAが持つもう一つの顔を示していると考えており、これも次回以降議論する。
ここまで主に転写される部分について見てきたが、ゲノムには多くの転写されない場所が存在する。例えば、染色体のヘテロクロマチンと呼ばれる場所に存在する繰り返し配列の集合は、全ゲノムのおおよそ6%を占めている。分裂時に染色体を引っ張る微小管の結合部位である動原体が結合するために使われているセントロメアや、分裂時に染色体が削られて重要な遺伝子が消失するのを防いでいるテロメアなどは、転写はされなくてもゲノムの複製や維持に必須の領域であることがわかっている。しかし、ヘテロクロマチンを形成する他の多くの繰り返し配列は、機能がよくわかっていない。実際、ヘテロクロマチンとそれに対応する繰り返し配列は、種を越えてひろく存在しているが、その配列自身は保存されていない。他にも、超可変ミニサテライト(hypervariable minisatellites)と呼ばれる、ユークロマチンに存在する繰り返し配列も存在する。
ヒトゲノムの解読結果を見た時の一番大きな驚きは、トランスポゾンに由来する配列が全ゲノムの5割近くを占めていたという事実だ(図5)。トランスポゾンとは、基本的には細胞の中で染色体から染色体へ伝搬できる遺伝子単位を指し、図に示すようにLINE, SINE, LTR—トランスポゾン(レトロビールス型)、そしてDNAトランスポゾンに分類されている。
これらはレトロトランスポゾンと、DNAトランスポゾンに大別され、レトロトランスポゾンはレトロウイルスと同じように、ゲノムからはRNAとして読み出され、そのRNAが逆転写酵素でDNAに転写されたあとゲノムに挿入されることで伝搬する。完全型のレトロトランスポゾンは、従って逆転写酵素をコードしている。逆転写酵素を持たない不完全型レトロトランスポゾンの場合は、完全型のトランスポゾンが発現する逆転写酵素を利用することで伝播が可能だが、基本的には伝搬能力を失っていると見たほうがいいだろう。RNAとしてゲノムからそのまま転写されるレトロトランスポゾンと異なり、DNA型トランスポゾンは自らを正確にゲノムから切り出し、また他の箇所に挿入するためのトランスポゼースと呼ばれる酵素をコードしている。多くの種では、完全なトランスポゼースを持ったトランスポゾンがゲノム中に存在しているが、ヒトゲノム中に存在しているほぼすべてのトランスポゾンは、トランスポゼースの活性を失っている。従ってトランスポゾンの活性を失った化石といえる。
今回は話を進めるための基礎知識として、ゲノムの構造要素の概略を述べた。こうしてヒトゲノムを解剖していくと、こじつけもあるが、おおよそ6割の配列になんらかの意味を対応させることができる。ただ意味や機能が想像だにできない部分が4割近く存在する。また私たちのゲノムのほぼ9割をトランスポゾンか、意味のわからない配列が占め、これらの塩基配列に何か積極的な意味があるようには思えない。このため、ジャンクDNAと呼ばれたりしている。ただ、意味が無いのか、理解できないだけなのか、9割を占めるジャンクについて考えることが必要だ。もちろん種によって、この構造は多様で、ジャンク配列のゲノムに対する割合も大きく違う。次回からは、ゲノムを構造化することで新しい情報が生まれるようすを見ながら、さらにゲノムの理解を進めてみたい。
[
西川 伸一 ]
構造としてのゲノム
2015年6月15日
ここまで、ゲノムが細胞の生き死にに左右されない(言って見ればPCが止まっていてもメモリーは残るようなもの)情報であることを見てきた。しかし、ゲノムに組み込まれた情報が全てATCG塩基配列で表現されていると考えると、大きな間違いを犯すように思う。すでに見たように、翻訳されるたんぱく質をコードする情報自身は塩基配列で表現されているが、ゲノム上に全くランダムに存在するのではなく、適当な長さのエクソンに分かれ、それを転写するための様々な指令情報が組み合わさった単位として存在している。すなわち、一定の構造をとっている。「何を今更?」と言わずに続いて聞いてほしい。この転写を調節する時に使われる様々な「コト」についての指令標識は塩基配列として表現されるが、それ以外にも情報化されていることがある。例えばイントロンの長さ、エンハンサーの位置などは、ゲノム上の構造として表現されるものだ。もしイントロンの長さが遺伝子の転写に重要な役割があるとすると、全く意味がわからない塩基配列も情報として意味を持つ可能性がある。我々のゲノムのかなりの部分が、情報として具体的な何かに全く対応していないジャンクと呼ばれるDNA配列だと述べたが、これも塩基配列で表現できる情報としてみると意味がわからないからジャンクと呼んでいるだけで、構造としてゲノムを見た時重要な役割を持つのかもしれない?そこで、まずゲノムが構造化されることで生まれる塩基配列とは違った情報の可能性について見ていこう。
1、遺伝子の秩序立った配置:Hox遺伝子の衝撃
ゲノムが構造化されることで、DNAが新しい情報媒体になることを我々が最も実感したのは、頭から尻尾まで、体の各体節のプランを決めているHox遺伝子のゲノム上の構造が明らかにされた時ではないだろうか(この遺伝子の変異で触覚が足に変わったショウジョウバエについては既に第6話で述べた)。急速に進む様々な種のゲノム解析から、ほぼ全ての動物種で、何個ものHox遺伝子が小さな領域にクラスターを作って集まっていることがわかってきた。図1に示すように、現在ではこのクラスター内のHox遺伝子を5’から順にHox1,Hox2….Hox13と名付けている。
図1ショウジョウバエと哺乳動物のHox遺伝子構成と、その発現。体軸に沿った発現のパターンが、遺伝子の構成と対応している。この対応関係はcollinealityと呼ばれている。
脊椎動物より未熟な動物ではこのクラスターは一つしかないが、脊椎動物では重複により別々の染色体に4つのHox遺伝子クラスターが存在する。驚くべきことに、体の体制が完成した胎児期にHox遺伝子の発現を調べると、ショウジョウバエも、マウスでも図1に示すようにゲノムに並んだ順番、すなわちHox1からHox13まで順番にそって、頭部から尾部へHox遺伝子が発現している。このゲノム上の遺伝子の配置と、頭部から尾部への発現場所の対応性はcollinealityと呼ばれ、左右相称動物では広く保存されており、このHox遺伝子の決まった配置を維持することの重要性を示している。
次に、図2に従ってHox遺伝子クラスターの進化過程を見てみよう。第一段階では遺伝子重複によりまず4種類のHox遺伝子が並んだクラスターが形成される。こうして生まれたゲノム上のHox遺伝子クラスターは、次の左右相称動物の進化過程で原型が完成し、各Hox遺伝子の塩基配列だけでなく、配置そのものが情報として体の前後の体制の形態形成に利用されるようになる。その後それぞれの動物の体制に合わせてHox遺伝子の数は増減し、また配置も変化しているが、基本的には各遺伝子の配置は前後軸に合わせて構造化されたまま維持される。この事実を見ると、遺伝子の配置という構造が塩基配列とは異なる情報をゲノムの中に持ち込んでいるのがわかる。構造やデザインが機能を持ち、情報になることは生物の世界では当たり前だ。当然ゲノムも形質と同じように、特定のデザインの下に構造化されることで新しい情報を持っても不思議はない。例えばHox遺伝子の塩基配列はそのままで、順序が狂うことで新しい体の体制が生まれたとしよう(例えば尾が長くなる)。もしこの結果生まれた形質が自然選択されたとすると、この時選ばれた変異は塩基配列の変異ではなく、遺伝子の配置、すなわち構造の変異が情報として選択されたことになる。あるいはまたHox遺伝子間の距離が一定に保たれることが重要だとすると、その距離を埋めているのは特定の配列というより、ATCGを積み重ねて一定の長さを実現できるDNA
の物理的性質によっていると言える。すなわち、塩基配列が問題ではなく、構造が問題になっている。重要なことは、構造化により生まれる情報も、子孫に伝える時は塩基配列情報として複製される点だ。複製だけを見ていると塩基配列だけが情報だと勘違いするが、このように伝達時には塩基配列情報として、機能発揮時には構造情報として働くゲノム部分があることを無視してゲノムは考えられない。
2、ヌクレオソーム
染色体を見ると、塩基配列とは無関係にDNAを基材とする構造が形成されている。これもDNAが持つ構造化能力の例だ。具体的に見てみよう。図3に示すようにDNAは4種類のヒストンが集まった8量体に巻きつくヌクレオソームという構造を取っているが、ヒストンとDNAの結合には原則として特異的な遺伝子配列は必要ない。
図3 ヌクレオソーム単位の構造。一つのヌクレオソームには200bpのDNAが巻きついている。
<引用>http://commons.wikimedia.org/wiki/File:Nucleosome_structure_and_subunits.svg http://commons.wikimedia.org/wiki/File:Pioneer_Factor_rearrange_the_nucleosome.jpg
これまでヌクレオソーム構造は、長いDNAを核内にコンパクトにたたむために進化してきたと考えられてきた。しかし、遺伝子の大きさが4Mbしかない古細菌類の一部がヌクレオソームをもつことが発見され、今では転写を効率化するために進化してきたと考えるようになっている。実際、古細菌、真核生物の両方で、転写開始点のほぼ全てがヒストンに巻きついていないリンカーDNA部位に存在している。すなわち、ヌクレオソームは高々200bpの長さのDNAからなる小さな単位で、構造も単純なため複雑な情報を持つことはないが、ゲノム内の最小構造単位として、転写開始場所を構造的に指示するために進化してきたようだ。
ヌクレオソームの出現は、その後の生物情報の可能性を一変させ、最終的に人間の言語獲得にまで至る道を決定付けたと思っているが、このことはまたいつか議論しよう。ともかくヌクレオソーム構造獲得のおかげで、このコアヒストン構造をさらに修飾してゲノムの使い方を決めるエピジェネティック機構が進化し、ゲノムにさらに複雑な構造化を導入することを可能にした。実際先にあげたHox遺伝子の配置はこの新しい機構を巧みに取り込んでいる。体の節、すなわち体節を形成する中胚葉では最初HoxA遺伝子クラスターは全てH3ヒストンの27番目のリジンがメチル基で修飾されており、これによりHoxクラスター全体の遺伝子の発現が抑えられている。即ち、ヒストンの修飾により転写に必要な分子が近づけない領域を構造的に保証している。この抑制型ヒストンは発生が進み前方から体節が発生する時には、前側のHox遺伝子領域から外れ、体の体制に合わせてHoxクラスターが発現できるための重要なメカニズムになっている。最終的に、体幹部では後ろ側のHox遺伝子が存在する領域は抑制型ヒストンが維持されるため、後ろ側のHox遺伝子は発現できない。一方、体の後方ではほとんどの領域から抑制型ヒストンが外される。このようにHoxクラスターの配置が体の位置と対応しているおかげで、Hoxクラスターの発現調節を大まかに区域化することが可能になり、体の複雑なプランを指示することが可能になっている。ただ、H3K27のメチル化を介するゲノムの区域化は特殊な例で、普通はH3の4番目のリジンがメチル化したH3K4me3と、9番目のリジンがメチル化したH3K9me3が引き金となって、染色体構造をそれぞれユークロマチンと呼ばれる開いた状態と、ヘテロクロマチンと呼ばれる閉じた状態に構造化することが、最も普通に見られる転写活性の区域化のやり方だ。この構造化はDNA自体のメチル化も含め様々な分子が関わる複雑な過程で、マトリックスとしての ゲノムを考える時に議論したい。また、生命誌ジャーナルでもクロマチンについて国立遺伝研究所の広瀬さん 、前島さん に解説をいただいているので、是非参照いただきたい
引用<Sha, K. and Boyer, L. A. The chromatin signature of
pluripotent cells (May 31, 2009), StemBook, ed. The Stem Cell Research
Community, StemBook, doi/10.3824/stembook.1.45.1. http://www.stembook.org/node/585 >
今回は、ヌクレオソームを基盤として、ゲノムを構造化する重要な機構がエピジェネティックス機構だという結論で止めておく。ただ、ヌクレオソームやエピジェネティック機構の進化は実際にはHoxクラスターの進化より先に起こっている。したがって、エピジェネティック機構というゲノム構造化を可能にする機構をさらにうまく利用する方法の一つとして、Hoxクラスターのような新たな構造化が加わってきたと考えるのが正しい。次回は、ヌクレオソームより大きなゲノムの構造単位、topology associating domaiから話を続ける。
[
西川 伸一 ]
ゲノムの構造単位
2015年7月1日
1、topology associating domain (TAD)
最近、遺伝子の組織や発生時期特異的な発現調節の基本構造単位としてtopology associating domain(TAD)と呼ばれる領域に注目が集まっている。ヒトゲノムには約2000のTADが存在すると考えられているが、TADの存在が広く認められるようになったのはつい最近のことだ。TAD概念の確立には、核内で位相的に接して存在しているゲノム領域を特定するchromosome conformation captureと呼ばれる方法の開発が大きく寄与している。一つのTADは平均500kb—1Mb程度の大きさで、その中に1個から複数の細胞特異的、あるいは発生時期特異的に働くcoding遺伝子と、その発現調節(エンハンサー)領域を含む長いDNA単位が大きな塊を作って核内に存在していると考えられる。図1はPopeらの論文(Nature, 515:402,
2014)から拝借したTADのイメージ図だが、それぞれのTAD単位を構成するDNAが、分離した毛糸玉のようにまとまって核内に存在していることが表現されている。なぜこのような構造化が必要なのか?これについては、遺伝子発現の時期や場所を決めている調節ユニットを一つの塊として構造化する必要に答えたのがTADではないかと考えられている。
実際、HiCと呼ばれるChromosome conformation capture法を用いて、どの領域がどの領域と隣接していかを調べると、遺伝子やエンハンサーの相互作用がTAD内に制限されていることがわかる。図1のヒートマップはHiCの結果をマッピングしたもので、各領域がコンタクトしている確率が高いほど赤くなるよう示されている。核という狭い3次元空間では、原理的に各領域はどの領域とも近接することは可能だが、実際にはTAD内にある領域は同じTAD内の領域と相互作用する確率が高い。TAD内部の塩基配列は特に保存されているわけではないが、各TADの間には、種間でよく保存された、CTCF分子の結合配列、house keeping遺伝子、tRNA遺伝子、そしてSINEトランスポゾンなどが集まった境界領域が存在している。最近の研究から、この境界が、一つのTAD内のエンハンサーの効果が、隣接したTADに影響を及ぼさないよう制限するインシュレーターの働きをしているのではと考えられるようになってきた。私たちの体は何百種類もの細胞から出来ており、それぞれの細胞ごとに働いている遺伝子は違っている。とはいえ、それぞれの細胞分化に必要な遺伝子群を、分化ステージや細胞系列に合わせて狭い領域にまとめることは難しい。このため全く異なる細胞で発現する遺伝子が隣接して存在することはゲノムでは普通に見られる。従って、一つのTADの発現が、隣のTADにある遺伝子の発現に影響を及ぼさないよう構造化されていることは重要だ。次に、これをより具体的に示した2編の論文を紹介しよう。
論文1:TADによるHox遺伝子制御(Andrey et al, Science 340, 1234167, 2013)
TADによるゲノム構造化の重要性が強く認識されたのもまたHox遺伝子の研究からだった。HoxDクラスターは腕と指両方の発生に関わっているが、例えばHoxD10のマウス発生時の発現を経時的に調べると、図2に示すように、四肢発生の初期段階で前腕の形態形成に関わっていたHoxDクラスターが(図2:青色で示した部位)、時間とともに今度は指の形態形成に関わるようになるのがわかる(図2:茶色で示した部位)。同じHoxクラスターがほとんど同じ発生時期と場所で異なる構造の発生に順番に関わることを可能にするメカニズムを追求していたスイスのDubouleらは、HoxDクラスターが2つの隣接するTADの境界に存在することを見出した(図2)。
HoxDクラスター内の遺伝子が、前腕から手指へと発現が移動するのに呼応して発現を調節するエンハンサーも、TAD2のエンハンサーから、TAD1内のエンハンサーに移行する。
さらに、それぞれのTADに存在するエンハンサーの活性を調べると、テロメア側のTADには前腕での発現に関わるエンハンサーが、セントロメア側のTADには手指で発現するエンハンサーが集中していることをつきとめた。この結果からDubouleたちは、HoxDクラスターの全ては最初テロメア側のTADの支配を受け前腕形成に関わっているが、発生が進むと一部がセントロメア側のTADの影響を受けるようになり、徐々に支配されるTADをシフトさせることで、前腕と手指の発生に連続的に関わることを示した。すなわち、もともと構造化されているHoxクラスターに、TADという遺伝子調節単位構造が絡むことで、発生時のHoxD遺伝子発現の複雑なパターンが実現していることを示した。
論文2:TAD境界領域の機能(Lupianez et al, Cell 161, 1012, 2015)
Dubouleの研究からTADが構造化されたエンハンサーの供給単位になっていることがわかるが、TAD同士が影響し合わないよう機能的に分離されているかどうかはこの実験からはわからない。最近ドイツベルリンから、遺伝子領域の大きな欠失、反転、重複によりTADの境界が崩壊すると、TAD内のエンハンサー領域の影響が隣接するTADに拡大して、その結果発生異常が起こることを示す重要な論文が発表された。TAD間の境界の機能を教えてくれる研究なので、図3を用いて紹介しよう。
この研究では手指の発生異常に関わる変異が集中するヒト第2染色体の約2Mbの大きさの領域に注目して、まずそれぞれの奇形がどのような変異から起こっているのか調べている。図3に示すように、この領域には3つのTADが存在し、それぞれのTADには様々な組織の発生に関わる増殖因子や転写因子をコードする遺伝子が存在していることが分かった。これら遺伝子のうち、手指発生で発現が見られるのはTAD2に存在するEPHA4(ephrinに対する受容体)だけで、TAD1,TAD3にある遺伝子は手指には発現しない。このことから、手指発生時に遺伝子発現を誘導するエンハンサーの効果がTAD2内の遺伝子のみに限局されていることがわかる。次に、手指発生異常をおこす遺伝子変異を解析すると、境界2として示した領域が大きく欠損する変異では指が短くなる短指症が、境界1を含む領域の逆位が起こると、親指と人差し指の融合(F-syndrome)が、同じく境界1を含む部分の欠損では多指症が発症することが分かった。同じ変異を今度はマウスゲノムに導入して、人間とほぼ同一の手指発症異常をマウスで再現できることを確かめ、それ以降の実験はマウスで行っている。マウス手指発生過程でTAD1,TAD3に存在する3種類の遺伝子の発現を調べると、境界2がなくなるとTAD2エンハンサー活性がPax3遺伝子に及び、手指発生でこの遺伝子が間違って発現してしまう。同じように、境界1が変異を起こすと、手指発生時にIHHやWnt6の間違った発現が見られることが分かった(図3)。この結果は、核という極めて狭い領域に閉じ込められ3次元的に絡み合ったDNA上の遺伝子が一定の時と場所で正確に発現するために、TAD間の境界が重要な機能を持っていることを示している。しかし、この境界がなぜTAD外のエンハンサーの影響を食い止められるかについてはよくわかっていない。おそらく、さらに大きなレベルの、ゲノム構造化と関わるのではと考えられるが、これについては次回に紹介しよう。TADを説明するため、今回は手指発生に関わる遺伝子の発現についての研究した2つの論文を紹介した。最後に少し余談になるが、手指の発生異常についての詳しい研究を最初に行ったフランス人Maupertuis(図4)を紹介して今稿を終わりたい。
Maupertuisは、地球が縦にひしゃげた偏円であることを証明するためフランス科学アカデミーがペルーとラップランドの2カ所で観測を行った際のラップランド隊を率いた業績で有名になった物理学者・数学者だが、ビュフォンとともにフランス自然史を支える中心人物でもあった。彼はデカルトの機械論とそれを支持する前生説に反対し、後生説的有機体論展開の必要性を唱えた。1744年プロシア皇帝フリードリッヒ2世に強く請われてMaupertuisはプロシア王立科学アカデミーの会長に就任する。例えてみれば、日本学術会議の議長に中国や韓国から人を招くのと同じことで、待ち構えていたベルリン科学会の大きな抵抗にあうが、王室の後ろ盾と数学者オイラーの助けを借りて様々な改革を断行した。動物発生についてのMaupertuisの考えは、ライプニッツのモナド(単子)の概念に近い粒子が後生的に構造化されるというものだった。当時最も有力な説だったデカルトの機械論に基づく前生説を論破する根拠を探していた時、ベルリンで4世代にわたって多指症が維持されているRuhe家を知る。同じ形態異常が一族の母親からも、父親からも子孫に伝えることができることは前生説を否定する現象だとして詳しい研究を残している。ゲノム構造化単位TAD の意義を明らかにする記念すべき論文が、手指発生異常研究で最も長い歴史を持つベルリンからの論文であることを知り、Maupertuisを思い出し、深い感慨にかられた。
[
西川 伸一 ]
核によるゲノムの構造化
2015年7月15日
A対T、 C対Gの結合をベースにした2重らせん状の分子構造と、4塩基の並びで表現できる情報の無限性を考えると、DNAほど情報媒体として優れた物質はちょっと思いつかない。この線状に並んだ塩基対が持つ情報としての可能性に圧倒され、塩基配列を線状のコードとしてだけ見てしまうと、ゲノムが2次元、3次元と構造化されていることを忘れがちになる。しかし、遺伝子の配置、ヌクレオソーム形成、クロマチン構造、そしてtopology associating domains(TAD)と見てくると、ゲノムが1次元の配列情報だけでなく、構造化することで新たな情報を担えることを理解してもらえたのではないだろうか。ただ、構造化はこれだけにとどまらない。ミトコンドリアDNAを除くと我々のゲノムの全ては核の中に折りたたまれて存在している。今回はゲノムが収納されている核の構造とゲノムの関係について見てみたい。
クリエーティブコモンズに登録されている画像をchromosomal paintingで検索すると、Robert MayerらがBMC Cell Biology 6:44, 2005に発表した論文を見つけることができる。以前私の研究室に在籍していたTimm Schroeder君も著者に加わっているのを発見し、意外な出会いに喜んだが、この論文では染色体の核内の位置がランダムに決まっているわけではなく、細胞の種類に応じて特定の位置に収まっていることを示した論文だ(図1)。この写真に見るような染色体の核内での位置はクロモゾームテリトリーと呼ばれている。
図1ES細胞(上図)とマクロファージ(下図)の1番と14番(左図)、あるいは2番、9番(右図)染色体をin situ hybridizationにより染めだしている。(Mayer et al,
BMC Cell Biology 6:44, 2005)
図1は各染色体が、細胞の種類に応じて異なるクロモゾームテリトリーを形成していることを教えてくれる。すなわち、全体(核)が部分(染色体)の単純な集まりではなく、部分(染色体)が全体(核)によっても組織化される生命特有の特徴が、核と染色体の関係にも言えることを示している。もちろんクロモゾームテリトリーが染色体の位置を完全に決めているわけではない。細胞が分化して特定の遺伝子の発現が必要になると、その遺伝子が位置する領域はクロモゾームテリトリーから飛び出してくることも知られている。例えば、これまで幾度も登場したHoxD遺伝子の核内の位置をFISHと呼ばれる方法で調べた研究では、ES細胞分化に伴いクロモゾームテリトリー内に収まっていたHoxDがクロモゾームテリトリーから外れて存在することがわかっている(Morey et al, Development 134:909, 2007)。核全体から見たときの、このようなゲノム構造化を調節する仕組みはよくわかっていないが、他のゲノム領域と同様、次世代シークエンサーの開発により、核内に存在する構造とゲノムとの関係を直接調べることが可能になった結果、この分野は大きく進展しつつある。単純に見える核も複雑な構造を持ち、核酸以外にも多くの分子がこの構造を支えている。したがって、核によるゲノムの構造化についての研究は、ゲノムがコンタクトしている分子や構造の数だけ存在することになる。これではきりがないので、ここでは研究が進んでいるlamina associated domain(LAD)とnucleolus associated domain (NAD)について簡単に見ておこう。
・LAD(lamina associated domains)
図2 核膜直下の構築。青く染まるのは核酸、赤く染まるのは核膜孔。ここではLaminBを示しているが、核膜直下はLaminA,
LaminBが寄り合わさったラミナにより裏打ちされている。
電子顕微鏡を用いた核の解析から、核膜直下にはヘテロクロマチン構造が多いことは古くから知られており、このことから核膜直下に位置する遺伝子の発現は抑制されているのではないかと想像されていた。核膜はLaminA,Bを主成分とするラミナに裏打ちされている(図2)。ラミナとコンタクトしているDNAを標識するDNA adenine methyltransferase identifyication(DamID)と呼ばれる方法が開発され、これによってマップされる領域をlamina associated domain (LAD)と呼んでいる。DamIDは哺乳動物には存在しないアデニンメチル化酵素を利用して特定のタンパクと接する DNAをメチル化標識する方法だ。LADを検出するときはラミナの主成分であるLaminB1にアデニンメチル化酵素を融合させた遺伝子を細胞に導入、この細胞のラミナとコンタクトを持つDNAのアデニンをメチル化させる。哺乳動物のDNAにはメチル化アデニンが全く存在していないため、この細胞のゲノム中のアデニンがメチル化された領域を特定することで、LADを定義することができる(図3)。
これにより、ヒトやマウスでは0.1−10Mbの大きさのLADが1300程度存在し、全ゲノムの4割を占めることが分かった。LADはcoding遺伝子が少ない領域が濃縮されており、75%程度は細胞の種類を問わず保存されている。逆に言うと、残りの25%は細胞種に応じてLADだったり、なかったりしておりで、LADが発生によりダイナミックに変化する構造であることを意味している。LADに存在する領域に結合するヒストンの構造などと比較する研究から、LAD内の遺伝子は一般的に抑制されていると考えられている。最近の研究で、TADと領域が重なっている場合があること、あるいはCTCF (CCCTC-binding factor,抑制性の転写因子)がLADの境界に結合していることなどが明らかになり、両方の構造化はメカニズムを共有していることが想定されている。しかしLADの研究は始まったばかりで、TADやクロモゾームテリトリー、あるいは次に取り上げるNADとの関係や、ラミナとコンタクトをとるメカニズム、あるいは発生過程でダイナミックに組織化されるメカニズムなど、まだまだ研究が必要だ。とりあえずこれまで分かっていることを単純化して、図4にTAD,LADの関係が細胞分化で変化する様子を示しておく。
・Nucleolus associated domain (NAD)
核小体はリボゾームRNAが転写され、リボゾームが形成される核内の一種の構造物だ。この構造とコンタクトしているゲノム領域を網羅的に調べる研究も行われ、NADと呼ばれている(図5)。
NAD領域の特定は、核小体と共に精製されてくるDNAを採取し、次世代シークエンサーで調べることで行われる。従来、核小体にはRNAポリメラーゼのうち、Pol I, Pol IIIが選択的に存在していることが分かっていたが、NAD領域にも、Pol I, Pol IIIによって転写される遺伝子が濃縮していた。このことから、確かに核小体の構造と密接に関わっているDNAが濃縮されていることがわかる。ゲノム全体の40%近くを占めるLADと比べると、NAD領域ははるかに小さく、ゲノム全体の5%に満たない。もっともはっきりしたNADの特徴は、染色体分配や細胞分裂時に重要な細胞小器官である中心体近くの繰り返し配列(次回紹介する)が濃縮されていることだ。実際染色体上にNADをマップすると、中心体と接した領域にNADが存在するのがわかる。このように、NADもランダムに決められているのではなく、どの領域が核小体とコンタクトするのかも一定のルールで制御されていることが理解できる。ヒトHeLa細胞のNAD内には1300近くの遺伝子があるが、NAD内にある遺伝子の全般的傾向としては、LADと同じで、遺伝子密度の低い領域が濃縮されていると言っていい。またNADに結合しているヒストンの修飾を調べると、H3K4me3やH3K27me3などの抑制性のヒストンが濃縮されており、LADと同じようにこの領域の遺伝子発現は抑制的に支配されているといえる。NADに存在する遺伝子で最も特徴的なのは嗅覚遺伝子だが、ほとんどの細胞で発現が抑制されている嗅覚受容体遺伝子が濃縮されていることも、NADが遺伝子を抑制するための構造化の一つであることを示唆している。一方、ヘテロクロマチン構造により抑制されているトランスポゾンは、特に領域を限らず均一に分離している。NADも研究が始まったばかりで、今説明した現象の分子メカニズムはほとんど分かっておらず、今後の研究が必要だ。
3回にわたって、遺伝子の配置、ヌクレオソーム、TAD, LAD,NAD,そしてクロモゾームテリトリーと、ゲノムが様々なレベルで構造化されており、構造化されることで、おなじ塩基配列でも転写される情報とは違った情報を生み出すことも見てきた。また、LAD, NAD,そしてクロモゾームテリトリーのように核の構造との相互作用により決まるケースでは、部分が全体を構成し、全体が部分を組織化するという生命特有の性質を見ることができる。この生命特有の部分と全体、原因と結果問題は、進化過程を通してしか説明がつかないが、幸いそれぞれの構造は進化の異なる段階で誕生したことが、これら構造の系統学からわかる。この意味で、ゲノムを様々なレベルで構造化し、新しい情報を開拓してきた進化過程の研究は重要分野になる気がする。
[
西川 伸一 ]
構造部材としてのセントロメア DNA
2015年8月3日
ここまでゲノムには、転写して利用される情報だけでなく、構造(あるいは順序、位置など)としての情報も含まれていることを示してきた。今回は構造としての情報を考える最終回として、例えば家の柱や壁のような構造部材としてDNAが使われている場合について見てみよう。
すでにゲノムの一部はヘテロクロマチンという構造を取り、他の部分と比べてコンパクトに折りたたまれ転写が抑えられていることを紹介した。ただゲノムの中には常にヘテロクロマチン状態をとる領域と、細胞や分化段階に応じてヘテロクロマチン構造から解放され、転写が可能になる領域の2種類が存在する。常にヘテロクロマチン構造をとっているゲノム部位を調べていくと、全く遺伝子が存在しない大きな領域が見つかる。この領域のうち代表的なものが、セントロメアとテロメアで、共に真核生物の細胞分裂時に重要な働きをする。ここでは、セントロメアに焦点を当てて見てみよう。
まずセントロメアとは何か。真核細胞はDNAの倍加後、2つの細胞に分裂する。その時、細胞の中心に並んだ染色体を両方の細胞へと正確に分配する(図1)。
図1 細胞分裂中期。中央に並んだ染色体に微小管が結合して染色体を分離しようとしている。緑色蛍光は微小管、青色蛍光は染色体、赤い蛍光は動原体を染めてある。動原体は染色体セントロメアと微小管を結合させる構造である。(Wiki Commonsより)
この時、2つの細胞に別れた中心体から放射する紡錘糸(微小管)はキネトコア(動原体)を介して染色体と結合し、細胞分裂の経過とともに染色体を両方の細胞へと引っ張り込む。この動原体と染色体の結合の中心になっているのがセントロメアと呼ばれる場所のヌクレオソームだ。他の部位のヌクレオソームと比べると、セントロメアのヌクレオソームにはcenH3と名付けられた特殊なヒストンが存在している。このcenH3は動原体を構成する分子と結合して染色体と紡錘糸を結びつける役割を持っている。cenH3が普通のH3と置き換わって存在しヘテロクロマチン構造をセントロメアと呼んでいる(図2)。
私たちヒトの細胞ではセントロメアの数は染色体に一カ所あるだけだが、この様式は全ての生物に共通というわけではなく、例えば線虫では一つの染色体上に何カ所も形成される(図3)
図3 線虫とヒト染色体のセントロメアの位置をcenH3染色で示している。ヒトでは染色体中央に一箇所のセントロメアがあるが、線虫では一本の染色体に複数のセントロメアが存在する。
動原体は分裂が終わると消失する。したがって、分裂ごとに同じ場所にセントロメアが再構成される必要がある。即ち、cenH3とヘテロクロマチン型ヒストンが特定の領域のDNAと結合し特殊なヌクレオソームを構成する必要がある。この決まった場所に繰り返しセントロメアが形成されるメカニズムは完全にわかっているわけではない。最初、酵母を用いた研究では、セントロメアには一定の塩基配列が存在することが示され、セントロメア型ヌクレオソームは特定の塩基配列にガイドされて形成されると考えられた。しかし、ゲノムプロジェクトが進むことでセントロメアに特有の遺伝子配列があるという考えは揺らぐ。例えば、ヒトのセントロメアには171bpの長さのαサテライト配列と呼ばれる配列が繰り返しており、最も長い場合で5Mbにわたって存在している。マウスでも同じようなサテライト配列の繰り返し構造が存在することから、サテライト配列の繰り返し構造がセントロメア型ヌクレオソームをガイドする構造であると考えられた。しかし、馬の染色体の中にはこのような繰り返し配列が全く存在しない染色体が存在する。cenH3をリクルートするゲノム側の条件を理解することは一筋縄ではいかないことがわかった。いずれにせよ、セントロメアやテロメアはそれ自体何かをコードしているわけでもなく、また周りの遺伝子を構造化しているわけでもない。セントロメア領域から、様々な蛋白分子と共同して純粋に染色体の構造部材として働いているゲノム部分があることを理解していただいたのではないだろうか。
さて、染色体の構造部材としてのセントロメアはペリセントロメアと呼ばれるやはりヘテロクロマチン構造をもつ領域に挟まれている。ペリセントロメアは染色体が分離する際、染色体同士を結合しているコヒーシンと呼ばれる分子が最後まで残って結合している場所だ。このおかげで染色体が娘細胞に分配される時、最後に動原体部分が外れ、完全な染色体を分配することができている。この意味で、ゲノムのペリセントロメア領域もゲノムを支える構造部材と考えることができる。では、ゲノムのペリセントロメア領域をヘテロクロマチン化するための条件とはなんだろう?興味深いことに、セントロメアやテロメアと異なり、ペリセントロメアにはLINE,SINEを含む様々な繰り返し配列とともに、染色体の他の場所から転座してきた普通の遺伝子領域も見つかっている。したがって、繰り返し配列が存在するからヘテロクロマチン構造が生まれるのではなく、この領域自体が飛び込んできた遺伝子をヘテロクロマチン構造に変換する力があることを示している。このメカニズムについてはゲノムとRNAの関係という枠組みで次回に考えるが、飛び込んだ遺伝子をヘテロクロマチン化することで構造部分を拡大できる巧妙な仕組みが可能になっている。この観点に立つと、私たちゲノムの半分を占めるトランスポゾンの一部は構造部材として使われている可能性もある。というのも、ほとんどのトランスポゾンにヘテロクロマチン構造を取らせる仕組みを私たちは有している。この意味で(これは私の戯言だが)トランスポゾンは構造部材を新たに調達するにはうってつけの材料に思える。
3回にわたってゲノムが構造化されること自体新しい情報を生むことを見てきた。構造部材としてのDNAまでが情報と呼べるのは、構造も、材料も、コードも全て同じDNAを媒体とする線状の情報に置き換え、子孫に伝えるからだ。最初ただの物質でしかなかったDNAが様々なモノやコトと対応できる情報に転換する。最初DNAがコードとして何と対応付けられていたのかは21世紀重要な問題だ。これは私の戯言だが、おそらく最初に対応付けられたのはアミノ酸の並びではないような気がする。というのも、この対応関係はRNA,tRNAを必要として、あまりにも複雑だ。とすると、今セントロメアでみられるような部材としてのDNAと蛋白の関係と、DNA,RNAの関係が最初は別々に存在していたと考えたほうがわかりやすい。次回はこの問題を横目で睨みながら、ヘテロクロマチン転換のメカニズムから初めて、DNAとRNAの関係について考えてみたい。
[
西川 伸一 ]
DNA と RNA
2015年8月17日
DNAとRNAと聞くとすぐセントラルドグマ、すなわちDNA〜RNA〜ペプチド(タンパク)と続く情報から実体への流れを想像する。しかし、太古の昔、地球上で核酸が情報の媒体として使われ始めたとき、セントラルドグマに定式化されているDNA,RNA, タンパクの間の美しい関係があったとは考えにくい。DNAは地球上に物質として生まれた時点から、複製によって正確に伝えるという点ではすでに情報媒体としての条件を満たしている。ただ、最初から塩基配列のコードとアミノ酸が対応していたとは、神でも想定しない限りまず信じられない。すでに見てきたように、DNAはタンパク質のコード以外にも様々な情報を表現し、それを安定に子孫に伝えることができる。言い換えるとDNAはこれらゲノムの持つ全ての機能を最初に複製可能にした物質だったように思える。DNAが作り出す構造と、タンパクやRNAが、コードとは無関係に相互作用できることは現存のヌクレオソームを見れば明らかだ。一方、RNAとなるとさらに多様な構造を取り得ることがわかっている。実際RNAだけから特定の酵素活性を持つ構造を作ることが可能で、最初の生命体はRNAでできていたと考える人もいる。ただ生命がRNAから始まったという主張に完全に同意できないのは、複製という点でRNAが様々な問題を抱えているからだ。私自身は、まず物理化学法則に従って太古の昔にDNA,RNA,タンパク質が独立してランダムに生まれ、それが何か関わりあい続けるうちに突然情報体系への大転換を遂げたように思える。最近進んだノンコーディングRNA(ncRNA)の研究から、ncRNAがDNAやタンパクと直接関わりあって染色体構造を変化させているのを知ると、この過程に太古の3者の関係の名残が反映されているのではと妄想を巡らせてしまう。そこで、最後にこの妄想に付き合ってもらうためにncRNAが誘導するヘテロクロマチン化について見ておこう。
細胞が発現する全てのRNAを特定しようと試みたFANTOMやENCODEプロジェクトが終わって、全ゲノムの8割にも及ぶ領域が転写されているという事実が発表された時、私たちは何かの間違いではないかと驚いた。しかし前回紹介した、ヘテロクロマチン構造により固く閉ざされたゲノム領域であるセントロメアやペリセントロメア領域ですら転写されていることがわかり、低いレベルなら、クロマチンの構造とは無関係にゲノムのほとんどが転写されていることが認められるようになっている。ヒトセントロメアには174bの繰り返し配列からなるマイナーサテライト配列が、サテライトII,IIIを含む大きなメージャーサテライト配列からなるペリセントロメアに挟まれているが、この二つのサテライト配列もノンコーディングRNA(ncRNA)として、転写されている(図1)。
これまでの研究で、このncRNAがセントロメア、ペリセントロメアのヘテロクロマチン構造に重要であることが明らかになっている。例えば、マイナーサテライト配列から転写されるRNAはセントロメアにcenH3をリクルートするとともに、CENP-Cを含む様々な動原体の構成分子をこのヌクレオソームに結合させる機能を担っている。すなわち、セントロメアからRNAが転写されないと、正常のセントロメア・動原体の形成ができない。同じように、ペリセントロメアのメージャーサテライト配列から転写されたncRNAは、ヘテロクロマチン転換を誘導するタンパクHP1(ヘテロクロマチンプロテイン1)をペリセントロメアにリクルートし、ヘテロクロマチン構造を形成する。このようにそれぞれの領域の特異的なクロマチン構造を形成し維持するためには、低いレベルでRNAが転写されていることが必要だ。では、クロマチン構造を調節しているのは必ずその領域のゲノムから転写されるRNAだろうか?答えはNoで、様々なRNAがヘテロクロマチン誘導に使われていることがわかっている。最も大掛かりで典型的な例がX染色体不活化(XCI)なので次に見てみよう。
ゲノムからあまり間違うことなく予想できることの筆頭は男女の区別だ。男性はXY、女性はXXが人間の性染色体で、この差が男女を決めている。ただこの方式には一つ問題がある。すなわち男性にはXが1本に対して、女性は2本という数の差だ。というのもXには常染色体とおなじように生命維持に必須の遺伝子が存在するため、何もしないとX染色体上の遺伝子の発現量は女性が2倍になる。多くの遺伝子は発現に2倍の差があっても問題ないが、中には発現を男女一定に保っておく必要のある遺伝子もある。私たち哺乳動物はこの課題に、女性の片方のX染色体をすべて不活性化することで答えている。この不活化にはX染色体の不活化センターと呼ばれる部位に存在するXist遺伝子が主役を演じている。Xist遺伝子は8個のエクソンからなり、普通の遺伝子とおなじようにスプライシングを受けた後、polyAも普通に付加される(図2)。
Xist
RNAが他の遺伝子由来の RNAと異なる点は、RNAが核外に移動することはなく、従って翻訳もされない。転写が片方のX染色体だけに限られ、またもう一方のX染色体に結合しない巧妙な仕組みについて理解は進んでいるが、全て割愛して、とりあえずXist遺伝子から転写されたRNAは片方のX染色体全体を覆っていると理解してもらおう(図3)。
図3 メスの細胞では、片方の染色体だけがXistによりカバーされている。黄色で示されているのはXist領域で、両方の染色体に存在するが、XistRNAは染色体全体に広がっている。
先に紹介したセントロメアや、ペリセントロメアはその場所から転写されたRNAがホスト領域と結合するが、このXistは17kbの領域からだけ転写されるncRNAが染色体全体に結合する。したがって、Xist-RNAはDNAと塩基配列の相補性で結合するのではなく、Xist-RNA内に存在する繰り返し配列Cによりヌクレオソーム自体に結合することがわかっている(図2)。また、X染色体を覆うといっても実際にXistは2000個ぐらいしか発現していないことがわかっており、おそらくX染色体に飛び飛びに結合して、その場所からヘテロクロマチン構造を拡大していくのだろうと想像されている。実際Xistには遺伝子のサイレンシングやヒストンのメチル化に関わる分子をリクルートする繰り返し配列が何種類も存在しており、図2に示したrepeatAは遺伝子のサイレンシング、repeat F, Bはヒストン修飾に関わる分子、そしてrepeat CがXistがクロマチンと結合するのを媒介することがわかっている。このように、DNAとタンパク、ncRNAとタンパクがそれぞれ複合体を形成し、さらにこの両者が働き合うことで、ヘテロクロマチン構造が形成されていくのがわかる。この3者の相互作用には塩基配列コードは必要ない。
私たちのゲノムの5割はトランスポゾンで占められているが、最後にゲノムに飛び込んできたトランスポゾンをヘテロクロマチン化するメカニズムを担うPIWIタンパクとpiRNAについて見てみよう。海綿から人間まですべての動物に存在して、植物には存在しない遺伝子の一つがPIWI分子で、トランスポゾンの活動を抑える細胞レベルの防御反応の主役になっている。この時に働くRNAがPiwi interacting RNA (piRNA)で、のちに述べるようにこれは遺伝子の機能を抑制するための様々な分子を標的DNAやRNAにガイドする役目がある。このpiRNAは主に生殖細胞に発現している25-26のヌクレオチドからなる小さなRNAで、その種類は千種以上存在すると考えられ、2種類の方法で作られる(図4)。最初の方法は、ゲノム中に存在する200−数百kbのpiRNAクラスターと呼ばれる領域から転写される長いRNAがPiwi分子と結合して、短い機能的な長さに切り整えられることで作られる。このpiRNAクラスターには様々なトランスポゾンに実際に存在する領域が集められており、一種のトランスポゾンのカタログのような領域だ。従ってこのカタログ領域から転写されPiwi分子により処理されてできるpiRNAはトランスポゾン領域と相補的に結合することができる。このカタログのおかげで、ほとんどのトランスポゾンの配列を認識して、遺伝子発現を抑えるための機能分子をその領域へガイドすることができる。piRNAは、このクラスター外のトランスポゾンが活性化され転写が始まったRNAからも作ることができる。この時、トランスポゾン転写産物は、すでにその細胞に存在している相補的なpiRNAとpiwi分子上で会合し、トランスポゾンからの転写産物を短くカットする。こうして出来た短いRNAはPiwi分子上でさらに処理を受け、新しいpiRNAに変換される。どちらの方法でも、出来てきたpiRNAは様々なレトロトランスポゾンと相補的なガイドRNAとして働くことができる。
さてこうしてできたpiRNAとPiwi分子複合体は、piRNAによりガイドされてきた領域のヌクレオソームをヘテロクロマチン型に転換することができる。この場合、標的の情報はこれまで経験したトランスポゾン配列のライブラリーとしてpiRNAクラスターに記録してある。また、今活動しているトランスポゾン由来のRNAもpiRNAに変換してガイドに使うことで、トランスポゾンと他の領域を区別し、トランスポゾンだけをヘテロクロマチン化するのに関わっている。
以上の3つの例から、ncRNAが特定の遺伝子部位の染色体構造を決めるために重要な働きを演じているが、その形成方法と作用機序については多様性が大きいことがわかってもらえたのではないだろうか。さらにpiwiとpiRNAのペアには、ヘテロクロマチン化だけではなく、RNAによりガイドされて直接トランスポゾンのDNAをメチル化し、すでに転写されてしまったトランスポゾンRNAに結合してそれを分解する働きがあることがわかっている。この意味でpiRNAは、多様な武器をトランスポゾン攻撃に集中してその活動を抑える最前線の兵士のようだ。おそらく専門知識のある読者は、piwiとpiRNAの説明を見て、原核生物や古細菌に見られる外来遺伝子の侵入に対する防御機構、CRISPER/Cas9システムを思い出したのではないだろうか。次回は単細胞動物へとさかのぼってセントラルドグマとは異なるDNAとRNAの相互作用について調べてみよう。
[
西川 伸一 ]
ゲノムの自己
2015年9月1日
塩基配列が何を意味しているかわからないという理由だけでジャンクと名付けていた領域の中で、機能が明らかになって大ブレークしたのがクリスパーだろう。最初大腸菌ゲノムの中の不思議な繰り返し配列として見つかった配列(まさに当時はジャンク配列)が、実際には大腸菌に感染する様々なウィルスやプラスミドの断片であることがわかり、クリスパー上流にあるCas遺伝子群とともに、外来DNAを自己のゲノムから区別して抑制する一種の免疫システムを形成していることが明らかになった(図1)。
外来の遺伝子が侵入すると、その一部を切りとって、クリスパー領域に組み込むことで、侵入記録を遺伝子ライブラリーとして記憶(図1①)、次の侵入に備えるという免疫の仕組みだ。こうして形成された外来遺伝子のライブラリーは、Cas9と結合するRNAリピート領域と一体となったガイドRNAとして転写され、次に相補的外来遺伝子が侵入してくると、その遺伝子とハイブリダイズしてCas9を侵入遺伝子へと導き(図1②)、これを切断、分解する(図1③)。この最後の反応を利用して開発されたのが、遺伝子改変技術を根本的に改革したゲノムの配列特異的編集法で、今や医学応用を含めあらゆる生命科学分野で大ブレークしている。
さて外来遺伝子をライブラリーとしてゲノムの中に保持し、そこから転写されたRNAを標的遺伝子の抑制に使うという本来のクリスパーシステムを理解すると、まさに前回紹介したPiwi/piRNAとよく似た系だとわかるはずだ。まずどちらも自己と他を区別するための記憶として、外来遺伝子配列を特定の領域に蓄積し、それを自己ゲノムと他を区別するのに使っている。これも最初は機能がわからずジャンク配列とされていた。この例から、他のジャンク配列もまだまだ思わぬ機能が明らかになる可能性がある。進化では、役に立たないと決めつける方がいつも間違っていることが多い。
さて、クリスパーやPiwi/piRNAの例から再認識刺されるのは、情報としての自己のゲノムは、他のDNA情報に常に開かれていることだ。いつでも他のゲノムは自分のゲノムの中に侵入してくる。このため常に自己の情報と他の情報を区別して、自己の情報だけを守る仕組みが生命誕生後の早い時期から存在している。驚くべきことに、この機構を拝借して逆にホストのゲノムを分解する能力を獲得したしたたかなウイルスすら存在している。このphageウイルスは幾つかのCas遺伝子と侵入したバクテリアが持つ防御最前線で戦う分子PLE遺伝子をアタックできるクリスパー配列を持っている。すなわち、本来バクテリアがウイルスゲノムの侵入を守るセットを使って、ウイルス抵抗性に関わる遺伝子を攻撃して自らを守っている。生命誕生は、自己と他という関係の誕生でもある。自己のゲノムを他から区別する仕組みはこのように、ウイルスを含むあらゆる生物へと拡大する宿命にある。
クリスパーからわかるように、ncRNA(non-coding RNA)はあらゆる生物で機能しており、生命誕生初期から、あるいはそれ以前からこのようなDNAとRNAの関係があったことをうかがわせる。しかし、なかでもゾウリムシやテトラヒメナのような繊毛虫類でのncRNAの大胆な使い方には驚かされる。最後に、テトラヒメでncRNAがどのように使われているか見てみよう。ただその前に、これまで紹介しなかったsiRNA(small interfering
RNA)について、piRNAと比較しながら簡単に紹介しておく。Piwi分子の結合するpiRNAは、piRNAクラスターか活性化されたトランスポゾン由来だが、どちらも転写された一本鎖RNAだ。ただ、様々な方法でできてきた2本鎖RNAからも同じような遺伝子抑制性のRNAを形成することができ、siRNAとよばれている(図2)。
この系では、2本鎖RNAはDicerと呼ばれる分子で決まった長さに切断された後、piwi分子の代わりに、RISCと呼ばれる分子にロードされる。このアンチセンスRNAとRISCの複合体は、このRNAをガイドとして、外来RNAの分解や、標的遺伝子のヘテロクロマチン化に関わっている。ガイドに利用するRNAが最初2本鎖である点がpiRNAと異なるが、共にトランスポゾンの活動を抑制するメカニズムだ。この2つのメカニズムを頭に入れておいて、次に繊毛虫類の一つ、テトラヒメナを例に驚くべき精巧なncRNAの利用法を見てみよう。これから述べる話のほとんどはウィーン・IMPに在籍するこの分野の第一人者、望月一史さんたちの総説を参考にしたことを断っておく。
さてゾウリムシやテトラヒメナは、一つの単細胞の中に大核と小核の2種類の核を持っており転写は大核からだけに限ることで、高い転写効率を達成している。以後は望月さんたちの研究しているテトラヒメナに限って見ていこう(図3)。
さて栄養が豊富な環境では、テトラヒメナは分裂により増殖する。この時、大核も小核も同じように複製され、両方とも娘細胞に分配される。一方、栄養条件が悪くなると、2つのテトラヒメナが接合し二つの個体で遺伝情報の交換を行う。おそらく異なる個体のゲノムを合わせることで、厳しい環境に適応しやすくするための戦略と考えられる。しかしこの時、高等動物の減数分裂に当たる過程が小核だけで起こる。Wiki commonsからの図を参考にして接合過程を見てみよう。まず図の左上から、減数分裂により一倍体の小核を最終的に1個形成する(残りの小核は全て分解される)。次に小核が分裂して一つの細胞の中に2個の1倍体の小核ができる。この間、大核はそのままで転写を続け細胞を維持している。次に、それぞれの個体は小核を交換し合って、最終的に別々の個体由来の一倍体の小核が融合した2倍体の小核が生まれる。この小核はその後2回の分裂により4つの小核を作り、そのうち2つが新しい大核を形成するのに使われる。この小核から大核への転換時に、それまで転写をまかなっていた大核は分解する。こうして生まれた新しい2つの小核と2つの大核を持った個体が次に分裂することで、接合した結果できた新しい遺伝情報を持った一個の大核と一個の小核を持つ2つの個体が生まれるという複雑な過程だ。
なぜこれほど複雑な接合過程を持っているのか不思議だが、これは大核のゲノムと小核のゲノムが異なっていることに起因する。正確に言うと、小核中のゲノムには全域にわたって6000以上の0.5-30kbの遺伝子断片が挿入されていて、IES(internal eliminated sequence)とよばれている。IESもクリスパー・piRNAと同様にトランスポゾンや繰り返し配列から出来ており、これまでの定義ではジャンクと呼ばれる配列だ。しかし、IESは有性生殖の初期以外の時期において、小核からの転写を抑制する積極的役割を持っている。すなわち全てのジャンクはジャンクであることで機能を持つ。一方、小核から大核ができるとき、新しい大核内の全てのIES(=ジャンク)が正確に除去されないと、遺伝子の転写ができない。実際、大核にIESが残ってしまうとテトラヒメナが死んでしまうことがわかっている。これに加えて、大核のゲノムは250ぐらいの断片に分解され、それぞれは増幅されているおかげで、転写レベルを上げるよう改変されているが、この過程についてはここでは深追いしない。
ではどのようにしてIESは小核ゲノムから正確に除去されるのだろうか?ここにDicerやPiwiに似た分子と、小核から転写されるncRNAが一役買っている(図4)。まず新しい大核への転換が始まる前に小核全体が双方向性に転写され、ゲノム全域をカバーする2本鎖RNAが形成される。この2本鎖RNAはDicerに似た分子Dcl1pによって小さく断片化されncRNAになり細胞質へと移行し、piwiに相同な分子Twi1pに結合する。Twi1p上でガイドRNAだけを残してパッセンジャー鎖は除去される。こうして形成したガイドRNAを結合したTwi1pは大核に移行し、大核中のゲノムと比較され、大核中に存在する配列が全て除去される。この結果残るのはIESに対応するRNAをと結合したTwi1pだけになる。
この選択が実際にどう起こっているのかは研究途上にあるようだが、大核のゲノムと相補的なRNAはゲノムDNAによりTwi1pから引き剥がされ、分解されると考えられている。メカニズムはともかく、これにより大核ゲノムと小核ゲノム間で引き算を行うことができ、結果として全てのIESに相当するncRNA をロードしたTwi1pが残る。次にこのTwi1p/ncRNAは新しく形成された大核に移行して、今度はIESに結合し、IESをヘテロクロマチン化する(H3K9, H3K27のメチル化)。このヘテロクロマチン化が標識となって、IES配列がゲノムから全て除去される。残念ながら、ヘテロクロマチン化された領域がどのようにゲノムから切り離されるかについての具体的なメカニズムについてはまだまだ明らかでない。しかし、テトラヒメナでは小核ゲノムからIESを大規模かつ正確に取り除く目的でncRNAが利用されることがわかる。
IESの多くがトランスポゾンを起源としていることを知ると、テトラヒメナではトランスポゾンが自己ゲノムを調節する機能ユニットとして積極的に活用されていることがわかる。テトラヒメナの2核構成も情報論から見ると面白い。一般的に情報理論は、伝えるためのコミュニケーション理論とオペレーションのためのコンピュータ理論に分かれる。ゲノムもそうで、子孫に伝える役割と、細胞のオペレーションとに役割を演じ分けている。問題はオペレーションのための情報は、伝えなければならない情報のほんの一部だということだ。そのため、真核生物はエピジェネティックな機構を進化させ、様々な方法でオペレーションに必要でないゲノム領域をオペレーションから隔離し、オペレーションの邪魔をしないよう抑制している。しかし、分裂のたびにエピジェネティック標識を正確に再構築するためには複雑な機構が必要になる。その代わりに、必要のない領域を全て除去した大核と小核に分けて、オペレーションと伝達を完全に分離してしまう戦略は、一見複雑に見えても、実は最も簡単で安心な戦略なのかもしれない。実際、テトラヒメナは普通、両方の核をただ単純に複製し続ける。そのとき、エピジェネティック状態を常に再構築しないで済むことの利点は計り知れないはずだ。このように情報のコミュニケーションとオペレーションを分離したテトラヒメナは驚くべき生物と言えるだろう。
これでゲノムの構造については終わり、次からはゲノムの働きについて考えていく。
[
西川 伸一 ]
ゲノムの働き
2015年9月15日
ゲノムの解剖学に続いて、次はその働き方を見てみよう。前回紹介した、ゲノム情報を大核と小核に分けて使っているテトラヒメナは、ゲノムの働きを理解するための優れたモデル生物になっているので、これを参考にしながら見ていこう。
ゲノムの働きの第一は、複製を通して親と同じゲノム情報を子孫に伝えることだ。無生物と比べる時、生命が示す特徴の一つは複製(replication)だ。私たちの細胞のように有糸分裂で増殖する細胞の場合、細胞分裂時にほぼ正確に複製され、子孫細胞に分配されるものに、ゲノムと中心体がある。しかし、原核生物になると複製分配されるのはゲノムだけになる。生物全体を通して見たとき、複製されて子孫に伝達されるものは結局ゲノムしかない。このことから、ゲノムの働きは親と同じ状態を増殖させるためコピーして子孫に伝える情報としての働きがあることがわかる。
しかし正直に言うと、なぜ生物は分裂し、増殖しようとするのかについてはよくわからない。熱力学に逆らって、平衡に陥らないようにメタボリズムを維持するだけなら増殖は必要ない。実際、全く分裂しない赤血球は200日の寿命があるし、神経細胞のように数十年にわたって分裂なしに生き、新陳代謝も盛んな細胞は存在する。ただ、複製のない細胞システムはどれほど新陳代謝が維持できたとしても、環境が変化してしまえば物理的に滅びる。環境に適応し、さらには環境まで変えてしまえる可能性があるという点で、結局は複製能力を持つシステムだけが地球上で生物として存続できたのだろう。
一方複製自体に情報の複製は必要ない。例えばウイルスの被膜を考えてみよう。被膜形成に必要な幾つかの構成タンパクが必要なだけ調達できるなら、一定の大きさのウイルス被膜は自然に形成される。ここでもし被膜が物理的強度の問題で一定の大きさになると壊れると仮定しよう。不完全な被膜は、壊れた一部を核にしてもう一度完全な新しい被膜を形成できるだろう。すなわち、平衡から遠く離れた条件さえ満たせれば、形成、破壊、再形成を繰り返して増殖するウイルス被膜のような構造は十分考えることができる。同じように、例えば核のないプロトセルのような液胞が一定の大きさになると物理的にちぎれるとしよう。このちぎれる限界の細胞内成分の量と膜の強度(この時膜も自然に成長するとしておく)が物理的に決められておれば、情報はなくても一定サイズになると2個の液胞が作られ、またその液胞が分裂するというサイクル、すなわち複製サイクルを考えることは可能だ(実際そのような実験が行われている)。しかし実際には、何らかの情報がないと同じものを作り続けることは難しく、生成されるプロトセルの大きさも時間とともに大きくばらつくだろう。判を押したように同じ大きさのプロトセルを作り続けるためには、デザインや機能を指示できる情報が増殖には必要になる。
もちろん情報といっても、最初から核酸が情報媒体を担っていたと考える必要はない。例えばたんぱく質の構造を変化させるだけなら、プリオンのような例もある。しかし、増殖・生存に必要な情報を、核酸媒体を使って細胞の化学的オペレーションから完全に分けることに成功した私たちの先祖だけが結局地球上で生き残れた。この結果、現存する全ての自立生命は、DNAをゲノム情報の媒体として使っている。このように、ゲノムの働きの第一は、生物の増殖を支えることになる。
テトラヒメナにもどろう。テトラヒメナは単細胞生物で、通常は分裂により増殖する。このとき、大核も小核も同じように複製され、それぞれの娘細胞に分配される。では両方の核が複製されることはテトラヒメナの維持に必要なのだろうか。例えば、小核を除去したテトラヒメナは増殖が可能だろうか? 実験が行われたかどうか明らかではないが、おそらくかなりの期間分裂を続けることはできるだろう(原理的には無限に分裂していい)。実際、核を一つしか持たない真核生物の方がこの世には多く存在し、増殖を繰り返している。テトラヒメナの場合大核ではゲノムが200以上に断片化されているなど、特殊な構造を持っているため、大核は長い期間にわたって安定な複製を維持しにくいかもしれないが、基本的には小核がなくとも増殖は可能だろう。
では小核は何をしているのか?前回説明したように、小核は二つの個体の接合時に独自の活動を始める。まず減数分裂を行い1倍体の核を2個形成する。次に、同じように減数分裂によりできた他の個体からの1倍体の小核を交換し合い、最終的に融合する。この結果、異なる個体のゲノムを集めた2倍体の核が作られる。この小核からまず新しい大核と小核を作り直したあと、その後は通常の分裂増殖サイクルに戻る。
この複雑な過程から出来るのは2倍体の小核なのに、なぜこれほど面倒臭いことをしなければならないのか。テトラヒメナの小核の場合、新たに何千箇所もの挿入配列を取り除いて大核まで作らなければならない。なぜこんな複雑な仕組みが選ばれたのか?一つの可能性については前回述べた。ここまで複雑な接合の仕組みが維持されていることは、テトラヒメナにとって最も効率のいい方法なのだろう。
もともと異なる個体間でゲノム情報を交換し合い、ゲノムレベルの雑種を作ることは種の生存のために重要だ。もちろん逆もあるだろうが、一般的に多様な情報を持っている方が多様な環境に対応できる。もう一つ重要なのは、これにより有害な突然変異を元に戻したり、薄めたりできる。ゲノムでは接合だけが異なる個体の情報を一つの個体に統合することを可能にしている。接合だけではそれぞれのゲノムは独立したままで、いわば2人3脚ではあっても本当の融合ではない。しかし、次の減数分裂が起こるときには、染色体間で相同組み替えがおこる。すなわち染色体同士で部分の交換が行われ、異なるゲノム由来の情報が一つのゲノムに文字通り融合する。テトラヒメナでは、このゲノムの統合、交換、融合を通したゲノム情報の間のコミュニケーションを小核が専門的に行っている(前回の図参照)。一方、ほとんどの真核生物は、これを一つの核で行っている。
生物学ではこのゲノム間のコミュニケーションを「性」と定義している。ほとんどの真核生物ゲノムが共通に持つ働きだ(例外については最後に紹介する)。テトラヒメナの場合、個体全体が接合したままコミュニケーションが行われるが、より一般的な戦略は、コミュニケーション(接合)用の細胞が特別に分化し、その細胞同士で融合が起こる。またこの細胞を作る過程で減数分裂が起こり、ゲノムの交換と融合が可能になっている。例えば、出芽酵母では2倍体の分裂個体が減数分裂で1倍体の胞子を作り、この胞子が接合して2倍体の個体を作る(図1)。一方、生殖細胞が体細胞から分離した高等動物では、この減数分裂と接合は、生殖細胞系列の配偶子、例えば精子と卵子、植物では花粉や雌しべの役目になる。それぞれが分化し接合する方法は全く異なるが、全てで共通に行われているのは個体間のゲノム情報の交換だ。面白いのは分裂個体が減数分裂サイクルに入るのはほとんどの場合、外界の栄養状況が悪くなるなど逆境に晒された時だ。すなわち、逆境では他の個体と情報交換することで、自分にはない能力を取り込める可能性がある。この異なる個体間でゲノム情報を交換するコミュニケーション能力が、生存に負の作用を持つ突然変異を薄め、ゲノムの多様性を増大させてきた。まとめると、ゲノムの働きの第2は個体間でゲノム情報を交換することだ。
ゲノムの働きの第3は多様化して進化の原動力になることだが、この話題は次回に回す。今回は、2番目の働き、性、すなわちゲノム間のコミュニケーションを全く行わない生物のゲノムについて最後に紹介して終わる。2年前の8月Natureにワムシの一種belloid
rotifer(Adineta vaga)ゲノムについての論文が掲載され、注目を浴びた(Nature, 500:453-457, 2013, 幸いこの論文はcommonsとして図の掲載が許されている)。注目を浴びた最大の理由は、このワムシに性別や、雌雄同体や、減数分裂の気配が全くないからだ。すなわち、異なるゲノム間の情報交換なしにワムシが何千万年も生きてこられた秘密がゲノムからわかると期待したからだ。期待通り、ワムシは2重人格とも言えるゲノム構造を持っていた。
図2 ワムシゲノムに見られる対立関係にある遺伝子とオオノログ(ohnolog)な関係にある遺伝子のマップ。ワムシの遺伝子の多くは、相同性の高いペア遺伝子(青色で示す)、すでに多様化が進んだペア遺伝子の2種類を持っている。
図2には、この論文の図2bをそのまま掲載したものだが、ここで青い線で結ばれているのが相同性の強い対立遺伝子に相当する遺伝子ペアで、一方オレンジの線で結ばれているのが故大野乾博士の名前に由来するOhnologous遺伝子ペアだ。Ohnologous遺伝子とは、全ゲノムの重複後にコピーされた遺伝子を失わずに保持している重複遺伝子で、独立に進化し多様化してきた。ここでavとあるのはワムシゲノムでアッセンブリが確定している領域と考えて貰えばいい。重要なことは、ワムシでは対立遺伝子といっても二倍体のゲノムが存在するわけではなく、一つのゲノムの中に対立遺伝子セットが組み込まれていることだ。さらに、ゲノム重複によるペアも独立に存在するという不思議な構造をとっている。ゲノムは情報交換なしに単独で分裂を続けると、変異が蓄積して維持が難しくなる。ゲノム間で情報を交換しあうことは、この問題の解決のために必要で、真核生物は性生殖を通してこれを行う。性のないワムシでも、やはり情報交換が必要で、対立遺伝子の代わりに、重複した遺伝子を同じゲノム上で維持し、その間で情報交換することで異常が蓄積しないようにしている(図3)。
図3で示すように、この同一ゲノム内の相同遺伝子間の情報交換は、相同組み替えではなく、遺伝子転換で行われていると考えられている。相同遺伝子が同じゲノム上に散らばるワムシのようなゲノム構造が一旦できると、減数分裂、接合過程を介した情報交換はうまくいかないと考えられる。なぜなら、異なる個体の配偶子同士が接合したとしても、相同組み替えのための染色体のペアリングが正確に行えない。
この図からわかるように、同じゲノム上に存在していても、独立した対立遺伝子のペアを持つことで、ペアどうして相互に情報を交換して、有害な突然変異などを除去することが出来る。他にも、ゲノム内対立関係にある遺伝子と、それに対応するOhnologous遺伝子を比べると、相同性に大きな違いがあることから、相同組み替えがなくとも、遺伝子転換(gene conversion)メカニズムにより十分な多様性が得られることがわかる。
性生殖をやめたのが先か、ゲノム構造が特殊化したのが先かよくわからないが、結果的にワムシは有性生殖に頼らず、分裂に伴う遺伝子転換などの情報交換のみで多様化し、何千万年も生きることができている。面白おかしく考えると、ワムシは、普通なら異なる個体間に存在する対立遺伝子が一つのゲノムの中に統合されている2重人格者と言えるかもしれない。ただ、異なる個体間の情報交換をやめてワムシが何千万年も生きているからといって、性を通した個体間での情報交換が不必要かどうかはわからない。というのもワムシは普通の生物にはない不思議な性質をいくつも持っている。例えば、完全に乾燥しても水に触れれば生き返る。また放射線にも驚くべき抵抗性を示す。これほどの環境に対する耐性を獲得してしまえば、個体間の経験の差など取るに足らないのかもしれない。
[
西川 伸一 ]
続・ゲノムの働き
2015年10月1日
昨年5月、第6話 で紹介したようにダーウィンの進化論の柱の一つは、集団内で形質の多様化が自然に起こるとする考えだ。ゲノムやDNAはおろか、遺伝の法則についても何もわからなかった時代にダーウィンがこれを着想したことに驚く。一方自然選択の概念は、マルサスや、適者生存による社会進化を唱えたスペンサーの著作からわかるように、当時の社会的思想風潮の一つではなかったかと思う。ダーウィンも適者生存の法則を説明するより、自然に起こる形質の多様化についての説得がはるかに難しいと予想していたのだろう。「種の起源」を集団中に自発的に起こる多様化の話から始めている。しかし、ゲノムの理解が進んだ今日では、自然に起こるゲノムの多様化(突然変異)が形質の多様化の背景にあることを疑うものは誰もいない。逆に自然選択については、適者生存といった単純なものではなく、形質の自然選択によるゲノム変化の研究は複雑で挑戦的な分野だと考えられるようになっている(後にできる範囲で議論したい)。進化がゲノムを持つ生物に内在する機能である以上、生物の多様化を推進する原動力がゲノムの3番目の働きになる。
私たちのゲノムに変異が導入される方法は、点突然変異から全ゲノム重複まで、極めて多様だ。具体的には、1塩基置換、欠損、挿入による点突然変異、小さな配列の挿入・欠損・逆位、染色体を含む大きな領域の欠失、挿入、転座、重複などがあり、全てがゲノムの多様化に寄与する。これほど多様な方法があるとわかっていたらダーウィンも苦労せずに済んだだろう。もちろんこのような変異は理論的可能性というだけではなく、実際に一定の確率で起こっていることは、多くのゲノムデータが蓄積されてきた現代では当たり前のことになった。ヒトゲノムを比べてみると、一塩基置換による特定部位多形性、すなわちSNP(single nucleotide polymorphism)は一千万箇所、小さな領域の挿入、欠損、逆転による変異は10万箇所に上ることが知られている。大きな染色体の変異となると、さすがにヒトゲノムデータベース内に見つけることはほとんどできないが、染色体重複だと例えば21番染色体の重複によるダウン症は有名だ。さらにがん細胞を調べると、様々な大きなスケールの変異を目にすることができる。例えば小児ガンの一つ神経芽腫の多くは13番染色体の特定部分が欠損することが知られているが、1983年に13番染色体全てが一本欠損した神経芽腫が発見されている(Science 219, 973-975, 1983)。他にも、ガンの遺伝的原因として染色体転座と呼ばれる異なる染色体同士の結合が知られている。例えば、ほぼ全ての慢性骨髄性白血病細胞は9番染色体と22番染色体の一部が結合した新しいキメラ染色体が形成される。これにより、bcr分子とabl分子が結合したキメラ分子が生まれ、これが血液幹細胞の増殖を促進し、白血病を引き起こす。こうして獲得される増殖優位性も適者生存の一つの形と言えるだろう。このような転座がガンの引き金になっている例は数え切れない。
ゲノムの多様化を考える時ガンゲノムから学べるもう一つの重要な事は、細胞が増殖を続ける中で驚くほど多くの変異が蓄積して行く事だ。例えば多数の悪性黒色腫の全ゲノム解読を行った論文によると(Cell vol161, 1681, 2015)、それぞれのガンごとに1Mbあたり平均16.8個の何らかの変異が見つかる。ヒトゲノムを3Gと考えると、この数字の3000倍、すなわち約5万個の突然変異が、ガンに蓄積していることになる。そしてこの中に異常増殖や転移性などに関わる機能的変異が複数個存在している。本当に個体の形質の多様化が目に見える形で起こっているだろうかというダーウィンの心配は全く杞憂でしかない。私たちのゲノムは猛烈な勢いで多様化するようできているようだ。
では、これほど様々な方法でゲノムを多様化させる原動力は何か?一時世間を騒がせたガン研究の大御所Vogelsteinたちが発表した論文にこのヒントがあるように思う(Science, 347,78, 2015)。私たちの体にはガンになりやすい組織となりにくい組織がある。この論文は、組織ごとのガンの起こりやすさと、その組織を維持するために必要な幹細胞の増殖回数をプロットして、両者が見事に相関することを示した論文だ。例えばガンの発症の多い直腸は、組織の維持のため幹細胞が10の13乗回近く分裂しなければならない。一方、小腸は長いように見えても幹細胞全体の全分裂回数は大腸の50分の1で、ガンの起こる頻度は100分の1であるのと一致する。すなわち、ガンにかかりやすさは、ガンが発症する組織の維持に必要な幹細胞の分裂数に比例し、つまるところ分裂時に起こる全く確率論的な変異により決まっているとする結論だ。もちろん生活習慣要因もガンのかかりやすさを変化させるが、背景となる分裂との相関は変わらないとした。これに対し、あまりに単純化しているとの非難の声が上がったが、私にとっては当然のことに思えた。というのも、ゲノムの複製は最も変異リスクが高い過程であることがわかっているからだ。2013年、7000にのぼる異なるガンのエクソーム解析からガンでどのような突然変異が起こっているか調べたNatureの論文(502,258,2013)でも、様々なガン共通に見られる突然変異の種類(例えばCからTへの変異)は、DNA修復や複製時に起こることが明らかになっている。DNA修復というと、私たちは放射線や紫外線、あるいは様々な化学物質などによるDNA損傷に対処するためのメカニズムだと思ってしまう。確かに地球上で暮らす限り損傷を避けることができないため、損傷を受けてもすぐに修復するための複雑な仕組みを開発してきた。実際、タバコや紫外線で修復が追いつかないほど損傷を受けるとガンの発生は上昇する。また修復酵素の力が弱まると少し紫外線に当だけでガンになる確率が高まる。その例が色素性乾皮症で、皮膚ガンの発症率は正常の20倍以上に達する。しかし普通の生活で起こる放射線照射や化学物質暴露よりはるかに強い突然変異誘発要因が存在している。それがDNA複製だ。詳しくは述べないが、DNA複製は2本鎖がチャックで開いたり閉ったりするように連続的に起こるものではなく、3種類のポリメラーゼ(一つはプライマーゼとも呼ばれている)が関わる複雑な不連続過程だ。この解明には当時名古屋大学の故岡崎博士の貢献が大きく、複製された短い不連続なDNA鎖を彼の名をとって岡崎フラグメントと呼んでいる(サイエンティストライブラリー岡崎恒子夫人の記事で詳しい解説有り )。最近DNAの変異が岡崎フラグメントの5’ 端に集中しており、これが複製間違いの多いポリメラーゼαで複製される短いフラグメントが完全に除去されず残ってしまうためであることが報告された(Nature 518,502,2015)。さらにポリメラーゼの複製間違いを修復する酵素(ミスマッチ修復酵素)の機能低下が多くのガンの引き金になっていることも分かっており、この酵素が先天的に欠損した小児のガンでは、普通のガンの何十倍もの突然変異が蓄積している(Nature Genetics 47,257, 2015)。これは点突然変異の話だが、染色体レベルの大きな変異の多くはやはり細胞分裂や減数分裂時に生じることがわかっている。これらの例から、形質の多様化の背景にあるゲノムの多様化を駆動するもっとも大きな原動力とは、生命に必須の細胞増殖そのものであることがわかる。言葉を変えると、複製されて子孫に分配されるというゲノムの働き自身が、多様化の原動力になっている。
最後に、生命の維持に必須のタンパク質や機能的RNAを作り続けるための情報としての働きがゲノムの4番目の働きで、テトラヒメナの大核が担っている。ただこの働きについては、ゲノムの解剖学 で詳しく述べたので割愛する。
以上紹介したゲノムの4つの機能から見えてくるのが、ゲノムが時間スケールの異なる未来に向けての情報として用意されていることだ。まずゲノムは次の瞬間から未来に続く生命の維持のために、必要なタンパク質や機能RNAを必要な量だけ作り続けるための情報として働いている。次に、あらゆる生命は増殖を維持することが必要だが、ゲノムはこのとき様々な時間スケールで必要とされる細胞増殖の際に子孫細胞に分配するためコピーされる情報として働いている。以上二つのゲノム情報の働きが関わる時間はほぼオーバーラップしており、いずれも現在の環境に対応して生命を維持することに関わっている。ところが、テトラヒメナの小核の説明で述べたように、個体同士の情報交換の媒体としてゲノムは働いている。単細胞動物では、この交換は通常環境が変化したとき行われることから、もう少し長いスケールの時間で予想される環境変化に対応する情報として働いている。そして最後に、ゲノムは複製時に多様化する性質を身につけることで、遠い未来に備えるための進化可能性媒体として働いている。このようにゲノムは情報として様々な未来に備える働きをしている。面白いのは、転写や増殖のような近い未来に対しては、変化を抑えるよう安全弁を働かせ、一方、もっと長いスパンで予想される環境の変化に対しては自ら変化する性質を積極的に利用して備えている。
今回は、図のない説明になってしまったが、これでゲノムの働きについての説明は終わる。次回は、DNAを媒体とする生物の情報と、私たちが情報という言葉で一般的にイメージするものとの相違について見ていく。
[
西川 伸一 ]