2023年11月9日
現役時代は徹夜することもあったが、覚えている限り次の日はあまり調子よくなかった。ましてや、活動的になって仕事がうまくいった覚えは全くない。ところが今日紹介する米国ノースウェスタン大学からの論文は、働くための徹夜は、ドーパミン神経を活性化する結果、活動性が上昇し、ストレスによるうつ症状も改善する、という意外な研究で、11月2日 Neuron にオンライン掲載された。タイトルは「Dopamine pathways mediating affective state transitions after sleep loss(寝られないとドーパミンを介して感情状態の変化が起こる)」だ。
この研究のポイントの一つは、マウスにあまりストレスを与えることなく睡眠を妨げる方法を開発したことだ。通常眠りを妨げるためには、音や光で睡眠を妨げるか、ケージの床が動かせて眠りを妨げる。後の方法は徹夜で働く状況に近いが、しかし動く床で動きながら飲んだり食べたりするため、環境が悪化し感覚的ストレスになる。この研究では動く床とともに、少し高いところに小さなプラットフォームを作成し、ここからしか飲み食いが出来ないようにすることで、環境を清潔に保ったまま、しかし動き続ける状況を作っている。
これにより睡眠を完全に阻害したあと、すぐに様々な行動テストを行うと、まず活動性が高まり、さらに性的活動性も高まる。また、知らないマウスに対する攻撃性はほぼ2倍に上昇する。これだけでなく、電気刺激を続けて誘導したうつ状態も、一回完全に睡眠を妨げることで大きく改善することがわかった。
これらの行動の背景にはドーパミン神経の活動があることがわかっているので、視床腹部のドーパミン神経を阻害できる遺伝子改変マウスを用いて、睡眠を妨げている間中ドーパミン神経が働かないようにすると、睡眠を阻止することで現れる症状のほとんどが消えることがわかった。ただ、性的活動の上昇は変化がなかった。
ドーパミン神経は様々な領域に投射している。そこで、側座核、内側前頭前皮質、視床下部、そして線条体にそれぞれ投射するドーパミン神経を逆行性アデノウイルスベクターを用いて阻害すると、側座核へのドーパミン神経阻害では他動だけが抑制され、視床下部へのドーパミン神経抑制では性的活動性上昇が抑えられ、ストレスによるうつ症状の改善効果は前頭前皮質へのドーパミン神経により調節されていることがわかった。一方、攻撃性などの社会性については、様々な領域が関与していることもわかった。以上の結果は、ドーパミン神経は投射場所に応じて異なる行動を支配しているが、睡眠が妨げられると、ほぼ全ての経路が活性化していることがわかった。
最後に、このドーパミン刺激が、それぞれの領域でのシナプス形態を変化させる可塑性を誘導していることも、スパインの形状変化に必要なシグナルを抑える方法で確認している。
以上が結果で、そのまま徹夜をうつ病の治療に使うわけにはいかないと思うが、一つの可能性として慎重に人間でも効果を確かめるのは重要だと思う。
2023年11月8日
Treg は免疫システムを制御して自己抗原に対する反応を抑える重要な細胞で、現在大阪大学の坂口さんにより発見された。これは抗原特異的細胞を標的にする反応が念頭にあるが、損傷を受けた組織で炎症を抑える保護作用も最近注目されている。
今日紹介する論文は、以前「胸腺びっくり動物園」として紹介し、YouTube 配信も行った胸腺トレランスに関する重要な発見を行った Dian Mathis 研からの論文で、運動による筋肉の炎症を抑え、運動機能を高めるのに抑制性T細胞(Treg)が重要な働きをしていることを示した論文。11月3日 Science Immunology に掲載された。タイトルは「Regulatory T cells shield muscle mitochondria from interferon-γ–mediated damage to promote the beneficial effects of exercise(抑制性T細胞は筋肉のミトコンドリアをインターフェロンγ から守り運動機能向上に寄与する)」だ。
この研究では、マウスに乳酸は高まるがクレアチンキナーゼは高まらない程度の運動を課すと、運動後24時間をピークに筋肉に免疫細胞やマクロファージが集まり、インターフェロンγ が分泌されることで、筋肉疲労が起こることを、組織学的、RNA解析などから確認している。また、運動を自由に続けさせる慢性運動では、2週間目がピークの細胞浸潤、ミトコンドリアの酸化リン酸化の上昇が起こること明らかにする。
この実験系で、Treg だけジフテリアトキシンで除去する実験系を用い、運動による筋肉組織の変化を調べると、リンパ球の浸潤が抑えられず、インターフェロンγがさらに上昇し、炎症反応が高まるとともに、筋肉障害も起こることを発見する。
この結果、Treg 存在化では認められる運動後に見られる筋肉の酸素消費量上昇を介する運動機能の上昇が認められず、 Treg が筋肉負荷後の運動能増強に必須であることを示している。すなわち、運動負荷は筋肉自体に様々な変化を誘導するが、同時に炎症を誘導してしまう。この炎症の効果を Treg が抑えることで、運動負荷による筋肉増強を守っていることがわかる。
実際、Treg が存在しないと、筋肉のミトコンドリアは膨らんでしまい、回復増強過程での酸化的リン酸化が維持できないことがわかる。
最後に、Treg がこのような機能を発揮できる原因を探り、他の組織障害に続く炎症時と同じで、インターフェロンγ の産生を抑制することで、筋肉を炎症から守っていることがわかる。実際、インターフェロンγ に対する抗体を注射すると、Treg が存在しなくても、炎症を抑え筋肉増強が可能になる。また、インターフェロンγ 受容体が筋肉で欠損したマウスでは、運動付加による運動機能の上昇が著しい。
以上が結果で、運動することは身体に良いが、局所の炎症を誘導してしまうので、これに対応できないと、運動の良い効果が発生しない。これを担っているのが Tregで、主にインターフェロンγ 抑制を介して機能を発揮していることになる。
日常の運動は、カロリー制限とともに、長生きの秘訣とされているが、この一端を Treg による炎症抑制が担っているとすると、Treg を高める長寿法も可能かも知れない。
2023年11月7日
今日は膵臓ガン制圧に向けた新しい経路についての研究を2編紹介する。
まず紹介したいのはテキサス大学からの論文で、膵臓ガン細胞特異的にフェロプトーシスを誘導して免疫を高める治療法の開発で、11月1日 Science Translational Medicine に掲載された。タイトルは「Tumor-specific GPX4 degradation enhances ferroptosis initiated antitumor immune response in mouse models of pancreatic cancer(マウス膵臓ガンモデルで、腫瘍特異的に GPX4 を分解することでフェロプトーシスに誘導されるガン免疫を誘導できる)」だ。
細胞死では様々な炎症物質が周りにまき散らされる危険性があるため、アポトーシス過程はできる限り周りを巻き込まないよう細胞死を誘導してこっそり死ぬように出来ている。これはガンに対する免疫を誘導する観点からはマイナスに働く。一方、場合によっては周りを巻き込みながら大騒ぎして起こる細胞死もある。この一つがフェロプトーシスで、ガンの周りに集まってきた白血球もフェロプトーシス型で死ぬことで、さらに白血球を呼び集めることが行われる。このように、ガン免疫という観点ではガン細胞のフェロプトーシスを誘導する治療法は理想的だが、現在得られるフェロプトーシス抑制因子 GPX4 を標的とする化合物は、ガンだけでなく白血球や腎臓など様々な細胞のフェロプトーシスを誘導するため利用が難しい。
この研究では膵臓ガン細胞特異的に GPX4 を抑制しフェロプトーシスを誘導する化合物を探索した。GPX4 が多くの細胞に発現していることを考えると、この不可能に挑戦したこと自体が立派だ。しかもうまい具合に N6F11 と名付けた化合物が見つかった。
この化合物は GPX4 に直接働くのではなく、ユビキチンリガーゼの一つ TRIM25 に働くことで GPX4 のユビキチン化、続く分解が誘導されることでフェロプトーシスが起こることを明らかにした。TRIM25 は低いレベルで多くの細胞に発現しているが、ガンでは発現が高く膵臓ガンでは発現は悪性度と相関している。
実際腫瘍を移植したマウスで投与実験を行うと、ガンの増殖を抑えることが出来、ガンではフェロプトーシスが起こっていることを確認できるが、浸潤している白血球を含め他の細胞ではフェロプトーシスを誘導できない。
重要なのは、ガンの抑制が完全にT細胞と死んだガン細胞から分泌された炎症分子に依存していることで、この治療をガン免疫を誘導するために利用できる可能性を示唆している。
このようにガン細胞特異的なユビキチンリガーゼを利用してGPX4を分解することが可能だとわかると、今後多くの製薬会社でより効率の高いリガンドが開発できる可能性がある。個人的には極めて有望な方法で、これまで免疫治療の対象になりにくかった膵臓ガンも対象に出来る。是非多くの会社で競争して追求して欲しい。
もう一つのイタリア・ミラノ、サンラファエロ研究所からの論文は IL1β とプロスタグランジンE2が膵臓ガンの治療標的になる可能性を示した研究で、11月1日 Nature にオンライン掲載された。タイトルは「IL-1β + macrophages fuel pathogenic inflammation in pancreatic cancer( IL1β陽性マクロファージが膵臓ガンの病的炎症をたきつける)」だ。
元々膵臓ガン周囲には炎症像が見られるので、この論文ではマクロファージに絞って調べ、膵臓ガン周囲のマクロファージが IL1β を発現していることに気づく。IL1β は自然炎症の主役だし、膵臓ガン周囲には炎症が見られるので特に意外性はないが、膵臓ガン周囲マクロファージで IL1β が誘導される仕組みを探った結果、以下のシナリオが明らかになっている。
膵臓ガンとマクロファージは、膵臓ガンが強く発現しているプロスタグランジン E2(PGE2) と TNF により刺激され、IL1β を発現、またこの IL1β は膵臓ガンの周りに炎症を強めるだけでなく、腫瘍にも直接働きかけて炎症細胞のリクルートメントに関わり、このサイクルが回ることで膵臓ガンがより悪性化する。
以上の結果は、PGE2 と IL1β 経路をブロックすることで、膵臓ガンとマクロファージの相互増強回路を止める可能性があることを示しており、実際 COX2 がノックアウトされたガン細胞を移植すると増殖は低下するし、IL1β に対する抗体でガンの増殖が抑えられることも示している。また、Cox2 阻害剤でもある程度腫瘍の増殖が抑えられることも示している。
以上が主な結果で、最初の論文と比べると驚くほどではないが、しかしすぐに治験を行う可能性がある発見なので是非可能性を確かめて欲しいと思う。
2023年11月6日
脳内に電極を留置して深部を刺激する方法がパーキンソン病などいくつかの疾患で広く使われるようになり、一定の周波数で脳を刺激することで、神経の興奮を同調させたり、可塑性を高める機能的な治療が、健常人も含めた広い対象に使える可能性が示されている。しかし、手術して電極を挿入するという方法は、健常人に使うことは、将来は別として、当分は許されない。
このため、特定の領域を頭蓋の外から刺激する方法の開発が続けられており、その一つが TMS と呼ばれる磁場を使う方法だ。ただ、この方法は装置も大がかりで、手軽な治療になるには時間がかかる。
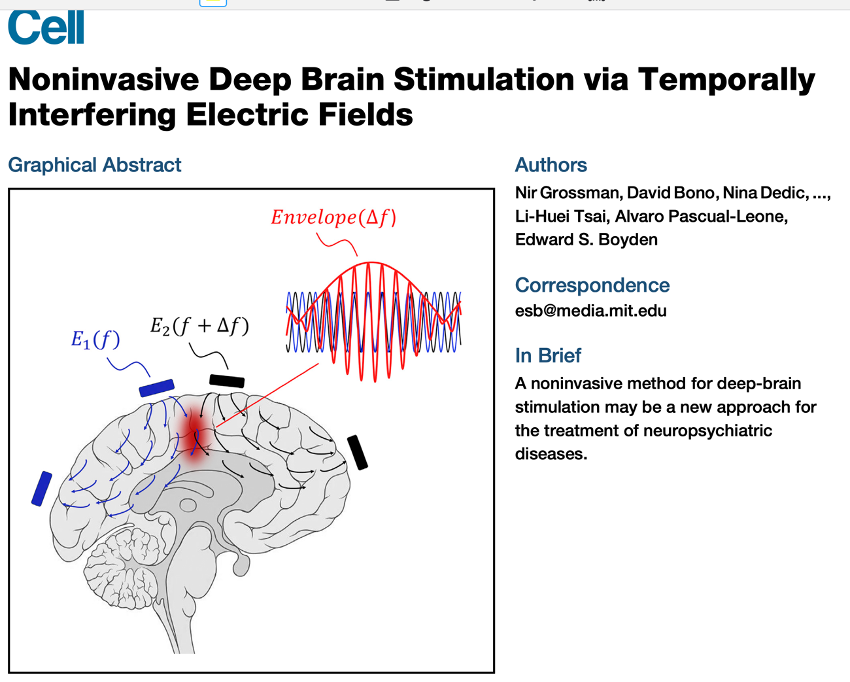
これに対し2017年 MIT のグループは、脳神経に影響のない高い周波数の電場を脳内に形成させる時、少しだけ周波数を変えておくと、両方の電場が重なるところで干渉が起きて、Envelope と呼ぶ低い周波数で大きい振幅(TMSのθバースト刺激に相当する)の刺激を局所的に発生させらることを明らかにした。
それからすでに6年が経過したが、ようやくこの方法を海馬及び線条体に対する深部刺激として使えることを示した論文が11月号の Nature Neuroscience に2報掲載された。
最初の論文は2017年の筆頭著者の研究室、英国サリー大学からで、この方法を海馬刺激に用いると、記憶の呼び起こしの正確度が増すことを示した。タイトルは「Non-invasive temporal interference electrical stimulation of the human hippocampus(非侵襲的時間干渉電気刺激を用いた人海馬の刺激)」だ。
この研究では死体脳を用いて、時間干渉電気刺激(TIS)で海馬だけにθ波を発生させられるか調べている。その上で、電場の量を調整することで、海馬全体、及び主に前方にθ波を局在させられることを確認している。
その上で、覚えた人の顔を思い出す課題を刺激下で行わせ、海馬前方を刺激すると、大きくはないが正確度が高まることが示された。この時、同時に機能的MRI (fMRI) を行うと、意外なことに刺激した方が脳血流が低下することが明らかになった。メカニズムは完全にわかっているわけではないが、θ刺激で同じようの結果が見られるので、おそらく思い出す時の反応が落ち着くことで、記憶の正確度が上がるのだろうと考えている。
もう一つはスイス・ローザンヌ EPFL からの論文で、運動学習の際に線条体を TIS で刺激する効果を調べており、タイトルは「Noninvasive theta-burst stimulation of the human striatum enhances striatal activity and motor skill learning(人間の線条体の非侵襲的θバースト刺激は線条体の活動と運動スキル学習を高める)」だ。
この研究では刺激の効果をまず線条体の脳血流量を fMRI で調べて確かめている。海馬と異なり、刺激により線条体の血流量は高まる。重要なのは、学習に使っている場所だけでこの現象が見られることで、利き手とは逆の指でボタンを押す操作に関わる右の線条体のみ、TIS の効果が現れる。そして、学習によるボタンを押す正確度は改善する。
すなわち、学習に使う領域の同調性を高めることで、シナプスの可塑性が高められていることがわかる。
この研究のハイライトは、同じ実験を高齢者と若者で行って、高齢者ほど TIS の効果が高いことを示している点で、おそらく神経結合性を高める効果が高齢者ではよりはっきり見えるのだろう。
以上、詳細は全て省いているが、簡単な非侵襲的刺激法の開発は、深部刺激研究の裾野を大きく拡げると考えられる。勿論個々の脳の形態から刺激法を計算する安全な方法の開発が必須だが、おそらく規制が必要になるぐらい様々な目的で利用されるようになるのではと思っている。それがいいのか悪いのか、今のところ予想できない。
2023年11月5日
行動時の脳活動を記録するエンコーダーと活動から行動を予測するデコーダーが開発されて、脳科学に回路学とは異なる研究領域が生まれた。その典型がオキーフとモザー夫妻のノーベル賞で、動物が認識している場所に対応する場所細胞や場所の空間的位置に対応する格子細胞の発見で、特に格子細胞は記録した活動をもう一度デコードしたとき脳内に格子が現れることでわかる。
ただこれまでのエンコード/デコード実験は行動と全く切り離した状況、すなわちイマジネーションの世界で行われたわけではない。というのも、実験動物が何をイマジネーションしているか問いただすわけにはいかず、結局行動から判断するしかなかった。一方我々人間は、昨日通った道を頭の中で再現することが出来るのは明らかで、動物でも同じようなイマジネーションの世界があるはずだ。
そんな中で、夢の研究から覚醒中に経験した神経刺激パターンが睡眠中に再現されていることが実験動物でも明らかにされた。これは行動と切り離されているのだが、意志に従って想像しているわけではない。面白いのは、以前紹介したように(https://aasj.jp/news/watch/20414 )、マウスが覚醒時の経験をもう一度夢で再現しているときは、目の動きとして行動にも表れることだ。この行動から、マウスが何を夢見ているのか読み解けることがわかった。
今日紹介するハーバード大学からの論文は、エンコード/デコード実験をさらに進めて、ラットの覚醒時に、イマジネーションの中だけで自分が移動したり、物を目的の場所に移動させたり出来るかを調べた研究で、11月3日 Science に掲載された。タイトルは「Volitional activation of remote place representations with a hippocampal brain–machine interface(離れた場所に対応する神経表象を海馬とコンピュータの間のbrain-machineインターフェースを用いて活性化する)」だ。研究の内容をGPT-4にインプットして出来た漫画も掲載しておくが、残念ながら理解の足しにはならないので文章を読んで欲しい。
研究は海馬を128チャンネルの電極でカバーし、その活動を25ヘルツの頻度で記録し、また刺激できる様にしている。このラットを、ボール型のトレッドミルで走らせ、トレッドミルに連動したプレーグラウンドという外界イメージに基づいて、海馬に場所細胞を形成させる。次に目的を定めて同じ外界を走らせると、海馬の場所細胞が対応する場所に応じて興奮しながらゴールにたどり着くパターンをデコードすることが出来る。
これを確かめた後、今度はプレーグラウンドからの情報が全く入らない、すなわち周囲は白紙のトレッドミルにラットを置いて、これまでのデータからデコーダーが特定した場所情報(ゴール)を海馬に刺激としてラットにインプットしたとき、ラットが頭の中で示されたゴールに到達するかを調べている。勿論イメージの中でのゴールに到達するとご褒美がもらえる。
結果は期待通りで、頭の中で示されたゴールに、そこに至る場所細胞を順番に活動させながら到達する。面白いことに、最初はイメージに合わせて足も動いていたが、慣れてくると全く動かないで頭の中だけでゴールに到達して褒美をもらえるようになる。すなわち楽をして完全にイメージの中だけで遊んでいる。
ラットもイメージの中で行動できることが確認された瞬間だ。さらに実験を進めて、今度はラットの場所を固定して、特定の場所細胞を刺激することで、イメージ上でラットのいる場所から少し離れた場所に対象物、そして他の場所をゴールとして示し、対象をゴールに運ぶ道筋をイメージさせている。自分が動くことをイメージするのと比べると、精度は少し落ちるが、それでも離れた場所から離れた場所への移動をイメージしていることが、順々にゴールに向けて場所細胞が活動することからわかる。言ってみれば、ラットも完全に頭の中だけでゲームで遊ぶことが出来る。
これらの実験は、夢実験と異なり、ご褒美を当てにして、意志を持って脳の活動を自分で調整出来たことを示している。これが、場所細胞を一定のベクトルに従って順々に活動させることで行われることも確認している。
結果は以上で、脳全体の道具化を目指す人工知能研究が、今やbrain-machineインターフェース研究として実際の脳を巻き込んで研究を加速させていることがわかる。恐ろしいと思う人もいるかも知れないが、私のような老人は毎日新しい世界を経験できる今を楽しんでいる。
2023年11月4日
胸腺トレランスは1950年代から、自己と非自己を区別する免疫学の重要なドグマとして多くの研究者を魅了し続けてきたが、昨年6月(https://aasj.jp/news/watch/19920 )及び今年9月(https://aasj.jp/news/watch/22849 )に紹介したように、自己抗原を胸腺内で提示する仕組みについては全く新しい進展を見た。ただ、この新しい進展も自己反応性のT細胞は胸腺内で細胞死が誘導され除去されるというドグマはそのまま継承している。というのもこのドグマについてはトランスジェニックマウスを駆使して行われた von Boehmer 達の見事な論文があるからだ。
ただ、ドグマもよく調べてみると例外が見つかることが多い。今日紹介する米国国立衛生研究所からの論文は、CD8T細胞の少なくとも一部は胸腺内で細胞死せず、未熟な内に末梢へ移行し、そこで一部は疲弊し、一部は抑制性T細胞へと分化することを示した研究で、11月3日号の Science に掲載された。タイトルは「CD8 T cell tolerance results from eviction of immature autoreactive cells from the thymus(CD8T細胞のトレランスは未熟自己反応性T細胞を胸腺から排出することで達成される)」だ。
以前から自己反応性CD4T細胞は胸腺内で完全に除去されることが確認されているが、自己反応性のCD8T細胞は末梢に一部流れているという指摘があった。すなわち、胸腺内での除去が完全でない可能性が高い。そこで、Y染色体上に存在するオスだけで発現する自己抗原に対するT細胞の反応を調べると、胸腺で確かにY抗原に対して反応する細胞は存在するが、PD-1を強く発現して刺激を緩和しており、その結果細胞死に必要なカスパーゼの活性化がほとんど見られないことを発見する。逆にクラスII 抗原に対するT細胞はPD-1をほとんど発現していない。
以上の結果からクラス1+自己抗原に対する細胞のかなりの部分が胸腺内で除去されていないと確信をもち、反応性のT細胞の抗原受容体もY抗原特異的なモデルマウスを駆使し、胸腺内で細胞除去が出来ないとしたら、どのようにトレランスが維持されているのかを調べている。膨大な結果なので、詳細を省いて結論だけを箇条書きにする。
クラス1+Y抗原で刺激された未熟T細胞(CD4/CD8陽性)は胸腺内で自己抗原の刺激を受けるが、除去される前に胸腺外に排出される。
この排出には通常成熟した細胞が胸腺から末梢に移行するときに利用するスフィンゴシン受容体S1P1 が関わっており、T細胞で SIP1 がノックアウトされると、未熟CD4/8T細胞は胸腺にとどまり、そのままCD8細胞へ分化する。残った細胞はしかし完全に除去されることなく、胸腺内でインターフェロンを発現し炎症を起こす。すなわち、CD8T細胞は早く胸腺から排出されるから細胞死へと向かわないのではなく、PD-1の発現などからみてもともと除去されにくいと考えられる。そう考えると、除去ではなく胸腺から排出することが、CD8T細胞トレランスには重要な経路であることがわかる。
さらに、CD4とCD8の胸腺を離れる時期の違いについて、S1P1発現調節に関わる転写因子FOXO1の発現が成熟CD4T細胞では抗原刺激が低下してから誘導されるのに対し、未熟T細胞では強い抗原刺激を受けたときに誘導されると説明している。
では、末梢に排出された自己反応性未熟CD8T細胞の運命はどうなるのか。まず胸腺を離れたばかりのT細胞をラベルし、CD4/CD8陽性細胞はCD8細胞へと分化するが、末梢CD8T細胞ではほとんど自己反応性が認められないことから、トレランスが成立していることを明らかにする。
そして、このトレランスは、末梢で出会った自己抗原により一部は細胞死で除去される可能性は残るが、多くはCD8特異的抑制性T細胞、すなわちCD8Tregへと分化することで、トレランスを維持することを示している。
結果は以上で、CD8T細胞では最初から末梢でのTregを誘導する仕組みが組み込まれたトレランス維持が行われていることが見事に証明された。これは、CD8T細胞によるガン免疫や自己免疫を考える上でも重要な発見だと思う。
2023年11月3日
ブドウ糖の吸収と排泄は糖代謝のファーストステップで、主に2種類のトランスポーターにより調節されている。一つは SGLT1/2 で sodium/glucose-cotransporter で、ナトリウムの勾配を利用して細胞内にブドウ糖を取り込む。もう一つは4種類存在する GLUT で、濃度差に応じてブドウ糖を出し入れする。例えば腎臓の近位尿細管では、取り込みに SGLIT2、細胞外への排出に同じ GLUT2 が用いられているが、GLUT2 が欠損すると細胞内のブドウ糖が上昇し、グリコーゲンが蓄積、尿細管機能不全症に陥る。これが Fanconi-Bickel 症候群(FBS)で、尿細管と肝臓のグリコーゲン蓄積症として知られている。一方、小腸上皮でも細胞外のブドウ糖を主に SGLT1 を使って取り込み、それを GLUT2 を通して細胞外へ移行させることでブドウ糖を取り込んでいるが、GLRT2 をノックアウトしても、リン酸化ブドウ糖を小胞体内で再処理して、細胞外へと運ぶ仕組みがあり、大きな異常は発生しない。当然ブドウ糖の調節が重要な筋肉では、GLUT1 と GLUT4 が働いており、FBS では異常は起こらない。
今日紹介するイタリア・ナポリにあるカンパニア大学からの論文は、GLUT2 を近位尿細管細胞(PT)で欠損させた、FBSモデルマウスを作成し、この症状を現在糖尿病薬として広く使われている SGLT2阻害剤で治療できることを示した研究で、11月1日号 Science Translational Medicine に掲載された。タイトルは「The SGLT2 inhibitor dapagliflozin improves kidney function in glycogen storage disease XI(SGLT2阻害剤Dapaglifozin は11型グリコーゲン蓄積症の腎機能を改善する)」だ。
GLUT2 が全身で欠損する FBS は、低血糖だけでなく、アシドーシス、低カリウム症、低リン血症とそれによるくる病、そしてグリコーゲン蓄積による肝臓肥大と尿細管機能不全が起こる。
マウスで GLUT2 を PT だけで欠損させると、肝肥大以外のほとんどの症状を再現することが出来、アシドーシス、低カリウム症、低リン血症、そしてくる病の全ては尿細管機能不全に依ることがわかる。
また試験管内の実験で、GLUT2欠損PT ではグリコーゲンの蓄積の結果、オートファジーの機能不全が生じ、PT の変性を誘導していることも明らかになった。
GLUT2欠損で PT は SGLIT2 の発現量を低下させ、細胞内へのブドウ糖の取り込みを抑えるが、効果は限られている。そこで、現在糖尿病治療の重要な薬剤として広く用いられるようになった SGLIT2阻害剤Dapagliflozin をマウスに投与して、症状の改善が見られるか調べている。
結果は予想通りで、カリウム、リン、プロトンなど全てのイオンバランス障害は見事に改善し、これに対応して PT でのグリコーゲン蓄積も低下することが明らかになった。
この前臨床研究の結果を見て、一人の患者さんに Dapagliflozin投与を行うと、カリウムやリンの血中濃度が上昇し、尿に排出される尿細管のグリコーゲン量が低下し、またリン再吸収トランスポーターの発現量が上昇することを確認している。
以上が結果で、予測可能で驚くほどの話ではないが、前臨床を経て治療法を確立できたことはFBSの患者さんには朗報だ。それと同時に、今慢性腎疾患の特効薬として最も注目されている SGLT2阻害剤や、尿細管でのグルコーストランスポートを勉強し直すには最適の論文だと思う。
2023年11月2日
チェックポイント治療(IC)は、抗原刺激が続くことで起こるT細胞の持続的活性化を抑えるフィードバック機構を抑制することで、過活性をあえて誘導し、ガンに対する免疫反応を持続させる治療だ。これがガンに効くことは明らかだが、治療自体に特異性がないため、他の免疫も活性化してしまい、多くの自己免疫反応を副作用として誘発することが知られている。幸い、多くの経験に基づいて、自己免疫反応を抑える治療法も開発され、使用が始まった当初と比べるとコントロールできるようになっている。
IC が原因の自己免疫反応の中で最もやっかいなのが、αミオシンを主な標的にする自己免疫性心筋炎で、発症すると3割以上の致死率という恐ろしい副作用だ。また、心筋炎が発症する患者さんでは、呼吸に関わる筋肉炎も併発し、重症筋無力症のような症状が現れる。
現在重症筋無力症に胸腺摘出が行われているのか把握していないが、私が臨床に関わっていた時代は胸腺摘出が行われていた。すなわち、胸腺でのトレランスの異常が背景にあると考えられていた。
ここまでは私でも連想できるが、今日紹介するフランス・ソルボンヌ大学からの論文は、さらに連想を拡大して、胸腺上皮腫瘍(TET)の患者さんに IC が使われることに気づいた。そして、TET に対する ICが心筋炎発症リスクが極めて高いことを明らかにした研究で、10月26日 Nature Medicine にオンライン掲載された。タイトルは「Thymus alterations and susceptibility to immune checkpoint inhibitor myocarditis(胸腺の変化とチェックポイント治療による心筋炎の感受性)」だ。
様々なデータベースを用いて、TET への IC と一般腫瘍への IC を比較し、一般腫瘍 IC 治療での心筋炎発症率が1%に対し、TET 患者さんが心筋炎を発症する率が16%に達することをまず確認し、これをソルボンヌの関連病院などの症例でさらに確認している。
そして、TET患者さんの IC治療では、心筋炎の症状も強く、重症筋無力症と同じレベルに発展すること、さらに治療後すぐに副作用が発生することを明らかにしている。
以上の結果は、重症筋無力症のような筋肉を標的にする自己免疫疾患には胸腺異常が潜んでいることを示している。そこで、一般腫瘍の IC で心筋炎を発症したケースについて、CTでの胸腺像を比較し、心筋炎を発症した人の15%が治療前に胸腺肥大が見られたことを明らかにしている。実際にはレントゲン形態的な詳しい検討が行われ、TET になる手前のグレード3の胸腺像が見られることを明らかにしている。
次に胸腺異常を末梢血で調べられるかにもチャレンジしている。まず、重症筋無力症で上昇するアセチルコリン受容体への自己抗体が当然上昇している。さらに、TcR の再構成で発生する環状DNAを指標に胸腺からのアウトプットが明らかに低下していることを明らかにした。
結果は以上で、心筋炎、重症筋無力症、胸腺、胸腺上皮腫と連想を続け、そこから胸腺異常と心筋炎のリスクを突き止めた、まさに臨床の気づきの研究と言える。
研究はここまでだが、結果は様々な免疫学的連想を生む。例えば最近紹介している胸腺動物園との関係は?あるいは、昔、胸腺リンパ体質と言われた体質との関係は?臨床研究はこのように連想が連想を呼ぶ。
2023年11月1日
私が在籍していた頃、京大では、医学部や理学部の教室が集まって研究発表会をしていた。当時の私にとっては、専門以外の現象を直接学ぶ素晴らしい機会だったが、中でも中西先生が話された網膜のガングリオン細胞の研究は、精緻な神経回路の合目的性に感心した記憶がある。
今日紹介するカリフォルニア大学バークレー校からの論文は、様々な動物で研究されてきた中枢機能とは別に、網膜自体に備わる対象の動きを追跡する神経回路が、サルにも存在し機能していることを明らかにした研究で、10月25日 Nature にオンライン掲載された。タイトルは「An ON-type direction-selective ganglion cell in primate retina(霊長類のオン型方向特異的神経節細胞)」だ。
網膜の視細胞は双極細胞により内部の神経節へシグナルが伝達されるが、中枢で統合されるまでに、網膜内で光のオン、オフを感知して対象を追いかける特殊な神経節システムが存在し、詳しく研究されている。両眼視が発達する前でも赤ちゃんは対象を追いかけるので、人間を含む霊長類も当然網膜内で動きの方向性を感知する仕組みがあると思っていたが、実際にはこの機能を担う細胞が特定されていたわけではないことがこの論文を読んでわかった。それほど高等動物を使った研究が難しいと言うことだ。
この研究ではこれまで蓄積されたサル網膜細胞の single cell RNA sequence データを元に、神経節細胞の種類を調べ直し、全部で18種類に分けられる神経節細胞の中から、他の動物についての研究でわかっている性質に最も近い神経節細胞をまず特定している。
ただ、遺伝子発現でオン型方向特異的細胞と言うだけでは証明にならない。この研究のハイライトは、サル網膜を取り出して、試験管内で異なる方向を持った動きに対する反応を調べ、特定した細胞がこの機能を担っていることを証明したことだ。サルの網膜を自由に調整できないことを考えると、大変な苦労があったと思われる実験で、これにより初めて霊長類のオン型方向特異的神経節細胞が特定されたと結論できる。
後は同じ網膜の培養を用いて、オン型神経節が上の層のオン型アマクリン細胞とシナプス結合を形成し、GABA作動性シナプス阻害によりこの結合を遮断すると、動きに対する反応が消失することを示している。
結果は以上で、大変な苦労をしてサルでも他の動物と同じような網膜内の方向性感知システムがあることを証明したのがこの研究で、高等動物での研究の苦労がよくわかる論文だった。その上で、人間網膜の single cell RNA sequencing データ解析と組織学から、ほぼ同じ仕組みが人間にも備わっていることを示している。このように人間にも当てはまる、方向性の追跡に必要な網膜内の細胞と回路の遺伝子発現プロファイルがわかることで、おそらくニスタグムス(眼振)を伴う遺伝性疾患のメカニズム解析が進むのではと期待できる。
2023年10月31日
以前も話したように、私が患者さんを見ていた1973年から1980年の時期には、外来で結核患者さんを見るのは普通のことで、また保健所の胸部X線検査の読影も結核を念頭に置いて見ていたが、この時代、結核にかかりやすい人、あるいはかかると重症化しやすい人、といった遺伝的背景を考えたことは全くなかった。しかし、20世紀後半から、ほとんどの病気について多型研究が進むことで、病気の理解は一段と深まってきた。すなわち、病気の分子メカニズムを、責任遺伝子と関連させて説明できるようになってきた。実際、コロナパンデミックでも、感染や重症化に関わるコモンバリアントだけでなく、希ではあるが病気のコースを決めてしまうレアバリアントも続々明らかにされた。
今日紹介するフランスのネッカー研究所、Inserum、そして米国ロックフェラー研究所からの論文は、ほとんどの微生物に対して抵抗力は維持しているにも関わらず、結核など抗酸菌感染特異的に重症化する突然変異の研究で、10月23日 Cell にオンライン掲載された。タイトルは「Human MCTS1-dependent translation of JAK2 is essential for IFN-g immunity to mycobacteria(MCTS1依存性のJAK2分子の翻訳がインターフェロンγ が媒介する抗酸菌への人間の免疫反応に関わる)」だ。
BCG は生菌ワクチンで結核予防のためまだ利用されている国もある。このような国では、摂取後 BCG が全身に広がり時には命に関わる抗酸菌症を起こす、比較的男性に多い遺伝的抗酸菌高感受性(MSMD)が希ではあるが発見され、遺伝疾患として認識されている。この研究では、様々な国で発見された MSMD 家族を集め、まずエクソーム解析で共通の変異を探し、最終的にX染色体上にある MCTS1遺伝子が変異により、機能できなくなっていることを発見する。
MCTS1 は、あらゆる細胞に発現しており、DENR と結合してリボゾームと脱アシル化された tRNA を外して、リボゾームを再利用したり、あるいは翻訳を再開するのに機能している分子で、この変異が抗酸菌に対する抵抗性だけに関わるというのは全く予想外の結果と言える。
そこで、なぜこのようなあらゆる細胞で機能しているメカニズムが特殊な症状につながるのかを徹底的に追求している。
長い話なので結論だけをまとめると以下のようになる。
MCTS1 の相手方の DENR が欠損するとマウスは生まれてこないが、MCTS1 は他の分子で代償可能で、欠損しても正常に生まれてくるし、驚くことに抗酸菌以外の微生物への抵抗性は全く傷害されていない。しかし細胞レベルで調べると、翻訳再開などの効率が低下する結果、蛋白質の合成効率は多くの分子で低下する。ただ、これも量的問題で、結局一番大きく MCTS1 に依存していたのが、様々なサイトカインシグナルを伝える JAK2 であることが明らかになった。
ただこれだけでは説明にならない。というのもJAK2 は様々なシグナルの下流で働いている。また、この変異では JAK2 の低下も完全ではなく、大体正常の 1/3 ぐらいに低下する。この条件でシグナルが強く抑制される経路を探していくと、なんと Vδ2陽性 γδT細胞と、Vα7.2遺伝子を発現する MAIT細胞の IL23への反応が強く抑制されていることを発見する。
実際には一歩一歩犯人捜しをした結果なのだが、結論としては JAK2 への依存性が細胞やサイトカインごとに異なる結果、このような特殊な欠損が発生してしまったことになる。そして、結核菌が侵入したとき、マクロファージから分泌される IL23 に反応するこの極めて限られた経路から作られるインターフェロンγ が欠損し、抗酸菌による重症の感染症を発症するというシナリオだ。
なぜ抗酸菌感染に対して、この細い経路を利用するようになったのかは極めて面白い謎だ。昔、結核患者さんを見ながら、面白い病気だといろいろ考えたが、それを遙かに超える人間と細菌の関係が拡がっていることがよくわかった。