2021年11月18日
私たちの脳の神経回路形成には、特異的なシナプス形成制御が必須で、特に間違った神経同士でシナプスが形成されないように調節が行われる。例えばニューロリギンやそのリガンドニューレキシンなどはシナプス形成のオーガナイザーとして有名だが、ノックアウトマウスの解析から、このような単純な図式はもはや受け入れられない。もう一つ重要なオーガナイザーがRTN4RのようなRNoGoシグナルに関わる分子で、神経の軸索伸展を抑制して正しい神経結合に必須と考えられている。逆に、脊髄損傷研究分野では、このNoGoシグナルを外して軸索を再生させられないか研究が行われてきた。
今日紹介するスタンフォード大学からの論文は、極めてオーソドックスな実験研究を重ねて、NoGoシグナル受容体RTN4RがBAI-Adhesion GPCRと結合し、軸索伸展、樹状突起、を抑制しつつ、シナプス形成に関わることを明らかにした、この分野では重要な研究で 11月24日号のCellに掲載された。タイトルは「RTN4/NoGo-receptor binding to BAI adhesionGPCRs regulates neuronal development(RTN4/NoGo受容体はBAI adhesion GPCRと結合して神経発生を調節している)」だ。
この研究は、これまでシナプス形成に関わることが知られているBAI-adhesion GPCR(BAI)と結合する相手側の分子の探索から始まっている。極めてオーソドックスな方法でBAI結合分子を特定すると、なんとNoGo受容体RTN4Rと同じファミリーのRTN4RL1が結合分子トップにリストされてきた。これは驚きで、RTN4Rはこれまで全く異なる分子と結合して働いているとされてきた。
そこで、BAIとRTN4RおよびRTN4RL1の結合を生化学的、細胞学的に検討し、
BAIとRTN4Rがナノモルレベルの親和性で結合する。 RTN4RはBAIのTSR3領域と結合するが、結合面にフコース、マンノースの糖鎖修飾が必要 を明らかにし、この2つの分子がセットで、NoGoシグナルを担っている可能性を確認している。
次に、RTN4R遺伝子をノックアウトしたヒトES細胞から神経を誘導、試験管内での神経間相互作用を調べる実験から、電気生理学的にも、細胞学的にも、RTN4RとBAI結合がシナプス形成に必須であることを証明している。
最後に、神経細胞やグリア細胞ごとにBAI発現を調節する実験系を用いて、
グリア細胞のBAIと神経細胞のRTN4Rとの相互作用により、神経軸索の伸展が抑制される。 神経細胞が発現するBAIにより相手神経細胞の樹状突起形成が抑制される。 ことを明らかにしている。
この結果をまとめると、BAIとRTN4Rは、神経伸展を抑制し、次に樹状突起形成を抑えることで、神経を限られた特定の神経に誘導し、特異的なシナプス形成を促すオーガナイザーの働きをしていることが明らかになった。
遺伝子がクローニングされ、ノックアウト動物が作成されても、詳しいメカニズムを解明するためには、地道なオーソドックスな努力の必要性を教えてくれる重要な研究だと思う。
2021年11月17日
新型コロナウイルスについては、ウイルス自体だけでなく、ウイルスの作用を通して様々な生命現象を学ぶことができた。たった30Kbの小さなしかし精巧なゲノムに実に多様な作用がコードされている。
今日紹介するドイツ・リューベック大学からの論文は、ウイルスゲノムが細胞内で働くために最初に必要とされる、メインプロテアーゼ(Mpro)が、NFkbシグナル経路のスキャフォールドとして機能しているNEMOを直接分解して血管炎を誘導する可能性を示した研究で、10月21日号Nature Neuroscienceに掲載された。タイトルは「The SARS-CoV-2 main protease M pro causes microvascular brain pathology by cleaving NEMO in brain endothelial cells(SARS-CoV2のメインプロテアーゼは脳血管のNEMOを分解して脳の微小血管病変を誘導する)」だ。
この研究は、なぜcovid-19で脳症状が発生するのかの原因を突き止めたいと始められたようだが、分析的なアプローチをとるのではなく、血管内皮のNFkBシグナル活性化に必須のスキャフォールドNEMOがMproにより破壊されて病気が起こるという仮説を最初から設定して、この仮説を確かめるための実験を行っている。
神経細胞に直接新型コロナウイルス(CoV2)が感染する可能性を示唆する人もいるが、血管炎がウイルス感染により起こることを示すため、covid-19患者さんでは脳血管の細胞死が高まっていること、またマウスへの感染実験でも、再現できることを示し、血管内皮が脳病変の場になる可能性を示している。
次に、患者さんの脳血管、および試験管内でCoV2を感染させた細胞では、NEMOが分解されていること、また感染細胞では5カ所のグルタミンサイトで切断が起こっていることを確認している。
この結果、NFkBシグナルが抑制されると予測されるが、期待通りMproを発現している血管内皮では、NFkB下流のIL1βの発現が低下している。また、NFkBはカスパーゼシグナルを押さえる役割を持っているが、これが破壊されているため、TNFなどによる細胞死が強く促進されていることを示している。すなわち、脳血管内皮の細胞死は、ウイルスのMproによるNEMO破壊の結果である可能性が支持された。
そこで最後に、生体内でこの回路が働いているか確認するため、まずアデノ随伴ウイルスでMproを脳血管に導入すると、微小血管の内皮の細胞死が誘導された。また、最初からNEMOが血管内皮で欠損したマウスを調べると、同じような血管病変が起こることを確認している。また、このNEMO欠損による細胞死シグナルにはRIPK1/3シグナルが関わることを突き止め、RIPK1阻害剤で血管病変を抑えられることを示している。
結果は以上で、ホストの脳血管病変を誘導するほうがウイルス進化にとって都合が良かったとはまず思えないが、偶然にしても面白い結果だ、というのも、この結果が正しく、しかも後遺症の原因にもなる脳血管異常にMpro活性が効いているとすると、現在認可を待っているファイザーや塩野義のMpro阻害剤が、ウイルス増殖抑制だけでなく、血管病変抑制にも効く可能性が出てきたことになる。感染初期だけでなく、できれば、血管炎が発症したケースにも試してみたら面白いかもしれない。
2021年11月16日
レビー小体認知症(LBD)やパーキンソン病(PD)で神経変性の引き金を引くのは、αシヌクレインの蓄積であることはこれまで何度も紹介してきたが、これに加えて多くの神経変性疾患では、免疫性の炎症が起こっていることが示唆されている。
今日紹介するシカゴ、ノースウェスタン大学からの論文は、ここからさらに進んで、これらのシヌクレイン症では、シヌクレイン自体に対する特異的T細胞が関わっている可能性を示した研究で、11月12日号Scienceに掲載された。タイトルは「CD4 + T cells contribute to neurodegeneration in Lewy body dementia(CD4陽性T 細胞がレビー小体認知症の神経変性に貢献している)」だ。
この研究は全て患者さんの脳組織や脳脊髄液、末梢血を用いた仕事で、最終的に病因を実験的に確かめることはできない。従って、現象を積み重ねるスタイルの研究だ。
まず、亡くなった患者さんの黒質を免疫組織的に調べ、PDやLBDの患者さんでは、T 細胞の浸潤が何倍も多いこと、またこれらのT細胞はシヌクレインが沈殿したレビー小体と接して存在していることを確認している。
次に、正常およびPD、DLB患者さんの脳脊髄液から血液細胞を集め、single cell RNAseqを用いて脳に浸潤している血液細胞の遺伝子発現を調べると、他の細胞腫と比べて、CD4T細胞の転写が活性型に変化し、特にCXCR4やCD69の発現が高まっていることがわかる。一方、末梢血CD4T細胞のsingle cell RNAseqでは同じような変化は認められない。
CXCR4はT細胞浸潤を誘導する可能性があるので、黒質血管のCXCL12の発現、および脳脊髄液中のCXCL12を調べ。それぞれ上昇が見られることを示している。また、認知症の進行具合との相関も調べており、認知症の進行と弱い相関があることも確認しているが、示されたデータの差は大きくない。
この研究で最も大事なのは、患者さんのT細胞がシヌクレインに対して反応するかどうかだが、末梢血T細胞のシヌクレイン由来ペプチドに対する反応を調べると、
元々患者さんのT細胞は抗原なしでも活性が高い、 ペプチドプールに対して患者さんT細胞は増殖反応を示す。 患者さんにより異なるが、特に強い反応を示すペプチドが存在する。 刺激によりCXCR4が上昇するとともに、炎症性サイトカインIL-17が誘導される。 を示している。すなわち、シヌクレインに対するT細胞が、患者さん末梢血、そしておそらく脳内にも存在しており、炎症の原因になっている可能性を示唆している。
もし本当なら、現象としては恐ろしいことだが、逆にPDやLBDを、免疫抑制やケモカイン阻害により治療する手立てがあることも示している。そこまで研究が進めないと、論文のための論文で終わってしまう。
2021年11月15日
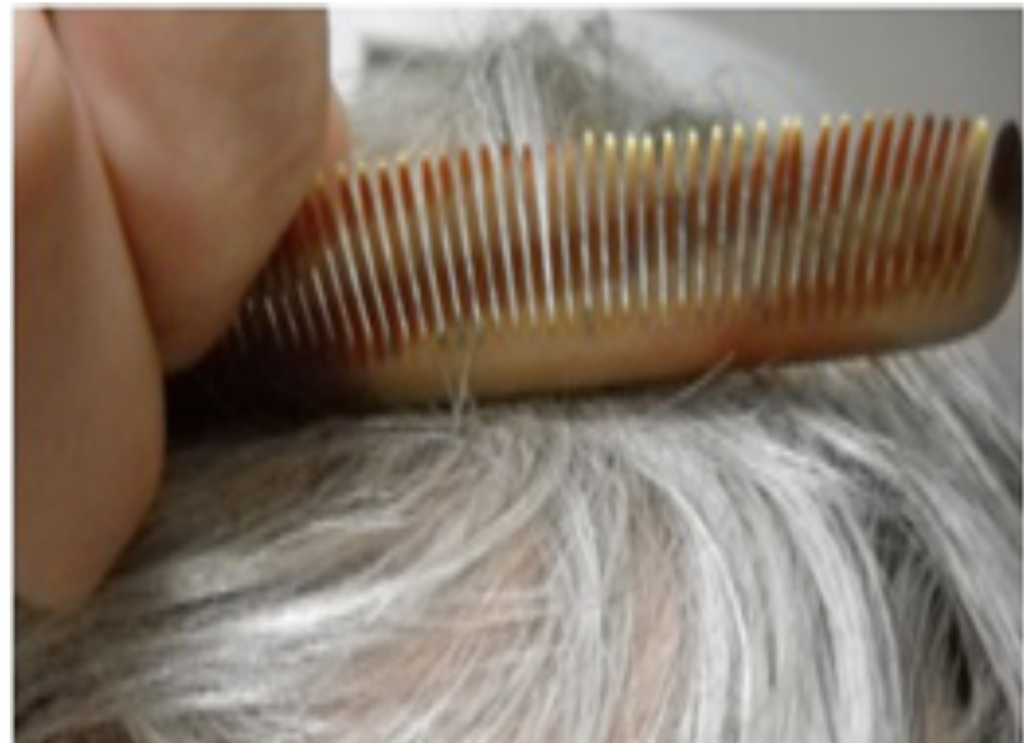
少し内容が古くなったかもしれないが、このHPに言語誕生についての研究をまとめた覚え書きを掲載している(https://aasj.jp/news/lifescience-current/10954 )。チョムスキーの最新研究から始めた後、言語を使うときの統語と、道具を使って仕事をするときの頭の中でのプランニングに関わる脳回路が共通している可能性についてもまとめておいた。この記事で、この可能性を示す証拠として挙げたのは、1)1年ぐらいでようやく意味のわかる単語の並びを話すようになるのと同じで、生後18ヶ月まで、道具とおもちゃの区別はできないこと。2)脳卒中で失語症が発症してしまう患者さんの中には、同時に道具の使い方がわからなくなる「失行症」を併発することがあること。の2点だった。
クシの使い方がわからなくなった失行症の患者さん(Wikipedia: https://en.wikipedia.org/wiki/Apraxia#/media/File:Apraxia_001.jpg) ただ、これらの研究は実際の脳回路特定までには至っていなかった。
今日紹介するフランス、リヨン神経科学研究センターからの論文は、機能MRI(fMRI)を用いて言語と道具使用の共通性に迫った面白い研究で、11月12日号Scienceに掲載された。タイトルは「Tool use and language share syntactic processes and neural patterns in the basal ganglia(道具使用と言語は統語プロセスと基底核の神経活動パターンを共有している)」だ。
この研究では、道具と言語について、2つの複雑な課題を設定している。まず言語だが、複雑な内容を単純な構文を組みあわせるだけ(CC)、主語の説明に関係代名詞を使う構文(SRC)、そして主語を目的格として説明するため関係代名詞を使う構文(ORC)を作っている。英語の例が出ているので引用すると「The writer admires the poet and writes the paper」(CC), 「The writer that admires poet writes the paper」(SRV)、「The writer that the poet admires writes the paper」(ORC)。これらの構文が正しく理解されるか調べると、少なくともフランス語の場合ORCが最も難しく、判断に時間がかかり、また失敗率も高い。
次に道具使用だが、長いピンセットを使ってボードに指してあるピンを抜いて、他の決められた場所に移動させるという課題を行っている。
この2種類の課題を行っているときに、機能的MRI(fMRI)で脳の活動を比べると、言語の統語を処理しているときと、道具を使うプランを構想しているときの基底核、特に淡蒼球の脳の活動パターンが類似していることを明らかにしている。さらに面白いことに、道具使用プランの際の脳活動と最も一致するのが、理解が難しいORC構文を処理しているときであることも示している。
普通の研究は、脳活動の共通性を特定できると、めでたしで終わるのだが、このグループの発想力はこれでとどまらない。もし同じ回路を使っているとしたら、道具を使う訓練によって、言葉の統語理解が高まる、あるいは逆もあるのではと、機能的実験を行っている。
ピンを決められたところに移すボードゲームを、ピンセットを使って、あるいは道具を使わず手を使って訓練し、先ほどのORC理解度を測定すると、期待通り、道具を使って訓練したときに最も言語構文の理解力が上がる。
また、ORC,SRCそれぞれの構文を何度も聞かせて、理解を早める訓練を行った後、道具を使ったピンを移すボードゲームを行わせると、ORCを理解するよう訓練したときのほうが、SRC理解の訓練より、ゲームのスコアが改善する。
結果は以上で、道具使用の構想過程と、言語の統語過程に同じ脳回路が利用されることを示しただけでなく、機能的にも両過程がオーバーラップしていることを示した、極めて面白い研究だと思う。
最後に一つだけ懸念するのは、私たちが道具を使うとき、言語能力に頼っている可能性がないかだ。ただ、この疑問はトートロジーになって答えるのが難しいので、気にしないでおく。
2021年11月14日
今年のノーベル医学生理学賞以来、心なしか痛みや体性感覚の論文が増えた気がするが、おそらくこれは違った目で論文を読むようになったからだろう。そんな目にとまったのが今日紹介するイスラエル工学研究所からの論文で、免疫反応を脳の島皮質神経が記憶するという話だ、タイトルは「Insular cortex neurons encode and retrieve specific immune responses(島皮質神経は免疫反応をエンコードしまたその記憶を読み出せる)」だ。
局所の炎症や免疫反応も体性感覚を誘導するから、脳に影響するのは当然で、何が面白いのかと読み始めた。ただ、イントロダクションを読むと、著者らは局所の免疫反応が脳神経に記憶され、この記憶がその後の炎症反応に影響するという大それた仮説を持っていることがわかった。
では、仮説をどう証明するかだが、興奮すると神経に一時的に発現するFos遺伝子を利用して、腸や腹腔での炎症時に興奮する神経をまず特定し、今度はFosを発現した同じ細胞を、これらの細胞だけ刺激したり、抑制したりすることができる、化学遺伝学的手法を用いて操作したとき、末梢で何が起こるかを調べる、という段取りで実験を行っている。
まず、腸に硫酸デキストランを投与して起こした炎症により興奮する神経を探すと、彼らが最初から狙っていた島皮質のグルタミン作動性錐体神経および一部のGABA作動性抑制神経がラベルされる。また、腸の神経をラベルして投射をたどると、炎症により興奮した細胞と一部オーバーラップするので、腸からの島皮質に神経投射があり、その結果神経興奮が見られることが確認されている。
ここまではなんの不思議もない。以前紹介したように炎症性サイトカインはTRPV を直接刺激することもあるから(https://aasj.jp/news/watch/18033 )、興奮した神経が島皮質に投射しておれば当然の結果だ。
ただここから先、すなわち島皮質で興奮した同じ神経を興奮させると、局所の免疫細胞や炎症細胞が変化するということは、想像だにしなかった。この研究では、Fosを発現した細胞だけが人工的リガンドで刺激できる受容体を発現するようにし、腸からの刺激に反応した島皮質神経をもう一度CNOと呼ばれる人工リガンドの注射で興奮させられるように操作したマウスを用いて、これを実現している。
驚くことに、腸の炎症により興奮した島皮質神経を再度興奮させると、今度は腸特異的にほぼ同じような炎症状態を誘導することができている。これは、自然免疫に関わる細胞だけでなく、γδT細胞や、CD4T細胞の浸潤も伴う、驚くべき再現だ。一方、島皮質神経をランダムに刺激しただけではこのような局所炎症の再現は全く見られない。また、同じ現象は、腹腔刺激でも誘導でき、この系で呼び起こされる炎症は、腹腔組織特異的で、どこで炎症が起こったのか、脳がしっかり区別していることがわかる。
そして最も驚くべき実験は、腸管の炎症を記憶した細胞の興奮を、抑制性のリガンドで今度は抑えると、硫酸デキストラン投与による炎症の程度を軽減することが可能であるという結果だ。
以上が結果で、例えばワクチン注射した炎症反応は脳でしっかり記憶され、また起こるのではと変に心配していると、副反応が持続し、さらに2回目の接種で反応が高まるといった話になる。鎮痛剤だけではこの記憶を抑制できないことも示されており、体性感覚もここまで精巧になると、制御不能になる心配がある。
2021年11月13日
メバルは100歳まで生きると何かで読んで驚いたことがある。以前紹介したキルフィッシュのように(https://aasj.jp/news/watch/4519)、寿命が5ヶ月ぐらいの短命の魚は観察するだけで寿命を特定しやすいが、長寿の魚となると、いくら耳石や鱗で年齢が推定できるとしても、サンプリングを繰り返して統計学的に調べる必要があり、地道な努力の積み重ねでわかってきたことだと思う。
今日紹介するカリフォルニア大学バークレー校からの論文は、この長寿で有名なメバルの仲間、88種類のゲノムを解読し、長寿の秘密を探った研究で11月12日号のScienceに掲載された。タイトルは「Origins and evolution of extreme life span in Pacific Ocean rockfishes(太平洋のメバル属の驚くべき長寿の起源と進化)」だ。
100歳のメバルにも驚いていたが、この論文を読んで我が国でアラメヌケと呼ばれている魚に近いS.Aleutianusではなんと200歳を超える長寿を誇る。この研究では、メバル科88種類のゲノムを解読しているが、各種で寿命は大きく異なり11年から200年まで、驚くほど多様だ。しかし解読されたゲノムのおかげではっきりとした系統関係が描ける。面白いことに、系統関係と寿命はある程度相関しているが、一方向への進化ではなく、それぞれの属の中でも多様性はある。また、系統的に長寿の多い属と離れていても、独自に長寿を獲得している種も存在する。
そこで、寿命が100年以上の種と、20年以下の種を分けてゲノムを比べ、長寿とともに選択されてきた遺伝子をリストすると、長寿とともに選択された遺伝子だけでなんと800種類近く存在し、また選択された、遺伝子は種ごとに異なっている。実際、2種類以上の種でリストされる遺伝子はたかだか15%にとどまっている。すなわち、特定の遺伝子で長寿が達成されるのではなく、それぞれの種で独自に長寿をもたらす遺伝子の進化が起こっていることがわかる。
ではどのような遺伝子が選択されているのか調べると、多くの長寿種で必ず選択される最も効果がありそうなのはDNA2重鎖切断修復に関わる遺伝子群だ。また、これ以外の長寿により選択される遺伝子には、期待通りテロメア、除去修復などに関わる遺伝子がリストされている。これらは長寿との関わりが指摘されており、北極鯨やゾウガメで特定されている遺伝子も含まれている。
もちろん他にも、代謝や炎症に関わる遺伝子もある。そこで、これら長寿遺伝子としてリストされた遺伝子を、体のサイズや、生息深度など、他の進化と関わる遺伝子との関連を調べると、ほとんどはこれらの形質とも相関していることから、生息環境に適応し様々な形質を獲得する中で長寿が達成されていくことがわかる。とはいえ、インシュリンシグナルのように、長寿特異的に残っている遺伝子も10種類ほど特定できている。
こうした中で、寿命とともに遺伝子コピー数が増大する遺伝子も特定されている。免疫チェックポイントに関わるB7と同じファミリーに属するbutyrophilinで、遺伝子コピー数と寿命が見事に相関している。
遺伝子の多様性から計算される個体数や世代時間についても調べ、長寿とともに個体数は大きく低下し、世代時間も延びることを示している。すなわち、長寿のメバルを乱獲してしまうと、取り返しのつかないことになることがわかる。
結果は以上で、ざくっといってしまうと、遺伝子レベルで見ても、長寿は一つの要因で達成できるのではなく、様々な要因が集まった結果としてあることがわかる。今回示された、DNA修復、テロメア、butyrophilinなどの炎症、mTorなどの代謝、低酸素反応などの寿命との関わりは何度も指摘されてきた。しかし、同じファミリーの魚の多様性を利用して比べた結果を見たのは初めてで、機能の確認が全くなくても十分説得力が高い、面白い論文だった。私たちも、長寿遺伝子のデパート:メバルから学ぶことは多い。
2021年11月12日
Amgenが開発したKRAS(G12C)阻害剤Sotorasibについては、長年待望されていたRAS阻害剤がG12C変異に限るとしても、臨床応用にこぎ着けた最初の薬剤として、このHPで紹介し(https://aasj.jp/news/watch/11638 )、さらに特別にYouTubeでも取り上げ(https://www.youtube.com/watch?v=xOe26eCpeoo )、個人的にも大きな期待を寄せていた。事実、この発表はAmgenの株価を大きく上昇させたことは、期待の大きさを物語る。その後、Amgenに続いて、同じメカニズムのKRAS(G12C)阻害剤が加速している。各国の承認についても、つい最近、経済性など厳しい審査の英国NHSが承認したし、我が国厚労省も希少疾患病用医薬品指定を行っており、臨床応用が加速すると考えられる。
ただ、最初の論文から、KRAS(G12C)阻害剤がガンの根治をもたらす可能性は低いことが推察されていた。確かに、KRAS(G12C)変異を持つ患者さんのガンを縮小させ、再発を平均7ヶ月程度抑えることができるが、その後はおそらく薬剤耐性ガンが現れる確率がかなり高い。
今日紹介する米国スローンケッタリング ガン研究所からの論文は、KRAS(G12C)阻害剤治療後の再発を誘導する遺伝子変異について、実際の患者さんと、動物実験系で確かめた研究で11月10日Natureにオンライン発表された。タイトルは「Diverse alterations associated with resistance to KRAS(G12C) inhibition(KRAS(G12C)阻害に対する耐性を誘導する様々な変異)」だ。
この研究では、この治療を受けた43例について、再発例は何らかの方法でガンゲノムをもう一度調べ、再発の遺伝的原因を確かめようとしている。
まずgood newsは、5%の患者さんではガンが完全に消失し、18ヶ月以上再発がない点で、部分縮小の場合でも、同じように再発がない例がさらに5%ほどいることだ。これらの患者さんの特徴を調べると、血中に流れるKRAS(G12C)の量が低く、体内のガン細胞の数が少ないことが想定される。従って、標的薬だからと、最初から使うのではなく、まず一般化学療法などでガンの量を減らしてからKRAS(G12C)阻害剤を使うプロトコルについて治験を行う重要性が示唆される。
このコホートでは、30例の再発があり、そのうち27例については遺伝子変異をキャッチすることに成功している。期待通り、最も多くの耐性につながると想定される変異は、他のRASの変異、あるいはKRAS自体の新しい変異によることが特定されている。しかし、RAS以外にも、様々な遺伝子の変異が再発の原因になっている。
今回特定された全ての変異が耐性に関わるとは思えないが、様々な変異が耐性とともに現れるというのはbad newsで、あらかじめ変異を予想して対応できないことを意味している。一方、RASと下流の変異については、最初から下流のMEKなどを抑制しておくことで、効果が長くなる可能性はある。
これを確かめる意味で、患者さんのガンを移植したマウスにKRAS(G12C)阻害剤を投与し、変異の出現を詳しく調べている。その結果、実験的な耐性獲得では、RASとその下流の新たな変異による場合が多胃ことが明らかになった。また、CRISPRを用いた遺伝子ノックアウトや、MEK阻害剤との併用で、確かにガンをより強く抑制できることが示されている。
結果は以上で、少なくとも2-3割の患者さんの場合、耐性がRASシグナル経路で起こってくることを考えると、最初からKRAS(G12C)阻害剤と、MEK阻害剤との併用は、耐性の出現を抑えるのに役立つように思える。
このように、耐性出現を丹念に追跡することで、新しい治療法が確立できる。今回のレッスンとしては、KRAS(G12C)阻害剤の前に、腫瘍細胞数をできるだけ減らす治療を先行させること、そしてできれば最初から(2-3割しか効果がないとわかっていても)、RAS経路の阻害剤を併用することがわかったと言える。
2021年11月11日
膜上に設置した穴をDNAが動くときに、電流の変化を感知して塩基の種類を判断してDNA塩基配列を決定するナノポアシークエンサーは、エラー率など様々な問題はあるが、その携帯性、簡便性、スピード、さらにディスポーザブルという面で大きなシークエンサーが使えない感染症の現場での利用価値が高まっているように感じる。
今日紹介するデルフト大学からの論文は、同じナノポアシークエンサーを用いてペプチドも読むことができる可能性を示した論文で、現実性はともかく、面白いチャレンジだと思う。タイトルは「Multiple rereads of single proteins at single–amino acid resolution using nanopores(ナノポアを用いて1アミノ酸レベルの解像度で一分子タンパク質を解読する)」で、11月4日Scienceにオンライン掲載された。
要するにナノポアを用いて電流の変化を見る方法で、アミノ酸配列も読めることを示すのが目的だが、そのままアミノ酸をナノポアに加えても何も起こらない。というのも、ナノポアでは穴に入ったDNAを少しづつ動かすためにDNA上を動くヘリカーゼなどのモータータンパク質が必要で、アミノ酸ではこれが働かない(https://www.nature.com/articles/s41598-019-41488-4/figures/1 )。
この問題を、このグループは読みたいペプチドを配列の決まったDNAと結合させ、DNAを動かすことでタンパク質の動きを作る方法を着想している。これはあくまでもアミノ酸を判別すると言うことを確かめるだけの研究なので、つないだアミノ酸はアスパラギン酸とグルタミン酸が並んだ単純な配列のペプチドにしてある。
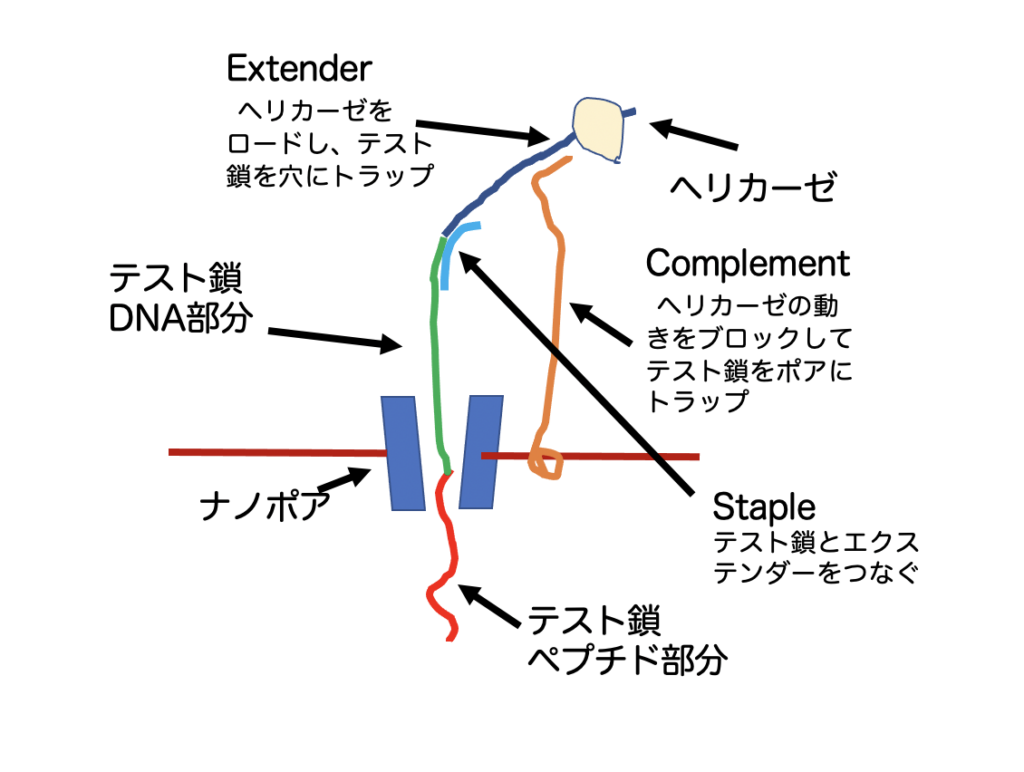
モータータンパクには一本鎖DNAを動かすヘリカーゼHel308を選びDNA部分を滑らせることでアミノ酸を動かせて配列を読むという仕掛けだが、これだけではもちろん足りず、図に示す仕掛けを組み込んでいる。DNA-ペプチド鎖(テスト鎖)をHel308にロードし、さらにナノポアを通すために、テスト鎖にExtenderと呼ぶDNA鎖を、テスト鎖、extender部分に相補的なDNA(Staple)を用いて結合させている。この複合鎖をExtender と相補的部分を持つComplementと呼んでいる、膜から突き出た一本鎖DNAでトラップする。この相補的二重鎖により、ロードされたヘリカーゼは動きを止め、穴にペプチド部分から侵入したテスト鎖が一種宙ぶらりんの状態になる。
このあと、ComplementとStapleの相補的部分を外してやると、ヘリカーゼはExtender とともにナノポアと結合し、挿入されたテスト鎖をDNA部分を用いて引っ張り上げる。このときの電流変化で核酸配列とともに、アミノ酸による電流変化が観察できるという寸法だ。
方法論文なので、図も入れて十分説明できたと思うが、結果はアミノ酸配列により規則的電流変化が見られることが確認され、アスパラギン酸とグルタミンの中に紛れ込ませた、グリシンやトリプトファンを正確に検出できることを示している。また、この変化は基本的にアミノ酸とナノポアの相互作用によるナノポアの変化に起因していることも調べている。
さらに検出の信頼性を示す目的で、同じテスト鎖を、同じナノポアで2回読める工夫をして、同じナノポアであれば、同じ変化が再現されることも確かめている。
以上が結果で、まだまだ実用化とまでは行かないが、1分子アミノ酸配列解読が可能になれば、それがもたらす可能性は計り知れない。
2021年11月10日
非小細胞性未分化ガン、トリプルネガティブ乳ガンなどは、脳転移の確立が高い。そして、脳血管関門など様々な要因で治療が難しく、脳転移は悪い予後を予測する要因となってしまう。確実にガンに届くという意味では、放射線治療が用いられるが、大きく予後を改善するところまでは行っていない。
今日紹介するコーネル大学からの論文は、脳転移腫瘍の放射線治療に対する感受性を、比較的大量に経口摂取するL-アルギニンが大きく高めることを示し、そのメカニズムを探った研究で、11月5日Science Advancesに掲載されている。
アルギニンは、NO産生を通して血流改善だけでなく、細胞の基礎代謝にも大きな影響を及ぼすことから、スポーツサプリにも使われている、明日からでも利用できる物質だ。この論文では、まず実際の臨床例の検討から行っている。
まずアルギニンからNOを合成するNOS2の発現を、非小細胞性未分化ガン、トリプルネガティブ乳ガンで調べると、9割近いガンがNOS2を発現し、そのうち19%は強く発現していること、そして機能的MRIを用いて、アルギニンを5−10g摂取した後24時間で、腫瘍中の乳酸が低下し、ガンの代謝に大きく影響していることを確認している。
この結果を基に、63人の脳転移の患者さんに、照射前にアルギニンを経口摂取させ、その後1日2回の分割照射を、最終的に54.4Gy照射を行っている。治験は無作為化偽薬試験で行っており、放射線以外の治療は受けていない。アウトカムはResponse evalutation criteria in solid tumorsガイドラインに沿ったと書いてあるだけで、長期予後を正確に調べたものではないと思うが、結果は上々で、少なくともcomplete responseが10%対30%、Partial responseが12%対48%と大きく改善し、脳転移に限れば、7割近い患者さんで、50ヶ月以上の再発なしの経過が期待できるというものだ。今後是非大規模な治験と、長期予後に関するデータをとって欲しいと思う。
この研究では、臨床データを示した上で、なぜアルギニン摂取がガンの放射線感受性を高めるのかを調べている。ガンを移植したマウスにアルギニンを投与、1時間でガンを取りだし代謝解析を行うと、解糖系がPhosphoglycerateのステップで抑制され、ピルビン酸、乳酸と合成が低下、TCAサイクルも押さえられ、ガンのエネルギー代謝が押さえられている。
重要なのはこれらの変化のほとんどが、NOを介して起こっている点で、NOS阻害剤で乳酸の合成など代謝異常は正常化する。さらにNOによる代謝異常を追求すると、PhosphoglucerateステップのGAPDHがNOを介してニトロシル化されて長期的に阻害されることを示している。
このようなエネルギー代謝抑制に加えて、同じニトロシル化による機構で、この研究では特定できていないDNA修復分子の抑制が起こる結果、放射線照射後の修復が著しく低下していることも示している。
結果は以上で、元々NOは血管新生による血流改善効果なども知られており、ガンへの薬剤の浸透も助けることから、アルギニンはメカニズムがわかった放射線療法の補助物質として期待できるのではないだろうか。
2021年11月9日
少なくとも我が国では、人間を守るために生活環境をできる限り無菌的にする方向に向かっている。除菌からダニの吸引まで、多くのコマーシャルが日常にあふれていることを見ると、一般家庭レベルでも、清潔な環境を目指す努力が払われている。今回新型コロナ禍は、この努力をさらに加速させただろう。
しかし、清潔であることの副作用も存在する。例えば、アトピーの発生率と石けんの使用量は正比例しているそうだ。今では、赤ちゃんを清潔にと、ゴシゴシ洗うことの問題は広く理解されている。特に私たちと環境をつなぐ腸内細菌叢の研究が進んで、一定の“不潔”が体内に存在することの意義が示されている。
今日紹介するロックフェラー大学からの論文は、日本人の腸から消失した寄生虫も私たちを守ることがあることを示した研究で11月11日号Cellに掲載された。タイトルは「Enteric pathogens induce tissue tolerance and prevent neuronal loss from subsequent infections(腸管の病原体は次の感染に対する組織寛容を誘導し神経喪失を防ぐ)」だ。
正直言って、論文としてはゴチャゴチャして、高いレベルとは思えない。ただ、実験の発想は面白い。
サルモネラの感染は、腸内の神経を傷害して、蠕動異常を誘導してしまうが、このグループは、サルモネラから細胞内での増殖に関わる分子をノックアウトして、病原性をなくすと、今度は次の感染から神経障害を守ること、そして筋肉叢に存在するマクロファージのアルギナーゼArg1が、次の感染から神経を守っていることを突き止めている。
ただ、病原性をエンジニアしたサルモネラの話はここまでで、あとはStrongyloides venezulenesis(Sv)と呼ばれる糞線虫を前もって投与すると、やはり筋層マクロファージのArg1発現などを介して、サルモネラ感染による神経障害を抑えることを確認した後、この過程のより詳しいメカニズムを解析している。
長い話を短くすると、糞線虫が感染すると、このとき自然免疫系を介してCD4T細胞が誘導される。このTh2型免疫反応は、マスト細胞や好中球を局所に誘導して、糞線虫の除去を図るが、このとき同時に筋層のマクロファージを活性化して神経保護作用を発揮する。
ではどの細胞が直接の神経保護作用に関わっているか調べると、T細胞から誘導されるIL-5により好酸球が局所に誘導され、この好酸球が分泌するIL-4やIL-13により、Arg1陽性マクロファージが筋層にリクルートされることが、神経保護作用の背景にあることを明らかにしている。この反応は全て寄生虫への免疫反応なので、この免疫反応が病原菌に対する神経保護作用を準備しているという話になる。
また、この効果は何ヶ月も維持されるが、これは最初のTh2型免疫反応により、骨髄での血液産生が好酸球を多く作るようにリプログラムされ、さらに腸局所の環境が好酸球のさらなる活性化を誘導するようリプログラムされるからだと結論している。
メカニズム解析としては以上が全てだが、この論文で面白かったのは、実験動物として管理されていないペットショップからのネズミを調べようと着想し、実際購入してSPFマウスと比べた実験で、ペットショップのネズミでは、寄生虫などに対する好酸球/IL-4/IL-13型の免疫が維持されており、その結果病原菌感染による神経喪失が完全に防がれていることを示している。
人間でも同じことが言えるなら、現代人からこの機能は完全に失せたことになる。とすると、人為的清潔を求めて、さらにさらに清潔を徹底させ、ひいては世界をSPF化しようとしているのが、文明かもしれない。