2019年10月21日
1型糖尿病(IDDM)は自己免疫病なので、他の自己免疫病と同じでウイルス感染が最初の引き金になる可能性についてはこれまでも議論されてきた。今日紹介するオーストラリア・ウォルター・エリザホール研究所からの論文は、小児の腸炎の最も多い原因であるロタウイルスがIDDMの引き金になる可能性を議論した意見論文でPlos Pathogen に10月10日オンライン掲載された。タイトルは「Does rotavirus turn on type 1 diabetes?(ロタウイルスはIDDMの引き金になるか?)」だ。
さてこの論文は実験論文ではないので、なぜ著者がロタウイルスがIDDMの引き金になると考えているのかについての証拠を一つ一つ紹介しよう。
これまでIDDMの自己抗原として働くことがわかっていたIA-2とGAD65ペプチドと、ロタウイルスのVP7由来ペプチドの一部が類似しており、自己抗原特異的T細胞を刺激する可能性がある。 膵島やインシュリンに対する自己抗体の上昇はロタウイルス抗原に対する抗体と相関していることが多い。 ロタウイルスの感染は膵島を障害することが、様々な動物実験で示されている。 IDDMは20世紀後半から患者さんが増えてきている。これは、保育所で子供がロタウイルスを貰う確率が高まったからとも考えられる。 50万人規模の調査で、ロタウイルスワクチンを受けた子供では、IDDMの発症が41%も低下した。特に、数種類のロタウイルスをカバーするワクチンを接種した子供の方に効果が高い。 以上が著者の考察で、リストされた証拠はかなり説得力がある。もちろん、同じ結果がわが国でも通用するかは、この病気の遺伝リスクの最も重要なものが組織適合性抗原であることを考えると、調べてみないとわからない。いずれにせよ、ロタウイルス自体膵臓の障害もあるとするなら、ワクチン接種は重要な手段として推進する方がいいだろう。
2019年10月20日
今でも、「チンパンジーと人間のゲノムはほとんど変わらないのに」という話を持ち出す人は多い。しかしこのブログでも何度か紹介したと思うが、チンパンジーと人間のゲノムをただ比べて、ただの違いを議論することは時代遅れになっている。代わりに、新しい遺伝子や機能が発生する、比較的大きな欠失や重複を(CNV)調べることの重要性が明らかになり、猿にはないが人間にある新しいCNVの研究が進んでいる。
今日紹介するワシントン大学からの論文は、CNVを人間進化での自然選択を調べるために詳しく調べた論文で10月18日号のScienceに掲載された。タイトルは「Adaptive archaic introgression of copy number variants and the
discovery of previously unknown human genes (古代人のcopy
number variantionの適応的流入を調べていくと新しい人間の遺伝子も見つかる)」だ。
統計学的手法にはもっぱら疎いので詳細は本当は理解できていないのだが、この研究では比較的自民族特有のゲノムが維持されており、またデニソーワ人から流入したゲノム領域が多いメラネシア人に焦点を置き、ネアンデルタール、デニソーワという古代人とともに、アフリカ人(サピエンス以外との交流はない)やその他の様々な人種のゲノムを比べ、それぞれのCNVをリストし、比べている。
もちろん各民族特有のCNVを見つけてそれが選択され新しい遺伝子に変化する様子を調べる研究も可能だが、著者らはこれらのCNVの中からネアンデルタール人、デニソーワ人由来のCNVを選び出し、その中からメラネシア人に高い頻度で見られるが、他の人種には稀にしか存在しないCNV、すなわちメラネシア人の民族形成で自然選択された確率が高いCNVを9種類リストしている。
この研究ではさらにこの中から、16番染色体のp11.1-p11.2領域と、8番染色体のp21.3 領域にそれぞれデニソーワ人、ネアンデルタール人から流入してきたCNVについて詳しくメラネシア人までの遺伝子の変化の歴史を調べている。
詳細は省くが、16番染色体のp11.1/2領域は100-200万年前に起こったNPIP遺伝子のこの領域への挿入により、このサイトが変異のホットサイトにかわり、デニソーワ人で重複や逆位がおこり、このCNVがデニソーワ人から我々の先祖に5万年前に流入し、他のユーラシア人では消え去っても、メラネシアでは高い確率で今も維持されていることがわかった。この領域は、自閉症スペクトラムの変異のホットスポットになっており、メラネシアに維持される変異がこの疾患とどのように関わるかは極めて面白い問題になる。
8番染色体の21.3領域に見られるTNFRSF10の重複はまず類人猿で3千万年前におこる。これによって、チンパンジーでは何種類かのこの分子が存在するが、ネアンデルタール人では新しく2つのTNFRSF10の融合した新しい遺伝子が生まれ、人類では他の遺伝子が非機能的になり、この融合遺伝子のみに集約する。ところが、ネアンデルタール人との交雑であらたに機能的な2種類のTNFRSF10が流入し、メラネシア人だけに流入した遺伝子がなんらかの機能を持って維持されているというシナリオだ。
このような精緻なゲノム解析を組み合わせることで、人間を今起こっている進化の対象として研究できることを示した力作だと思う。また、百万年ぐらいの人間の歴史の中で、新しい遺伝子が発生してくる可能性もよくわかる。もちろん、どのような選択が働いているのかはこの研究からだけでは明確でない。しかし自閉症など、今後見るべきエキサイティングなポイントはゲノムから示された。今後の大きな発展が期待できる予感がする。
2019年10月19日
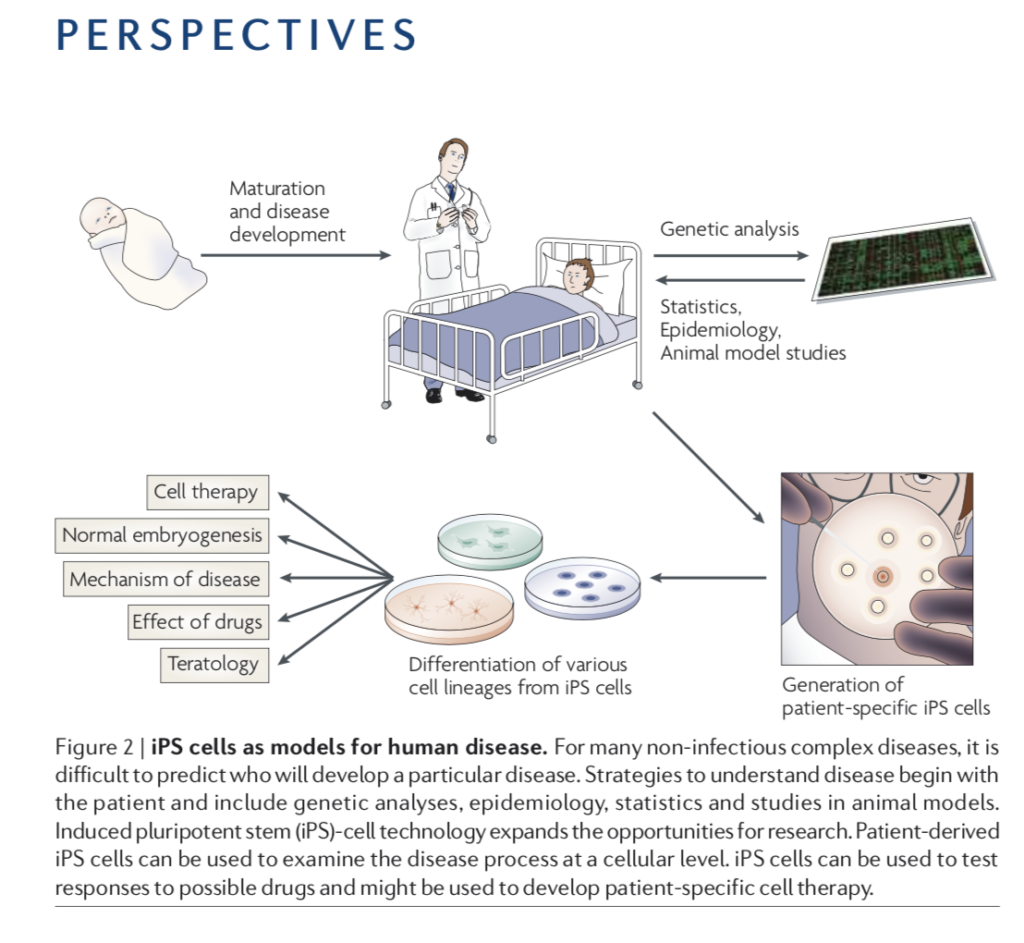
図は、山中さんがヒトiPS作成に成功したあと、私がNature Review Molecular Cell Biologyに米国の1型糖尿病患者団体JDRFの友人と一緒に描いた、iPSへの期待についての論文から転載した図だが、この時患者さんからiPSを作成し、一方でゲノム解析を行って、疾患の成立メカニズムを細胞レベルで調べる研究が大きく発展するのではないかと期待した。この時CRISPR技術は念頭になかったが、その後この技術で遺伝子変異を再構成して調べることも可能になっている。
今日紹介するニューヨーク・マウントサイナイ病院からの論文は、正常iPSに統合失調症と強く相関が見られるSNPや発現量の違いを再構成しようとする研究で疾患iPSを超える可能性にチャレンジした論文だが、読んだ後やはり病気の再構成は統合失調症のような多くの遺伝子が関わる病気については、先は長いという印象を持った。タイトルは「Synergistic effects of common schizophrenia risk variants(統合失調症リスクのコモンバリアント変異は協調的効果を持つ)」だ。
現在まで統合失調症と相関が認められる遺伝子変異は150種類に達しようとしている。異なる遺伝子でも、小さな変異が集まって共通の病気を誘導していると思われるが、さすがにこの小さな変異を集めてという点を細胞レベルで再現するのは難しい。そこで、この研究では、コモンバリアントの中でも特に遺伝子発現の差としてはっきり相関性が認められる遺伝子をまず探し、様々な前駆体タンパク質を活性化するセリンプロテアーゼFurin、およびシナプス形成に関わるSNAP91、TSNARE1に焦点を合わせることを決めている。ただ、この選択は恣意性がないとは言えないと思う。
さて、一番正しい再構成は統合失調症と相関するSNPをゲノムに導入することで、著者らもこれに挑戦しているが、これはまだまだ簡単ではない。というのも、今のところSNPを導入した細胞を選択するのは、個々の細胞の遺伝子を調べる以外に方法はなく、いくらCRISPRでも大変な実験なようだ。最終的には苦労が認められ、このサイトでAAがGGになると、細胞や分化時期で発現が大きく変化することが示され、また神経突起の伸長に異常があることを明らかにしている。すなわち、iPS を用いるとコモンバリアントの細胞レベルでの効果を確かに調べられる。
残念ながら、SNPを導入したのはfurinだけで、あとは細胞レベルの発現の違いをCRISPRで抑制したり、活性化したりする方法で、シナプス形成分子の発現を変えることで、たしかにシナプスでの興奮性が変化することが確認できる。ただ、furinのデータと比べると、インパクトは弱い。
そこで最後に、furinのSNPと、他3種類のシナプス形成分子の発現異常を組み合わせて導入した細胞を、それぞれの変異を持った細胞と比べ、統合失調症の変化を再構成されるか調べている。また、統合失調症患者をはじめとする様々な病気の患者さんの脳細胞のデータと遺伝子発現について比べている。
この再構成実験では機能的検討ができておらず、遺伝子発現のパターンで再現どを評価しているが、全てを合わせたことで、様々な疾患とより強い正の相関を得られることを示している。
結局多くのデータをうまくまとめたという印象があり、またSNP自体を導入するのはやはり大変な実験なので、遺伝子変異を細胞内に再構成するという道のりはまだまだだと思った。その意味で、2008年に期待しように、多くの遺伝子型の細胞を集めて分析することも意外と近道だと確信した。
2019年10月18日
タバコをやめるとメタボになるのは経験済みだが、タバコを吸っている人の方が2型糖尿病が多いという話は私も知らなかったし、それほどポピュラーな話ではないのではないだろうか。ただ、いくつか論文はあるようだ。
今日紹介するニューヨーク・マウントサイナイ医科大学からの論文はラットを用いてニコチンと糖尿病の関係を解析した研究で10月16日号のNatureにオンライン出版された。タイトルは「Habenular TCF7L2 links nicotine addiction to diabetes (脳内側手綱核のTCF7L2はニコチン中毒と糖尿病を結びつける)」だ。
この研究は、脳幹部の内側手綱核でまさに翻訳されつつある遺伝子を調べていたところ、TCF7L2がコリン作動性の神経に強い発現が認められるという発見がきっかけになっている。
内側手綱核はこれまでの研究でニコチン中毒に関わることが知られている。一方タイトルにあるTCF7L2は遺伝子発現を調節する転写因子の一つで、インシュリンの分泌を促すことが知られており、糖尿病に関連する遺伝子の代表として知られている。そこで、著者らはひょっとしたらTCF7L2がニコチン中毒に関わるかも知らないと着想したのだと思う。
TCF7L2 のβカテニン結合サイトを変異させたマウスを用いてニコチンに対する反応を調べると、正常マウスと比べニコチンを入った水を多く飲むようになる。また、クリスパーを用いて手綱核でのTCF7L2をノックアウトすると、やはり同じようにニコチンへの嗜好性が高まる。しかし他の嗜好性は変わらない。すなわち、ニコチン中毒が出たことになる。
この実験系で、糖尿病に関わる様々な因子の手綱核への影響を調べると、GLP-1をブロックするとニコチン嗜好性は低下するが、インシュリン自体は影響がないので、GLP-1が直接手綱核に働いて複雑なネットワークを作っていることを示している。
詳細は省くが、次に生理学的検討を行い、TCF7L2は手綱核のcAMPシグナルを抑制して、アセチルコリン受容体の刺激後の回復を遅らせる結果、TCF7L2の機能低下によりニコチン中毒が発生すると結論している。そして手綱核と糖尿に関して検討し、
手綱核の刺激は交感神経を介して血糖を高めること、 GLP-1は手綱核のTCF7L2の発現を高めて、ニコチンの影響を抑えること、 を明らかにしている。
最後に、ニコチン中毒ラットを作成して、
ニコチン中毒では、血糖が低下した時に見られる炭水化物への欲求が更新すること(Carb cravingとして知られる)、 血糖自体も手綱核のアセチルコリン受容体の作用を抑制して、フィードバックをかけること、 ニコチン中毒ではインシュリンやグルカゴンの分泌が高まっていること、 そして慢性中毒ラットでは血糖が上昇することを示している。 以上が結果で、手綱核がニコチン刺激と血糖や、GLP-1刺激のハブとして複雑なネットワークを形成しており、その結果ニコチン依存が高まると糖尿病の危険が高まることも理解できた。
2019年10月17日
田中耕一さんがノーベル賞に輝いた質量分析の分野は、地味とはいえ生命科学に大きな変革をもたらしている。例えばDNAが完全に分解してしまう恐竜時代のコラーゲンのアミノ酸配列を調べることが可能になり、古生物学や考古学に新しい分野が生まれている。同じように、様々な修飾を受けたタンパク質の定量も可能になり、これまで発現量のみで調べていた細胞内のグローバルな変化を、修飾タンパク質にも広げることができるようになった。
今日紹介するドイツ・ミュンヘンにあるルードヴィヒ・マクシミリアン大学からの論文は、質量分析技術をリン酸化タンパク質の定量に応用して、脳活動とタンパク質のリン酸化との関係を詳しく調べた論文で10月11日号のScienceに掲載された。タイトルは「Sleep-wake cycles drive daily dynamics of synaptic phosphorylation (睡眠と覚醒のサイクルが毎日のシナプスリン酸化の動態を支配している)」だ。
この研究のハイライトは12時間おきに繰り返す夜と昼のサイクルに合わせて、多くのタンパク質がリン酸化のレベルを変化させるという発見に尽きる。タンパク質でみると1600近く、リン酸化されるペプチドでいうと7200を越すサイトがリン酸化のサイクルを繰り返している。実際の図でみると本当に美しい。
また、リン酸化のサイクルも脳の活動をしっかりと反映している。これから覚醒するという時には細胞接着(シナプス)、イオンチャンネル、トランスポーター、水酸化酵素、リン酸化酵素などがリン酸化を受け、これからの電気活動に備える。一方、これから眠るという時には、軸索の伸長、細胞骨格、ユビキチン化、シナプスの細胞学的変化に備えるのにうまくフィットしている。
また、もともと500しかないリン酸化酵素のうち実に128種類が同じようなリン酸化のリズムを刻み、そのうちの65%は活動期にリン酸化される。しかもこのリン酸化のリズムはほとんどがシナプスに限定して起こっている。
最後にこれが遺伝的な概日リズムか、覚醒と睡眠行動にリンクしたものかを、マウスの眠りを妨げる実験で調べ、ほとんどが覚醒・睡眠の実際の行動にリンクしていることを示している。
話はこれだけで、データを見ていると美しいなと納得するが、よく考えると何も驚くことはないという論文だった。できれば、夜と昼で行動性が逆になっている動物などで同じような実験をして加えてくれればと思うが、まあこれだけはっきりしていると現象論でもいいだろうと許してしまう。とはいえ、何がこのリズムの引き金か、やはりフラストレーションは残る。
2019年10月16日
これまで転写というと、長いDNAの上にプロモーターやエンハンサーを配してて、そこに集まる転写因子とRNAポリメラーゼの相互作用として描くのが一般的だった。しかし、ゲノムは核内のタンパク質により濃縮されて折りたたまれており、このヌクレオソーム構造と転写因子実際にはどのように相互作用をするのか、頭の中で想像するのは簡単でなかった。ところが、特定のタンパク質が集まると液晶のように相分離して他のタンパク質から分離できることがわかり、このliquid-liquid phase separation(LLPS )がスーパーエンハンサーなど転写因子の集合の化学的背景としてクローズアップされてきた。これをみて、JT生命誌研究館の平川さんから、是非この問題でジャーナルクラブを考えて欲しいと頼まれた。確かにいい機会なので、11月か12月のいつかLLPSについてジャーナルクラブを開催することにした。
ただこのメカニズムは転写調節にとどまらず、ヌクレオゾームの様々な構造を形成するのにも重要な役割を演じているようだ。今日紹介するテキサス大学からの論文は、試験管内でヌクレオゾーム自体が相分離を起こすことで構成されることを示した研究で10月3日号のCellに掲載された。タイトルは「Organization of Chromatin by Intrinsic and Regulated Phase Separatio(内因的および調節的相分離によるクロマチンの組織化)」だ。相分離の化学としては大変わかりやすい論文なので、ジャーナルクラブではこの論文も詳しく取り上げる。
さて、研究では蛍光ラベルしたヒストン存在下に12個のヌクレオゾームを試験管内で再構成する実験を行い、塩濃度により見事にヌクレオゾームが相分離すること、また塩濃度により相分離した塊の大きさが変化することを発見する。
この発見が研究のハイライトで、あとはDNAやヒストンの条件を変えて、ヌクレオソームが相分離するかどうかを順番に調べている。方法などの詳細はジャーナルクラブの時に譲って、重要なポイントだけを箇条書きにすると次のようになる。
ヌクレオゾームの相分離には、塩濃度だけでなく、ヌクレオゾーム構成分子の様々な条件が絡んでいる。例えば、ヒストンテールが欠失すると、決して相分離は起こらない。 相分離した塊はタンパク質の濃度が高く、構成分子のターンオーバーは極めて緩慢。 ヌクレオソームの間のリンカー部分に結合するヒストンH1は相分離を増強する。 リンカーの長さは、相分離に重要で、リンカーが長すぎると相分離できない。 ヒストンがp300でアセチル化されると、相分離ができなくなる。 しかし、これにBRD分子が存在すると、異なるタイプの構造を持つ相分離がおこる。すなわち、クロマチンだけの相分離した塊と、アセチル化ヒストン+BRDによりそう分離した塊は接触しても決して融合しない。 試験管内だけでなく、核内にヌクレオゾームを注射する実験で、細胞内での分離の様相が観察できる。 などなど、クロマチン形成がまさに物理化学の問題に転換した、ビジュアルでエキサイティングな論文だ。試験管内で相分離したそれぞれの塊は丸いだけだが、じっと見ていると核内でヌクレオゾームが形成されているような気持ちになる。ジャーナルクラブを楽しみにしてほしい。
(これとは別に、今週18日7時からも光遺伝学の新しい進展について岡崎さんとジャーナルクラブを予定しています(https://www.youtube.com/watch?v=_o6cy7lJ_jA ))
2019年10月15日
先日パーキンソン病の患者さんから、超音波によるディスキネジアの治療が始まっていることを聞いた。正直、全くフォローしていなかったので調べてみると、高いエネルギーの超音波をMRIで決めた場所に集中させ細胞を障害する方法(おそらく患者さんが日本で行われていると教えてくれたのはこの方法だろう)と、深部刺激の代わりに用いる低いエネルギーで低い周波数の超音波で刺激する方法(LILFU)の2種類があることがわかった。
しかし後者の方法が深部刺激の代わりになるということは、超音波が神経刺激を誘導することになる。磁気照射なら理解できるのだが、この程度の低いエネルギーの音でなぜ神経を刺激できるのか、理解が難しい。
今日紹介する韓国科学技術研究所からの論文はこの謎に挑んだ研究で10月21日号のCurrent
Biologyに掲載された。タイトルは「Ultrasonic Neuromodulation via
Astrocytic TRPA1 (アストロサイトのTRPA1を介した超音波による神経系の調整)」だ。
超音波で神経が刺激されるとするなら、当然接触や機械的刺激を電気信号に変える受容体TRPA1が重要な働きをしていると想像できる。そこで、TRPA1ノックアウトマウスを
LILFUで刺激すると、正常では確かに神経細胞でCa流入が観察できるのにノックアウトマウスではその反応が低下している。また、普通の細胞にTRPA1を導入すると超音波に反応してカルシウム流入が観察できる。また、他の機械刺激に関わるチャンネルにはこの機能は存在しないことも確認し、LILFUに反応するのはTRPA1であることを確認している。
TRPA1は神経細胞にも、アストロサイトにも発現しているので、アストロサイトと神経を共培養する系でLILFUを照射、アストロサイトのTRPA1がLILFUに反応していることを突き止める。そして、このアストロサイトの興奮が、アストロサイトからのグルタミン酸分泌を促し、神経細胞のシナプスに存在するグルタミン酸受容体を介して神経細胞の活動を変化させることを明らかにしている。
また、LILFUが誘導するアストロサイトへの刺激がどのようなものか、様々な機会的刺激と比較し、最終的にゆっくり細胞を突くような刺激とほぼ同じ効果があることを明らかにしている。
以上が結果で、なぜ特定の超音波が神経活動を変化させられるのか、よく理解できた。こちらの治療はおそらく神経細胞には全く障害性がないことと、電気刺激と比べてグルタミン酸受容体を介した神経活動の変調だけが誘導されるので、もし震えなどの症状が軽減されるなら、安全な治療法として普及するかもしれない。
2019年10月14日
T細胞受容体の本態が明らかになってきた1980年代は、αβT細胞と並んで、発生の初期から腸管などに現れるγδT細胞についても研究は盛んだった。しかし現役を退いてT細胞免疫、特にガン免疫について再度論文を読み始めてわかったのは、一般紙ではγδT細胞についての論文をほとんど目にすることがないことだった。
と思っていたらロンドンのキングスカレッジから乳ガンの増殖を抑えるγδT細胞についての論文がScience Translational Medicineに掲載されているのを見つけた。タイトルは「An innate-like Vδ1 + γδ T cell compartment in the human breast is associated with remission
in triple-negative breast cancer(ヒト乳ガン組織の自然免疫型Vδ1 + γδT細胞はトリプルネガティブ乳ガンの寛解と相関する)」だ。
研究は全てヒトで行われている。まず乳腺組織の様々な場所からT細胞を調整し、正常乳腺にγδT細胞が存在し、そのほとんどがNKG2Dを発現しており、しかもV領域はVδ1を発現していることを発見する。そして、一般的なT細胞と異なり、抗原とは異なる自然免疫に関わるリガンド、γδT細胞の場合NKG2Dのリガンド MICAにより活性化されることを明らかにする。
全く機能的にも同じγδT細胞は乳ガン組織にも存在し、しかも試験管内で乳ガン細胞を障害することができるので、乳ガン免疫に関わるかどうか、トリプルネガティブ乳ガン患者さんを組織内のγδT細胞の多いグループと少ないグループに分けて予後を調べると、多いグループの方がはるかに再発率が低く、生存率が高い。もちろん同じ傾向は、αβT細胞と相関を調べた時も見られるが、γδT細胞は少ない細胞でより高い相関が見られている。
そして何より、ガン免疫には特定のγδT細胞のVδ1配列が必要なわけではなく、基本的にはT細胞受容体とは関係のない刺激により抗がん作用を発揮していることを明らかにしている。
もしこの結果が正しいとすると、ネオ抗原の必要のない、しかしほとんどαβT細胞と同じレベルの細胞障害を、少数の細胞で実現でき、しかも活性化のためのリガンドはいつも同じものを使えることになる。実際の細胞障害性についてはあまり理解できていないが、しかしこれまでなぜ研究されていなかったのか不思議に思ってしまう。おそらくαβT細胞と比べて数が一桁少ないために、あまり気にされなかったのかもしれない。期待したい分野だと思う。
2019年10月13日
現役時代、様々な細胞移植による疾患治療の研究を審査したり、あるいは支援したりしてきたが、マクロファージが原因を問わず肝硬変に効果があるとは考えもしなかった。
今日紹介するスコットランド・エジンバラ大学からの論文は9人の患者さんに末梢血からアフェレーシスで集めたマクロファージを投与したというだけの治験で、安全性の確認を第一のポイントにしている点で第1相試験と考えていい。タイトルは「Safety profile of autologous macrophage therapy for liver cirrhosis (肝硬変に対する自己マクロファージ治療の安全性)」で、10月号のNature Medicineに掲載されている。
もちろん肝硬変の患者さんにマクロファージを投与しても安全でしたという結論だけではNature
Medicineには掲載されないだろう。当然ある程度効果がありそうだと示す必要がある。
治験では、ビリルビンやクレアチンなどのMELDという肝硬変の重症度が10-14(肝臓移植までは必要ないが毎月フォローする必要がある)の患者さんを選び、3人づつに末梢血からCD14の発現を指標にMACSと呼ばれる磁気ビーズを用いた方法で生成したマクロファージを2−4日間M-CSFとともに培養した後、1回だけ1千万、1億、10億個静脈投与して、効果を調べている。
まず安全性だが、胸痛や腹痛など様々な症状が治療中に見られたが、ほとんどはマクロファージ投与とは無関係と考えられ、また投与量とも相関がない。結論的には治療を要する副作用はないとしている。
さて、肝硬変に対する効果だが、まず対照をとった研究ではないのでこれだけで効果を云々することはできないことを断った上で、しかし全ての症例で投与後90日でMELDスコアは低下し、9例中7人が1年後でも治療前より低下していた(平均で1程度の低下)ことから、確かに効きそうだと期待できる。他にも、肝臓の硬さを測るスコア(ELF)、血中3型コラーゲン量などは半分以上の人で改善が認められているが、自覚的な生活の質の上昇にまでは至っていない。
要するに効果があるという結果だが、データを見ると投与した量と比例するELFのようスコアから、コラーゲン量のように投与量とはあまり相関しないスコアまで存在し、最終的な治験をどのようなプロトコルで行うのか、おそらく悩ましいように思う。
結果はこれだけだが、この論文を読んど驚くのは、一般的にはマクロファージは炎症を高め、繊維化を悪化させると思うのに、タンパク質分解酵素を分泌できるという一点に期待して、この治療を動物実験から第1相治験までこぎつけてきたことだ。まだまだ先は長いと思うが、こんな簡単な方法で少なくとも1年間進行が止まるなら、ぜひ普及してほしいと思う。おそらく、細胞免疫療法を手がけるクリニックなら、どこでも実施可能だろう。
2019年10月12日
古代人のゲノム解析は民族の交流の歴史を続々明らかにし、新しい文明の伝播についてはかなり理解が深まってきた。ただ、これらの交流の基礎には必ず村落単位の習慣やしきたりが存在する。
今日紹介するドイツマックスプランク歴史学研究所をはじめとする国際チームからの論文は、ドイツ南部の小さな領域から出土した104体の新石器時代から青銅器時代にかけての人骨をゲノムだけでなく総合的に解析したまさに新しい考古学を感じさせる研究で10月10日号のScienceに掲載された。タイトルは「Kinship-based social inequality in Bronze Age Europe (青銅器時代のヨーロッパに見られた親族関係を基礎とした社会的不平等)」だ。
この研究では骨が出土した様々な考古学的状況(副葬品や場所、時代など)とともに、もちろんゲノム解析による血縁関係、そしてストロンチウムと酸素同位元素を用いた生活していた地域の比較などを組み合わせてそれぞれの骨を解析している。特にストロンチウムと酸素同位元素を用いる方法によると、ある骨が子供時代他の場所に移動し、またその場所に帰ってきたというような移動の歴史まで明らかになる。
出土した骨の時代は、縄目文土器時代、鐘状ビーカー土器、初期青銅器、中期青銅器などの出土品と同位元素による決定されるが、この研究で調べた骨は2750BCから1300BCまでの約1000年にわたってこの地域で生活した人たちになる。
この時代、ヨーロッパでは元々の狩猟採取民がYamnaya、そしてアナトリアからの民族で置き換わるが、実際この地域でも、最初多かったYamnayaゲノムがアナトリア人のゲノムで置き換わることがわかる。
ただこの研究のハイライトはこのようなグローバルな話ではなく、このように大きくゲノムが変化していてもその地域の家族の家族習慣が1000年近く維持されている点だ。
すなわち、同じ場所に埋葬されている骨は、ゲノムから同じ家族と言えるが、そこに両親とともに息子たちの骨は埋葬されているのに、全く娘たちの骨が存在しないという発見だ。また、ストロンチウム同位元素で母親と父親を比べると、父親はその場所で生まれ育っているが、母親は例外なく外部から移ってきていることがわかる。
すなわち女性は早くから他の場所へと移動しそこで結婚する族外婚が確立しており、男性が両親と一緒に暮らす家族形態だったことがわかる。実際、5世代を特定できる家族のゲノムを調べると、男性系統を代表するY染色体は5世代維持される一方、ミトコンドリアは全て変わっていることがわかる。この家族では例外的に、娘も同じ場所に埋葬されているが、副葬品が多く、おそらく裕福な家族で、若く亡くなった場合は同じ場所に埋葬されたと説明している。ただこれは例外で、ほとんどの家族ではこのような例が見られないことから、娘が若くして亡くなっても、同じ場所に埋葬されることはなかったと想像される。
以上の結果は、この時代すでに経済的不平等が発生し、裕福な家庭は富を世襲することが可能で、しかも埋葬に関する一般的なしきたりを破ることができたことを意味するように思える(私見)。大変面白い論文で、新しい考古学を感じさせる研究だった。おそらく考古学からノーベル賞が出るのもそう遠くない話に思える。